Le Cément Dentaire (Histologie)
Article destiné aux étudiants en odontologie — Licence, Master et préparation à l’internat
Introduction : Pourquoi le Cément est-il Incontournable en Odontologie ?
Le cément est l’un des tissus les plus sous-estimés de la sphère oro-dentaire, et pourtant l’un des plus examinés. Situé à l’interface entre la racine dentaire et le ligament parodontal, il joue un rôle central dans l’ancrage, la protection, la réparation et l’adaptation fonctionnelle des dents tout au long de la vie.
Comprendre son histologie, sa composition et ses rôles physiologiques est indispensable pour maîtriser la parodontologie, l’endodontie et la chirurgie orale. Ce guide vous propose une révision complète, structurée et enrichie de cas cliniques pour vous aider à mémoriser efficacement les concepts clés.
Pour approfondir ces notions dans le cadre de votre préparation à l’internat, les Annales corrigées de l’internat en odontologie 2022-2024 constituent une ressource incontournable.
Définition et Place du Cément dans le Complexe Dento-Parodontal
L’organe dentaire, ou complexe dento-parodontal, est une structure fonctionnelle composée de plusieurs éléments étroitement interdépendants. Le cément, l’os alvéolaire et le ligament parodontal (desmodonte) assurent ensemble l’insertion fonctionnelle des dents dans les alvéoles osseux. Cet ensemble joue un rôle clé dans la stabilité et la fonctionnalité des dents face aux contraintes occlusales quotidiennes.
Le cément est un tissu conjonctif minéralisé qui recouvre la surface externe de la racine dentaire. Sur sa face externe, il sert de point d’insertion pour les fibres du ligament parodontal (fibres de Sharpey), assurant ainsi l’ancrage de la dent dans l’alvéole osseuse.
Anatomie du Cément : Localisation, Couleur et Épaisseur
Aspect macroscopique
Lors de l’extraction d’une dent, le cément apparaît comme une couche fine recouvrant la racine. On le distingue visuellement par sa couleur beige crème ou jaune clair, différente de la dentine (plus foncée) et de l’émail (plus clair, brillant et translucide).
Épaisseur variable selon la localisation et l’âge
L’épaisseur du cément n’est pas uniforme. Elle dépend de deux facteurs principaux.
Selon la localisation sur la racine : elle est maximale à l’apex (150 à 200 µm) et plus fine au collet (20 à 50 µm).
Selon l’âge de l’individu : l’épaisseur peut tripler avec le vieillissement, en raison de l’apposition continue de couches cémentaires tout au long de la vie.
Rapports émail/cément à la jonction cervicale
La jonction amélo-cémentaire (JAC) peut prendre trois configurations anatomiques classiques :
- 35 % des cas : émail et cément en bout à bout (jonction franche)
- 60 % des cas : le cément recouvre partiellement l’émail cervical
- 5 % des cas : le cément et l’émail ne se rejoignent pas, laissant la dentine dénudée — cette configuration est cliniquement importante car elle peut provoquer des hypersensibilités dentinaires
Rapports dentine/cément
La jonction dentino-cémentaire est floue en raison de la structure particulière de la couche de Hopewell-Smith et de la couche granulaire de Tomes, deux structures intermédiaires qui rendent la limite difficilement identifiable en microscopie standard.
Comparaison entre le Cément et l’Émail
Tableau comparatif des tissus durs de la dent
Avant d’aborder l’histologie fine du cément, voici un tableau récapitulatif comparant ses propriétés avec celles de l’émail — deux tissus souvent confondus lors des examens :
| Caractéristique | Cément | Émail |
|---|---|---|
| Eau | 32 % | 2,3 % |
| Matière organique | 22 % | 1,7 % |
| Sels minéraux | 46 % | 96 % |
| Dureté | +++ | ++++++ |
| Couleur | Jaune clair | Blanc jaunâtre |
| Translucidité | – | + |
| Texture | Granulée | Lisse |
| Perméabilité | + (colorants vitaux) | – |
| Radio-opacité | ± radio-opaque | + |
| Cellules présentes | Oui (cémentocytes) | Non (acellulaire) |
| Réparation possible | Oui | Non |
À retenir pour l’examen : l’émail est le tissu le plus minéralisé de l’organisme, le cément est le moins minéralisé des tissus durs dentaires — et c’est le seul capable de se réparer.
Formation du Cément : Histogenèse et Cémentogenèse
Différenciation des cémentoblastes
Après la disparition de la gaine épithéliale de Hertwig, les fibroblastes de la couche interne du sac folliculaire, en contact avec la dentine radiculaire, se différencient en pré-cémentoblastes. La dentine radiculaire exerce un pouvoir inducteur déterminant, entraînant une augmentation de la taille des fibroblastes, leur polarisation, leur orientation à 45° par rapport à l’axe de la racine, et leur transformation définitive en cémentoblastes.
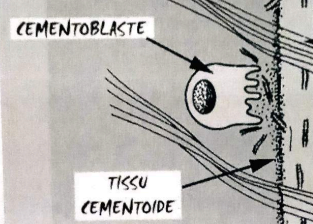
Formation de la matrice organique (tissu cémentoïde)
Les cémentoblastes déposent une matrice organique sur la couche de Hopewell-Smith et autour des faisceaux de fibres ligamentaires. Cette matrice comprend une substance fondamentale, de la sialoprotéine osseuse, de l’ostéopontine, un treillis de collagène intrinsèque (sécrété par les cémentoblastes, orienté parallèlement à la surface radiculaire) et des fibres de collagène extrinsèques d’origine fibroblastique, orientées obliquement ou perpendiculairement à la surface radiculaire.
Minéralisation
La minéralisation se fait progressivement par dépôt de cristaux d’hydroxyapatite. Les sites d’insertion minéralisés des fibres ligamentaires confèrent à la surface du cément un aspect pommelé caractéristique. Le cément acellulaire joue un rôle capital dans l’ancrage de la dent dans l’alvéole osseuse.
Origine des fibres de collagène
Les fibres de collagène du cément ont une double origine : les cémentoblastes (fibres intrinsèques) et les fibroblastes ligamentaires (fibres extrinsèques). La minéralisation forme des lamelles parallèles suivant le contour radiculaire, séparées par des lignes de croissance reflétant le rythme séquentiel de la cémentogenèse.
Formation du cément secondaire (post-éruptif)
Lors de l’éruption dentaire, le cément secondaire se dépose dès le tiers apical de la racine et au niveau des furcations des dents pluriradiculées. Cette cémentogenèse rapide entraîne l’inclusion des cémentoblastes dans leur propre matrice, formant des cémentocytes logés dans des cavités appelées cémentoplastes. Ces cémentocytes possèdent des prolongements cytoplasmiques inclus dans des canalicules péricémentocytaires, assurant les échanges nutritifs. Les fibroblastes desmodontaux synthétisent des fibres collagéniques qui s’unissent aux fibres extrinsèques du cément.
Composition du Cément
Matrice extracellulaire
La trame minérale est composée de sels de phosphate de calcium (hydroxyapatite) et d’oligo-éléments (notamment du fluor). La teneur minérale augmente avec l’âge.
La trame organique est principalement constituée de collagène de type I, associée à des complexes glycoprotéiniques et polysaccharidiques. Elle comprend des fibres intrinsèques (complètement minéralisées, formées par les cémentoblastes), des fibres extrinsèques (incomplètement minéralisées, d’origine desmodontale), ainsi que de l’ostéopontine, de la sialoprotéine osseuse et une substance fondamentale.
Cellules du cément
Cémentoblastes : cellules cuboïdes, polarisées, avec un noyau excentré. Leur cytoplasme est basophile, riche en organites (lysosomes, appareil de Golgi développé, cytosquelette). Ils sont dépourvus de tonofilaments et de jonctions intercellulaires — ce qui les distingue des cellules épithéliales de la gaine de Hertwig. Leur pôle sécrétoire est réversible.
Cémentocytes : cémentoblastes emprisonnés dans leur matrice cémentaire. De forme étoilée, ils sont logés dans des lacunes (cémentoplastes). Leurs prolongements cytoplasmiques relient les cellules entre elles pour assurer le transport des nutriments. Leur équipement intracellulaire s’appauvrit progressivement vers la surface dentinaire, avec persistance de structures vacuolaires et lysosomales. On note la présence de glycosaminoglycanes et de fibres de collagène dans l’espace péricémentocytaire.
Cémentoclastes : cellules volumineuses, multinucléées, situées dans les zones de résorption. Pourvues d’une bordure en brosse et de nombreux lysosomes à forte activité phosphatase acide, elles créent des lacunes de résorption isolées ou confluentes dans le cément.
Types Histologiques du Cément
Le cément se divise en plusieurs types selon sa chronologie de formation, sa cellularité et l’origine des fibres de collagène.
Cément primaire acellulaire
Cément acellulaire à fibres intrinsèques (CAFI) : sécrété par les cémentoblastes, qui produisent une substance fondamentale et des fibres collagènes intrinsèques complètement minéralisées, disposées parallèlement à la surface radiculaire. Il se dépose du collet jusqu’au tiers supérieur de la racine avant la différenciation du ligament parodontal, avec une épaisseur initiale de 15 à 20 µm.
Cément acellulaire à fibres extrinsèques (CAFE) : se forme après la connexion des faisceaux ligamentaires avec la frange fibreuse du cément initial. Il s’étend du collet aux deux tiers coronaux de la racine avec une épaisseur croissante (50 µm au collet, 200 µm à l’apex). En microscopie optique, il apparaît amorphe avec des lignes parallèles (dépôts successifs) et des striations perpendiculaires correspondant aux fibres de Sharpey partiellement minéralisées.
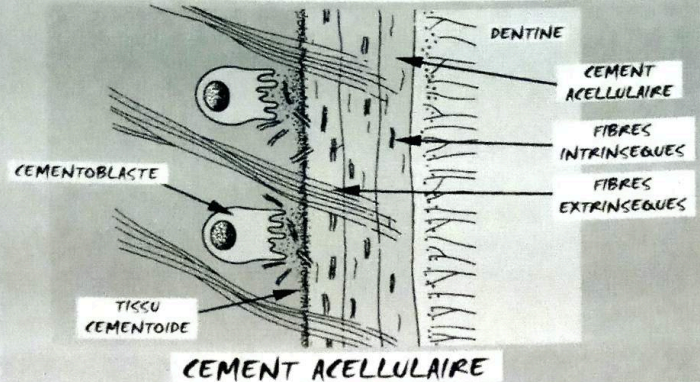
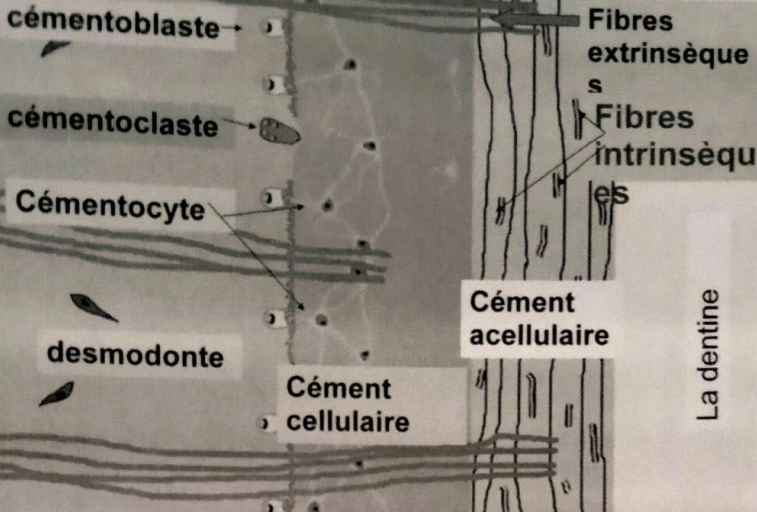
Cément secondaire cellulaire
Constitué d’une substance calcifiée soutenue par des fibres de la matrice, avec des cémentoblastes en surface et des cémentocytes inclus dans des lacunes (cémentoplastes). On y note la présence de glycosaminoglycanes dans les canalicules et des fibres de Sharpey disposées radialement.
Cément cellulaire à fibres intrinsèques (CCFI) : sa sécrétion débute avant l’organisation du ligament parodontal. Il est localisé au tiers apical et dans les régions inter-radiculaires, et se retrouve dans les zones de fractures ou de lacunes de résorption.
Cément cellulaire stratifié mixte (CCSM) : déposé au niveau apical et des furcations avec une formation rapide. Il est composé de trois couches imprévisibles (CCFI + CAFI + CAFE) et résulte d’une adaptation aux mouvements dentaires.
Cément acellulaire afibrillaire (CAAF) : cément particulier, déposé sur l’émail sous forme d’éperons ou de plaques. Dépourvu de collagène, il est issu de la métamorphose des fibroblastes du sac dentaire en cémentoblastes.
Vascularisation et Innervation
Le cément n’est ni vascularisé ni innervé. Il se nourrit exclusivement par diffusion à partir des tissus environnants (desmodonte, dentine). Cette caractéristique explique pourquoi le cément peut se maintenir même sur une dent dépulpée.
Physiologie du Cément : Ses Six Rôles Essentiels
Rôle de protection : le cément recouvre la dentine radiculaire, la protégeant contre les sensibilités dentinaires. Dans les 5 % de cas où la jonction amélo-cémentaire est inexistante, la dentine est exposée et les hypersensibilités sont fréquentes.
Rôle d’ancrage ou de fixation : avec la paroi osseuse et le desmodonte, le cément ancre les fibres ligamentaires (fibres de Sharpey), assurant la fixation de la dent dans l’alvéole osseuse. C’est sa fonction principale.
Rôle d’apposition : le cément s’épaissit tout au long de la vie par dépôt de couches successives. Cette apposition compense l’usure occlusale, maintient la dimension verticale et réagit à l’égression dentaire ou aux traitements endodontiques.
Rôle de réparation : le cément est capable de réparer des fractures radiculaires si le trait de fracture est éloigné du milieu buccal et si les fragments sont maintenus en contact. C’est le seul tissu dur dentaire possédant cette capacité.
Rôle de résorption : la résorption cémentaire est physiologique lors de la rhizalyse des dents temporaires, grâce aux cémentoclastes, en parallèle avec la résorption dentinaire. Elle est pathologique en cas de forces orthodontiques excessives.
Rôle d’échange pulpe/desmodonte : la perméabilité du cément facilite les échanges entre la pulpe et le desmodonte via les canalicules dentinaires et péricémentocytaires.
Rôle de compensation : l’abrasion dentaire et la perte de substance avec l’âge sont compensées par une éruption passive, avec apposition de cément au niveau apical pour maintenir la hauteur coronaire.
Erreurs Fréquentes à Éviter en Histologie du Cément
Erreur 1 — Confondre cémentoblastes et cémentocytes
Beaucoup d’étudiants pensent que cémentoblastes et cémentocytes sont deux types cellulaires distincts d’origine différente. Cette confusion entraîne des erreurs dans la description de la cémentogenèse et du cément secondaire. À retenir : les cémentocytes sont simplement des cémentoblastes emprisonnés dans leur propre matrice lors d’une formation rapide. Ce sont les mêmes cellules à des stades fonctionnels différents.
Erreur 2 — Affirmer que le cément ne subit jamais de résorption
Cette affirmation est inexacte et peut faire perdre des points. La bonne formulation est : le cément permanent ne subit pas de résorption physiologique en conditions normales, mais la résorption existe physiologiquement dans la denture temporaire (rhizalyse) et pathologiquement dans la denture permanente (forces orthodontiques excessives, traumatismes, ankyloses).
Erreur 3 — Oublier les 5 % de jonction amélo-cémentaire “ouverte”
Ne retenir que les deux configurations majoritaires est une erreur fréquente. Ce cas minoritaire a une importance clinique majeure : il explique certaines hypersensibilités dentinaires sans pathologie parodontale apparente. Toujours citer les trois configurations avec leurs pourcentages exacts et leurs conséquences cliniques.
Erreur 4 — Inverser l’origine des fibres intrinsèques et extrinsèques
Cette inversion fausse toute la compréhension de la relation cément/ligament parodontal. Mémoriser : intrinsèque = interne = cémentoblaste ; extrinsèque = externe = fibroblaste du desmodonte. Les fibres extrinsèques correspondent aux fibres de Sharpey dans le cément.
Erreur 5 — Simplifier le cément à deux types seulement
Réduire le cément à “primaire/secondaire” sans connaître la classification fine (CAFI, CAFE, CCFI, CCSM, CAAF) est insuffisant pour les QCM d’internat. Chaque type doit être connu par sa localisation, sa cellularité et l’origine de ses fibres.
Erreur 6 — Sous-estimer le rôle du CAAF
Le cément acellulaire afibrillaire paraît anecdotique parce qu’il est sans collagène, mais il est un marqueur histologique spécifique de la jonction amélo-cémentaire et peut apparaître dans des questions ciblées. Retenir qu’il est issu de la métamorphose des fibroblastes du sac dentaire et qu’il se présente sous forme d’éperons ou de plaques sur l’émail.
Cas Cliniques Commentés
Cas 1 — Hypersensibilité dentinaire cervicale sans pathologie apparente
Présentation : Julien, 32 ans, consulte pour des douleurs vives et brèves sur les dents antérieures inférieures lors de la consommation d’aliments froids. Aucune carie n’est détectée, les gencives sont saines, l’hygiène bucco-dentaire est irréprochable.
Problématique : L’analyse clinique évoque une configuration anatomique rare : une jonction amélo-cémentaire ouverte (5 % des cas), dans laquelle le cément et l’émail ne se rejoignent pas, laissant la dentine cervicale exposée directement au milieu buccal.
Prise en charge : Application de vernis fluoré pour occlure les tubules dentinaires, prescription d’un dentifrice désensibilisant comme le Sensodyne Sensibilité & Gencives, surveillance à 3 et 6 mois.
Résultat attendu : Nette diminution des douleurs en 4 à 6 semaines. Aucune intervention chirurgicale n’est nécessaire à ce stade.
Point pédagogique : Ce cas illustre l’importance clinique des 5 % de jonctions amélo-cémentaires ouvertes, souvent oubliées en cours mais à l’origine de consultations fréquentes.
Cas 2 — Résorption apicale après traitement orthodontique
Présentation : Camille, 19 ans, est en fin de traitement orthodontique par bagues. Le bilan radiologique de fin de traitement révèle des apex légèrement raccourcis sur les incisives supérieures, sans signe clinique particulier.
Problématique : Les images radiologiques suggèrent une résorption apicale externe, impliquant le cément et la dentine apicale, attribuée à des forces orthodontiques prolongées ayant activé les cémentoclastes au-delà du seuil physiologique de tolérance.
Prise en charge : Adaptation du traitement orthodontique (réduction des forces, pause de traitement), surveillance radiologique à 6 mois, contrôle de la vitalité pulpaire.
Résultat attendu : Stabilisation de la résorption. Une légère résorption apicale sans atteinte pulpaire n’a généralement pas de conséquence fonctionnelle à long terme.
Point pédagogique : Ce cas démontre que la résorption cémentaire n’est pas uniquement physiologique et rappelle les limites biologiques des tissus parodontaux face aux contraintes mécaniques excessives.
Cas 3 — Fracture radiculaire et réparation cémentaire
Présentation : Marc, 45 ans, consulte après un traumatisme facial. La radiographie révèle une fracture radiculaire horizontale au tiers moyen de la racine d’une incisive centrale supérieure. La dent est légèrement mobile, la pulpe répond aux tests de vitalité à J0.
Problématique : Le trait de fracture est situé à distance du sulcus et les fragments sont en contact étroit — deux conditions favorables à une réparation par le cément.
Prise en charge : Contention souple pendant 4 semaines, surveillance de la vitalité pulpaire à 1, 3 et 6 mois, radiographies de contrôle à 6 mois et 1 an.
Résultat attendu : Dans des conditions favorables, une cicatrisation par apposition de tissu cémentaire entre les deux fragments est possible.
Point pédagogique : Ce cas illustre concrètement le rôle de réparation du cément — le seul tissu dur dentaire capable de cette réparation intrinsèque — et le différencie de l’émail, totalement incapable de régénération.
Foire Aux Questions (FAQ)
Quelle est la différence entre le cément et l’os alvéolaire ? Bien qu’ils partagent une composition similaire (hydroxyapatite, collagène de type I), le cément et l’os alvéolaire ont des caractéristiques distinctes. L’os alvéolaire est vascularisé, innervé et subit un remodelage permanent. Le cément, lui, n’est ni vascularisé ni innervé, et ne subit pas de remodelage physiologique : il ne fait que s’épaissir par apposition continue tout au long de la vie de la dent.
Pourquoi le cément est-il plus épais à l’apex qu’au collet ? L’apposition de cément est continue et réactionnelle. À l’apex, le cément compense l’usure occlusale et les micromouvements dentaires en se déposant progressivement tout au long de la vie. Cette apposition apicale maintient la dimension verticale d’occlusion malgré l’attrition dentaire. Au collet, l’environnement est plus stable et la pression de formation initiale est moindre.
Le cément peut-il se reformer après une chirurgie parodontale ? Oui, c’est même l’un des objectifs de la régénération tissulaire guidée (RTG). Des cellules du desmodonte conservant des propriétés progénitrices sont capables de se différencier en néo-cémentoblastes et de déposer un nouveau cément sur la surface radiculaire exposée. C’est pourquoi la décontamination soigneuse des surfaces radiculaires est primordiale lors des chirurgies parodontales.
Qu’est-ce que les fibres de Sharpey et quel est leur rôle dans le cément ? Les fibres de Sharpey sont les portions terminales des fibres du ligament parodontal qui s’insèrent dans le cément (et dans l’os alvéolaire). Ce sont les fibres extrinsèques du cément, d’origine fibroblastique. Partiellement minéralisées, elles forment un ancrage mécanique résistant qui transmet les forces occlusales du ligament vers la racine dentaire.
Quelle est la différence entre résorption cémentaire physiologique et pathologique ? La résorption physiologique est normale lors de la rhizalyse des dents temporaires : les cémentoclastes détruisent progressivement le cément et la dentine radiculaire sous l’action des dents permanentes en éruption. La résorption pathologique concerne les dents permanentes : elle peut être provoquée par des forces orthodontiques excessives, des traumatismes, des granulomes périapicaux ou des ankyloses.
Pourquoi une dent dépulpée conserve-t-elle son cément ? Le cément se nourrit principalement par diffusion à partir du ligament parodontal et du desmodonte, et non depuis la pulpe. La suppression de la pulpe n’affecte donc pas directement la nutrition ou la viabilité du cément. C’est pourquoi une dent correctement traitée endodontiquement peut rester ancrée dans son alvéole de façon fonctionnelle pendant de nombreuses années.
Comment distinguer le CAFI du CAFE en histologie ? En microscopie optique, le CAFI apparaît homogène avec des fibres disposées parallèlement à la surface radiculaire. Le CAFE présente des striations perpendiculaires visibles (les fibres de Sharpey), en plus des lignes parallèles des dépôts successifs de cément. La localisation est également différente : le CAFI est plus coronaire et le CAFE s’étend sur les deux tiers de la racine.
Quelles sont les conséquences cliniques d’une hypercémentose ? L’hypercémentose est un épaississement excessif et localisé du cément, souvent apical. Elle peut être idiopathique ou réactionnelle (maladie de Paget, traumatisme, inflammation chronique). Cliniquement, elle complique les extractions dentaires en créant un ancrage renforcé difficile à mobiliser. Elle est généralement asymptomatique et découverte fortuitement sur radiographie.
Conclusion
Le cément est un tissu minéralisé, non vascularisé ni innervé, qui ne subit pas de résorption physiologique à l’état permanent. Il s’épaissit continuellement par apposition de couches successives tout au long de la vie de la dent, qu’elle soit pulpée ou dépulpée. Ce tissu joue un rôle essentiel dans la protection, l’ancrage, la réparation et l’adaptation fonctionnelle des dents.
Maîtriser ses six rôles physiologiques, ses cinq types histologiques et ses caractéristiques cellulaires est indispensable pour tout étudiant en odontologie. Pour aller plus loin, le Référentiel internat en parodontologie approfondit ces notions dans un cadre clinique, et ResiDentaire™ vous permet de vous tester sur des QCM ciblés.
Cette page contient des liens d’affiliation Amazon. En cliquant dessus, vous n’êtes pas tenu de vous procurer les produits suggérés, mais si vous le faites, cela ne vous coûte rien de plus et cela m’aide à financer ce site.



[…] (mécanocepteurs) : Contrôlent les mouvements mandibulaires et l’intensité des forces […]
[…] cycle assure le renouvellement et l’adaptation de l’os alvéolaire aux contraintes […]