Épidémiologie de la Population : Guide Complet en Médecine Dentaire
Introduction : Comprendre l’épidémiologie en santé bucco-dentaire
L’épidémiologie représente un pilier fondamental de la santé publique et de la pratique dentaire moderne. Pour tout étudiant en odontologie, maîtriser ces concepts permet non seulement de comprendre la distribution des maladies bucco-dentaires dans la population, mais aussi d’identifier les facteurs de risque et d’évaluer l’efficacité des interventions préventives.
Cette discipline scientifique, autrefois limitée à l’étude des épidémies infectieuses, s’est considérablement élargie. Aujourd’hui, elle englobe toutes les pathologies bucco-dentaires : caries, maladies parodontales, cancers oraux, malocclusions et bien d’autres affections touchant la cavité buccale.
Dans le contexte actuel de la santé dentaire, l’épidémiologie permet aux futurs praticiens de comprendre pourquoi certaines populations sont plus vulnérables que d’autres, comment les comportements influencent la santé bucco-dentaire, et quelles stratégies de prévention sont les plus efficaces.

Qu’est-ce que l’épidémiologie ? Définitions et évolution historique
Une science en constante évolution
L’épidémiologie est un terme dont la définition n’a cessé d’évoluer au fil des siècles. À l’époque d’Hippocrate, ce terme désignait tout événement affectant une communauté humaine : désastres naturels, guerres, famines. Progressivement, la discipline s’est recentrée sur les phénomènes pathologiques.
Avec l’ère pastorienne et les découvertes en microbiologie au XIXe siècle, l’épidémiologie s’est d’abord concentrée sur les maladies infectieuses. Aujourd’hui, son champ d’application est beaucoup plus vaste, incluant les maladies chroniques, les troubles mentaux, les accidents et même les comportements à risque.
Définitions contemporaines
Définition 1 – Approche causale
L’épidémiologie est la science qui s’intéresse aux causes de survenue des maladies dans la population humaine. Cette définition met en lumière trois axes majeurs :
- L’approche par pathologie (caries, gingivites, parodontites)
- L’approche populationnelle (enfants, adultes, personnes âgées)
- La recherche des causes et facteurs de risque (alimentation, hygiène, tabac)
Définition 2 – Approche distributive
Science qui étudie la distribution des phénomènes de santé dans la population et des facteurs (déterminants) qui conditionnent leurs fréquences. En odontologie, cela permet par exemple de comprendre pourquoi l’incidence des caries a diminué dans les pays développés depuis l’introduction du fluor.
Une science multidisciplinaire
L’épidémiologie est exercée par des spécialistes de divers horizons : médecins, chirurgiens-dentistes, vétérinaires, pharmaciens, biologistes, infirmiers, ingénieurs sanitaires, statisticiens, démographes, géographes, économistes et responsables de santé publique.
Cette diversité reflète la complexité des problématiques de santé publique qui nécessitent une approche holistique et collaborative.
Les quatre types d’épidémiologie en pratique dentaire
Épidémiologie descriptive
Cette branche mesure la fréquence et la distribution des maladies ou phénomènes de santé. En dentisterie, elle permet par exemple de quantifier la prévalence des caries chez les enfants de 6 ans en France ou de cartographier la distribution géographique des cancers de la cavité buccale.
Exemple concret : L’enquête nationale de santé bucco-dentaire menée tous les 10 ans en France permet de mesurer l’évolution de l’indice CAO (Carié, Absent, Obturé) dans différentes tranches d’âge.
Épidémiologie analytique
Elle étudie les causes et les facteurs de risque des maladies. C’est ici que l’on cherche à établir des liens de causalité : le tabac et le cancer oral, le sucre et les caries, le tartre et les maladies parodontales.
Application pratique : Les études cas-témoins permettent de démontrer que les personnes consommant plus de 4 boissons sucrées par jour ont un risque 3 fois supérieur de développer des caries multiples.
Épidémiologie évaluative
Elle mesure les effets et l’impact des actions de santé. En odontologie, cela peut concerner l’évaluation de programmes de prévention comme la fluoration de l’eau, les campagnes de dépistage ou les programmes de scellement des sillons.
Exemple d’application : Évaluer si une campagne de sensibilisation au brossage dans les écoles a effectivement réduit l’incidence des caries après 2 ans.
Épidémiologie prédictive
Elle étudie par anticipation la probabilité de survenue ou d’évolution future des maladies. Cette approche est particulièrement utile pour la planification des besoins en soins dentaires et la formation des professionnels.
Utilité pour les étudiants : Comprendre les tendances démographiques permet d’anticiper les besoins futurs en gériatrie dentaire avec le vieillissement de la population.
Les champs d’étude de l’épidémiologie dentaire
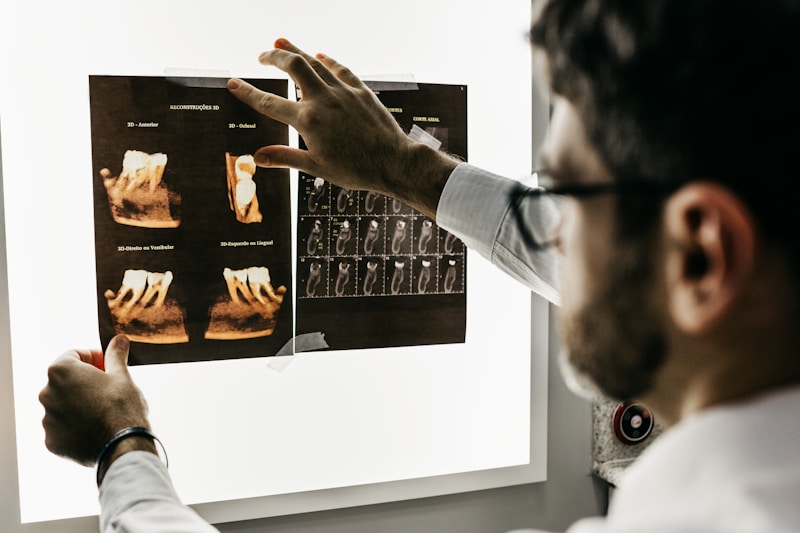
Approche par pathologie
Cette approche vise à améliorer les états de santé et allonger la durée de vie en bonne santé bucco-dentaire. Elle englobe :
- Maladies infectieuses : candidoses orales, herpès labial, infections bactériennes
- Pathologies carieuses : caries coronaires, radiculaires, récurrentes
- Maladies parodontales : gingivites, parodontites chroniques et agressives
- Lésions précancéreuses et cancers : leucoplasies, érythroplasies, carcinomes épidermoïdes
- Traumatismes dentaires : accidents, violences, sports de contact
- Troubles de l’occlusion : malocclusions, dysfonctions temporo-mandibulaires
Approche populationnelle
Elle étudie des groupes humains spécifiques pour en tirer des points communs et adapter les stratégies de prévention :
- Femmes enceintes et périnatalité : risques de gingivite gravidique, transmission bactérienne mère-enfant
- Nourrissons et enfants : caries du biberon, éruption dentaire, prévention précoce
- Adolescents : orthodontie, traumatismes, piercing buccaux
- Personnes âgées : édentement, xérostomie, pathologies muqueuses
- Personnes en situation de handicap : accès aux soins, besoins spécifiques
Approche par facteurs de risque
Cette dimension permet de mesurer l’impact et prévenir les pathologies en identifiant les populations vulnérables :
- Travailleurs exposés : industrie sucrière, boulangerie (exposition à la farine et au sucre)
- Groupes à risque : fumeurs, diabétiques, immunodéprimés
- Comportements à risque : consommation excessive de sucre, tabac, alcool, drogues
- Conditions socio-économiques : précarité, accès limité aux soins
| Approche | Objet | Exemple |
|---|---|---|
| Par pathologie | Améliorer les états de santé, allonger la durée de vie en bonne santé | Maladies infectieuses, psychiatriques ou mentales, génétiques, pollutions, accidents de la voie publique (AVP), violences, etc. |
| Populationnelle | Étudier des groupes humains voire l’ensemble de la population afin d’en tirer des points communs | Femmes et périnatalité, personnes âgées et dépendance |
| Par la recherche de causes ou de facteurs de risque | Mesurer l’impact, prévenir | Travailleurs et risques professionnels, groupes à risque : jeunes et comportements à risque, etc. |
Les objectifs de l’épidémiologie pour le chirurgien-dentiste
L’épidémiologie ne se limite pas à la recherche académique. Elle a des applications concrètes pour la pratique clinique quotidienne :
- Mesurer l’état de santé d’une population : Connaître la prévalence des pathologies dans sa zone d’exercice
- Mesurer les risques individuels et collectifs : Identifier les patients à haut risque carieux ou parodontal
- Identifier les agents pathogènes et modes de transmission : Comprendre l’étiologie des infections orales
- Prévenir la survenue des maladies : Élaborer des stratégies préventives personnalisées
- Évaluer les méthodes d’intervention : Vérifier l’efficacité des traitements et protocoles
Ces objectifs permettent au praticien d’adopter une approche fondée sur les preuves (Evidence-Based Dentistry) et d’optimiser la qualité des soins prodigués.
Mesurer l’état de santé bucco-dentaire d’une population
Les indicateurs démographiques essentiels
Pour comprendre les besoins en santé bucco-dentaire, il est indispensable de connaître la structure démographique de la population étudiée.
Indicateurs d’état (image statique de la population)
Pyramide des âges
Représentation graphique de la répartition par âge et sexe qui permet d’anticiper les besoins futurs. Une population vieillissante nécessitera davantage de prothèses et de traitements parodontaux, tandis qu’une population jeune demandera plus de soins préventifs et orthodontiques.
Proportion des personnes âgées
Calculée comme le rapport entre le nombre de personnes de 65 ans et plus et la population totale. En France, cette proportion atteint environ 20% en 2024, ce qui explique l’importance croissante de la gérodontologie.
Rapport de dépendance
Rapport entre l’effectif des enfants et des personnes âgées de 65 ans et plus et la population d’adultes actifs. Cet indicateur influence directement la capacité d’une société à financer les soins de santé.
Autres indicateurs socio-économiques
- Niveau de revenu moyen
- Taux de chômage
- Catégories socio-professionnelles
- Niveau d’éducation
Ces variables sont fortement corrélées à l’état de santé bucco-dentaire. Les populations défavorisées présentent généralement des indices CAO plus élevés et un accès aux soins plus limité.
Indicateurs de mouvement (dynamique démographique)
Taux brut de natalité
Mesure le nombre de naissances vivantes pour 1000 habitants.
Exemples internationaux (données 2024) :
- France : 10,9 pour mille
- Algérie : 16,6 pour mille
- Bénin : 41,1 pour mille
Un taux de natalité élevé implique des besoins importants en pédodontie et en prévention précoce.
Indice synthétique de fécondité
Nombre moyen d’enfants par femme :
- France : 1,8 enfant/femme
- Algérie : 2,3 enfants/femme
- Bénin : 5,9 enfants/femme
Espérance de vie à la naissance
Reflète l’état de santé général d’une population :
- France : 82,5 ans (moyenne hommes-femmes)
- Algérie : 77 ans
- Bénin : 61,5 ans
Une espérance de vie croissante augmente les besoins en soins dentaires pour personnes âgées.
Taux brut de mortalité
Nombre de décès pour 1000 habitants :
- France : 9,1 pour mille
- Algérie : 4,7 pour mille
- Bénin : 13,5 pour mille
Taux de mortalité infantile
Nombre de décès d’enfants de moins de 1 an pour 1000 naissances vivantes :
- France : 3,8 pour mille (2024)
- Algérie : 21,0 pour mille
- Bénin : 86,7 pour mille
Cet indicateur reflète la qualité du système de santé et l’accès aux soins préventifs.
Taux de mortalité maternelle
Nombre de décès maternels pour 100 000 naissances vivantes :
- France : 7,0 pour 100 000
- Algérie : 112 pour 100 000
- Bénin : 397 pour 100 000
Bien que ce soit un indicateur de santé générale, il influence indirectement la santé bucco-dentaire des nourrissons par le biais du suivi prénatal et postnatal.
Les mesures de base en épidémiologie dentaire
À partir du nombre de cas et de la taille de la population, plusieurs types de mesures peuvent être calculés. Chacune a sa spécificité et son utilité en recherche et en pratique clinique.
La proportion
Formule : P = a / (a + b)
Le numérateur est une partie du dénominateur. Les deux sont de même nature.
Expression : Nombre entre 0 et 1, ou pourcentage (%, ‰, pour 10 000, etc.)
Exemple en dentisterie
Dans une école primaire de 500 élèves de 6 ans, 380 ont au moins une dent cariée.
Proportion d’enfants atteints = 380 / 500 = 0,76 = 76%
Interprétation : 76% des enfants de 6 ans de cette école présentent au moins une carie. Cette information guide les actions de prévention à mettre en place.
Le ratio (ou rapport)
Définition : Rapport entre les effectifs de deux classes d’une même variable, mais exclusives l’une de l’autre.
Exemple en dentisterie
Dans un cabinet dentaire, sur 200 nouveaux patients atteints de maladie parodontale :
- 80 sont des hommes
- 120 sont des femmes
Sexe-ratio = 80 / 120 = 0,67
Interprétation : Il y a 0,67 homme pour 1 femme, soit environ 2 femmes pour 3 hommes atteints de maladie parodontale dans ce cabinet.
La cote (ou odds)
Formule : Ratio de la probabilité de survenue d’un événement sur la probabilité de non-survenue.
Utilisation : Principalement dans les enquêtes étiologiques pour mesurer l’exposition à un facteur de risque.
Exemple en dentisterie
Lors d’une épidémie d’intoxication alimentaire suite à un repas de gala, 45 patients se plaignent de symptômes digestifs. Parmi eux :
- 32 ont consommé la mousse au chocolat
- 13 n’en ont pas consommé
Cote d’exposition = 32 / 13 = 2,46
Interprétation : Il y a 2,46 cas exposés (ayant mangé la mousse) pour 1 cas non exposé. La mousse au chocolat est probablement l’aliment responsable.
Note : Bien que cet exemple ne soit pas strictement dentaire, le principe s’applique à l’identification des facteurs de risque en santé bucco-dentaire.
L’indice
Définition : Rapport de deux effectifs de nature différente.
Utilisation : Indicateurs de fonctionnement, notamment en économie de la santé et organisation des soins.
Exemples en odontologie
- Patients par praticien : 1500 patients / 1 dentiste = 1500 patients par dentiste
- Fauteuils par cabinet : 30 cabinets avec 75 fauteuils = 2,5 fauteuils par cabinet
- Assistantes par praticien : 50 dentistes, 35 assistantes = 0,7 assistante par dentiste
- Consultations par jour : 200 consultations / 20 jours ouvrés = 10 consultations par jour
Ces indices aident à évaluer la charge de travail et l’organisation du cabinet.
Le taux
Définition : Mesure de la fréquence de survenue d’un événement au cours d’une période donnée.
Composantes :
- Numérateur : Nombre d’occurrences de l’événement pendant une période déterminée
- Dénominateur : Population susceptible de connaître cet événement pendant cette période
Exemple en dentisterie
Taux d’incidence des abcès dentaires dans une population de 10 000 personnes suivies pendant 1 an :
- Nouveaux cas d’abcès : 150
Taux d’incidence = 150 / 10 000 = 0,015 = 1,5%
Ou 15 pour 1000 personnes-année.
Les indicateurs de morbidité en santé bucco-dentaire
La prévalence : mesurer le poids de la maladie
Prévalence absolue : Nombre total de cas existants (nouveaux et anciens) à un moment donné.
Prévalence (taux) : Nombre de cas existants / population à risque à un instant donné.
Caractéristiques
- Photographie instantanée d’un phénomène
- N’est pas un véritable taux de risque
- Particulièrement utile pour les maladies chroniques de longue durée
- Mesure le poids de la maladie pour la société
- Essentielle pour la planification sanitaire et l’allocation des ressources
Formule
Prévalence = Nombre de cas observés à l’instant t / Population à risque à l’instant t
Expression : Entre 0 et 1, ou en pourcentage (pour 100, 1000, 10 000, etc.)
Exemple en dentisterie
Lors d’un dépistage dans une entreprise, 250 employés sur 1000 présentent une maladie parodontale (gingivite ou parodontite).
Prévalence = 250 / 1000 = 0,25 = 25%
Interprétation : Un quart des employés souffre d’une pathologie parodontale. Cette information justifie la mise en place d’un programme de prévention et de sensibilisation au sein de l’entreprise.
Application clinique
La prévalence de la carie dentaire chez les enfants de 12 ans en France est passée de 4,2 dents cariées en 1987 à 1,2 en 2006, illustrant l’efficacité des politiques de prévention (fluor, scellements de sillons, éducation à l’hygiène).
L’incidence : mesurer la dynamique épidémiologique
Incidence : Nombre de nouveaux cas d’une maladie durant une période donnée.
Taux d’incidence (incidence cumulée) : Nombre de nouveaux cas / population moyenne exposée au risque durant la période.
Intérêt
- Mesure la force de la poussée épidémiologique
- Reflète le risque de contracter la maladie
- Permet d’évaluer les changements dans l’exposition aux facteurs de risque
Formule
Incidence = Nouveaux cas pendant Δt / Population à risque pendant Δt
Expression : Nombre de nouveaux cas pour 100, 1000 ou 10 000 personnes-temps
Exemple en dentisterie
Dans une école de 800 élèves suivis pendant 2 ans, 160 nouveaux cas de caries sont diagnostiqués chez des enfants qui n’en avaient pas au début de l’étude.
Incidence = 160 / 800 = 0,20 = 20%
Interprétation : Sur 2 ans, 20% des enfants initialement indemnes ont développé au moins une carie.
Taux d’attaque
Identique au taux d’incidence mais pour une très courte période (quelques jours ou semaines). Particulièrement utile pour la surveillance des épisodes épidémiques aigus.
Exemple : Lors d’une épidémie de stomatite herpétique dans une crèche, 15 enfants sur 40 développent la maladie en 1 semaine.
Taux d’attaque = 15 / 40 = 37,5%
Les indicateurs de mortalité en épidémiologie
Bien que la mortalité directement liée aux pathologies bucco-dentaires soit rare dans les pays développés, certains indicateurs restent pertinents, notamment pour les cancers oraux et les complications infectieuses.
Taux brut de mortalité
Formule : Nombre de décès durant une période / population moyenne durant cette période
Exemple général : France 2024 ≈ 9,1 décès pour 1000 habitants
Taux de mortalité spécifiques
Selon l’âge : Nombre de décès dans une tranche d’âge / effectif moyen de cette tranche
Selon le sexe : Nombre de décès masculins / effectif moyen des hommes
Selon la cause : Nombre de décès par cancer oral / population moyenne
Exemple en dentisterie
En France, le taux de mortalité par cancer de la cavité buccale et du pharynx est d’environ 3,5 pour 100 000 habitants chez les hommes et 0,8 pour 100 000 chez les femmes (données 2023). Ces chiffres soulignent l’importance du dépistage précoce et de la lutte contre le tabagisme.
Taux de létalité
Définition : Nombre de décès dus à une maladie / nombre de personnes atteintes par cette maladie
Formule pour maladie stable : Décès attribuables à une maladie / nouveaux cas pendant la période
Exemple en dentisterie
Le taux de létalité du carcinome épidermoïde de la cavité buccale à 5 ans est d’environ 50%, variant selon le stade au diagnostic. D’où l’importance cruciale du dépistage précoce lors des examens dentaires de routine.
Taux de mortalité proportionnel
Formule : Décès dus à une maladie donnée / nombre total de décès
Cet indicateur permet de mesurer le poids relatif d’une cause de décès dans l’ensemble de la mortalité.
Indicateurs de mortalité périnatale et infantile
Bien qu’ils ne soient pas spécifiques à la dentisterie, ces indicateurs reflètent la qualité du système de santé global qui influence indirectement la santé bucco-dentaire.
Taux de mortalité infantile
Nombre d’enfants décédés avant 1 an durant l’année N / naissances vivantes durant l’année N
Taux de mortinatalité
Nombre de fœtus ≥ 28 SA nés sans vie / naissances totales
Taux de mortalité périnatale
Décès entre 28 SA et 7 jours / naissances totales
Taux de mortalité néonatale
Nouveau-nés décédés avant 28 jours / naissances vivantes
Périodes critiques
28 SA → Naissance → J7 → J28 → 1 an
Ces périodes permettent d’identifier les moments où les interventions de santé publique sont les plus cruciales.
Standardisation des taux : comparer l’incomparable
La standardisation permet de comparer des indicateurs entre différents groupes de population ou différentes périodes en tenant compte des différences de structure démographique, notamment l’âge.
Pourquoi standardiser ?
Les populations ont des structures d’âge différentes. Une population âgée aura naturellement plus de pathologies chroniques qu’une population jeune. Pour comparer équitablement, il faut “neutraliser” l’effet de l’âge.
Standardisation directe
Principe : Appliquer les taux observés dans chaque classe d’âge de la population étudiée à une population de référence (généralement la population mondiale 2000).
Méthode
- Calculer le taux de morbidité/mortalité par classe d’âge dans la population étudiée
- Multiplier chaque taux par l’effectif correspondant dans la population de référence
- Additionner les cas attendus
- Diviser par l’effectif total de la population de référence
Avantage : Permet de comparer directement plusieurs populations
Inconvénient : Nécessite de connaître les taux spécifiques par âge
Standardisation indirecte
Principe : Appliquer les taux de référence à la population étudiée.
Méthode
- Appliquer les taux de référence (par exemple, taux nationaux) à chaque classe d’âge de la population étudiée
- Calculer le nombre de cas attendus
- Comparer au nombre de cas observés
- Calculer le rapport standardisé de morbidité (RSM) ou de mortalité (RSM)
Formule RSM
RSM = (Cas observés / Cas attendus) × 100
- RSM > 100 : surmortalité/surmorbidité
- RSM = 100 : mortalité/morbidité conforme à la référence
- RSM < 100 : sous-mortalité/sous-morbidité
Avantage : Nécessite moins de données détaillées
Inconvénient : Ne permet pas de comparer directement deux populations entre elles
Exemple en dentisterie
Pour comparer l’incidence des caries entre deux régions ayant des structures d’âge différentes, on applique soit les taux d’incidence régionaux à une population de référence (directe), soit les taux nationaux aux populations régionales (indirecte).
Les sources de données en épidémiologie dentaire
Pour les indicateurs démographiques
Recensement de la population
Réalisé tous les 5 à 10 ans selon les pays, il fournit des données exhaustives sur la structure de la population : âge, sexe, profession, lieu de résidence, niveau d’éducation.
En France, l’INSEE (Institut National de la Statistique et des Études Économiques) réalise un recensement continu depuis 2004.
Pour les indicateurs de morbidité
Sources permanentes exhaustives
- Registres de maladies : Certaines pathologies font l’objet d’un enregistrement systématique (cancers, diabète, insuffisance rénale chronique). En dentisterie, il existe des registres de cancers oraux dans certains pays.
- Systèmes de surveillance : Déclaration obligatoire de certaines maladies transmissibles
Sources permanentes par échantillonnage
- Réseaux sentinelles : Groupe de professionnels volontaires qui rapportent systématiquement certaines pathologies
- Panels de cabinets dentaires : Participation volontaire pour recueillir des données épidémiologiques
Sources périodiques par échantillonnage
- Enquêtes nationales de santé : Menées régulièrement pour évaluer l’état de santé bucco-dentaire (exemple : enquête UFSBD en France)
- Enquêtes en milieu scolaire : Dépistages organisés dans les écoles pour mesurer la prévalence des caries
- Études spécifiques : Recherches ponctuelles sur des problématiques particulières
Sources basées sur le recours aux soins
- Bases de données de l’Assurance Maladie : Enregistrement de tous les actes remboursés, permettant d’analyser la consommation de soins
- Dossiers hospitaliers : Données sur les hospitalisations pour pathologies bucco-dentaires sévères
- Registres de cabinets privés : Données collectées lors de la pratique quotidienne (avec consentement des patients)
Pour les indicateurs de mortalité
Certificats de décès
Documents médicaux obligatoires remplis par un médecin lors de chaque décès, précisant :
- La cause immédiate du décès
- Les causes intermédiaires
- La cause initiale (celle retenue pour les statistiques)
- Les facteurs contributifs
Ces certificats sont centralisés et permettent d’établir les statistiques de mortalité par cause.
Registres de cancers
Enregistrement systématique de tous les nouveaux cas de cancers, incluant les cancers de la cavité buccale, avec suivi de l’évolution et de la survie des patients.
Les facteurs de risque en santé bucco-dentaire

Définitions fondamentales
Risque : Probabilité qu’un événement (maladie, complication) survienne dans une population ou chez un individu durant une période donnée.
Facteur de risque : Caractéristique d’un individu ou de son environnement associée statistiquement à une probabilité accrue de développer une maladie ou un événement particulier.
Les facteurs de risque peuvent être :
- Modifiables : tabac, alimentation, hygiène bucco-dentaire
- Non modifiables : âge, sexe, génétique
Typologie des facteurs de risque de maladies bucco-dentaires
Facteurs alimentaires
Maladie : Carie dentaire
Facteurs de risque
- Consommation excessive de sucres fermentescibles (saccharose, glucose, fructose)
- Fréquence élevée de prises alimentaires sucrées (plus de 4 par jour)
- Grignotage entre les repas
- Consommation régulière de boissons acides (sodas, jus de fruits)
- Alimentation pauvre en calcium et en vitamine D
Exemple concret : Un enfant qui boit régulièrement des boissons sucrées au coucher multiplie par 5 son risque de développer des caries précoces.
Facteurs comportementaux
Maladie : Maladies parodontales
Facteurs de risque
- Tabagisme (actif et passif)
- Absence de brossage régulier (< 2 fois par jour)
- Non-utilisation du fil dentaire ou des brossettes interdentaires
- Absence de suivi dentaire régulier
- Stress chronique (favorise le bruxisme et compromet l’immunité)
Exemple concret : Les fumeurs ont un risque 3 à 6 fois supérieur de développer une parodontite sévère par rapport aux non-fumeurs.
Maladie : Cancer de la cavité buccale
Facteurs de risque
- Tabagisme (cigarette, pipe, cigare, chicha)
- Consommation excessive d’alcool (effet synergique avec le tabac)
- Chique de bétel (Asie du Sud-Est)
- Mauvaise hygiène bucco-dentaire
- Exposition solaire excessive (cancer des lèvres)
- Infection par le papillomavirus (HPV 16 et 18)
Chiffre clé : Le risque de cancer oral est multiplié par 100 chez les grands fumeurs-buveurs.
Facteurs iatrogènes (liés aux soins)
Maladie : Infections nosocomiales
Facteur de risque : Mauvaise hygiène dans le lavage des mains du personnel soignant, stérilisation inadéquate des instruments
Maladie : Résistance bactérienne
Facteur de risque : Prescription inadaptée d’antibiotiques à large spectre, automédication, non-respect de la durée du traitement
Prévention : Appliquer strictement les protocoles d’hygiène, utiliser des antibiotiques seulement quand nécessaire, respecter les recommandations de bonne pratique.
Facteurs environnementaux et professionnels
Maladie : Érosion dentaire professionnelle
Facteur de risque : Exposition professionnelle à des vapeurs acides (industrie chimique, galvanoplastie, batteries)
Maladie : Fluorose dentaire
Facteur de risque : Exposition excessive au fluor durant la période de formation de l’émail (eau de boisson, suppléments, dentifrices)
Maladie : Traumatismes dentaires
Facteur de risque : Pratique de sports de contact sans protège-dents (rugby, boxe, hockey)
Prévention : Port systématique de protège-dents sur mesure lors des activités à risque.
Facteurs génétiques et médicaux
Maladies parodontales génétiques : Certaines formes agressives de parodontites sont associées à des polymorphismes génétiques (gène IL-1)
Diabète : Les diabétiques mal équilibrés ont un risque 3 fois supérieur de parodontite sévère
Immunodépression : VIH, traitements immunosuppresseurs, chimiothérapie augmentent le risque de candidoses orales et de gingivites ulcéro-nécrotiques
Xérostomie médicamenteuse : Plus de 500 médicaments réduisent la sécrétion salivaire, augmentant le risque carieux
Syndrome de Gougerot-Sjögren : Maladie auto-immune causant une sécheresse buccale sévère
| Type de facteurs | Maladie | Facteur de risque |
|---|---|---|
| Alimentaires | Artériosclérose | Consommation excessive de graisses animales |
| Comportementaux | SIDA | Échanges de seringues |
| Comportementaux | Cancers pulmonaires | Tabagisme |
| Iatrogènes | Infections nosocomiales | Mauvaise hygiène dans le lavage des mains |
| Iatrogènes | Infections à bactéries multirésistantes (BMR) | Antibiotiques à large spectre |
| Environnementaux | Saturnisme | Exposition aux peintures de plomb |
| Environnementaux | Mésothéliome | Exposition à l’amiante |
La mesure du risque : le risque relatif (RR)
L’épidémiologie permet non seulement d’identifier les facteurs de risque, mais aussi de mesurer et quantifier la force de l’association entre une exposition et une maladie.
Définition du risque relatif
Le Risque Relatif (RR) est le rapport de l’incidence d’une maladie chez les personnes exposées sur l’incidence chez les personnes non exposées.
Formule
RR = Incidence chez les exposés / Incidence chez les non-exposés
Interprétation du RR
- RR = 1 : Pas d’association entre l’exposition et la maladie
- RR > 1 : L’exposition augmente le risque de maladie (facteur de risque)
- RR < 1 : L’exposition diminue le risque de maladie (facteur protecteur)
Plus le RR s’éloigne de 1, plus l’association est forte.
Intervalle de confiance à 95% (IC 95%)
L’IC 95% indique la précision de l’estimation du RR.
- Si l’IC 95% inclut 1 : l’association n’est pas statistiquement significative
- Si l’IC 95% exclut 1 : l’association est statistiquement significative
Exemple détaillé en santé bucco-dentaire
Question de recherche : Le tabagisme est-il un facteur de risque de parodontite ?
Étude de cohorte
- Groupe exposé : 500 fumeurs sans parodontite au début de l’étude
- Groupe non exposé : 500 non-fumeurs sans parodontite au début de l’étude
- Suivi : 5 ans
Résultats
Après 5 ans :
- 150 fumeurs ont développé une parodontite → Incidence = 150/500 = 0,30 = 30%
- 50 non-fumeurs ont développé une parodontite → Incidence = 50/500 = 0,10 = 10%
Calcul du RR
RR = 0,30 / 0,10 = 3,0
IC 95% = [2,2 – 4,1]
Interprétation
Les fumeurs ont un risque 3 fois supérieur de développer une parodontite par rapport aux non-fumeurs. L’association est statistiquement significative (IC 95% exclut 1). Le tabagisme est donc un facteur de risque majeur de parodontite.
Exemple académique : VIH et tuberculose
Pour évaluer si l’infection par le VIH est un facteur de risque de tuberculose (TBC), deux cohortes ont été suivies pendant 2 ans :
- Cohorte VIH+ : 215 sujets, 83 cas de TBC
- Cohorte VIH- : 298 sujets vivant dans les mêmes conditions, 10 cas de TBC
Calculs
| Exposition | Cohorte | Cas TBC | Incidence | RR | IC 95% |
|---|---|---|---|---|---|
| VIH+ | 215 | 83 | 38,6% | 11 | 5,8-21,3 |
| VIH- | 298 | 10 | 3,4% | 1 | – |
Interprétation
L’incidence de la tuberculose est 11 fois plus élevée chez les personnes VIH+. L’intervalle de confiance [5,8 – 21,3] exclut la valeur 1, confirmant que l’association est statistiquement significative. Le VIH est donc un facteur de risque majeur de tuberculose.
Application en santé bucco-dentaire
De la même manière, les études épidémiologiques ont démontré que :
- Le tabagisme multiplie par 2,5 à 6 le risque de parodontite
- Le diabète non contrôlé multiplie par 3 le risque de parodontite sévère
- La consommation quotidienne de boissons sucrées multiplie par 2,5 le risque de caries multiples chez l’enfant
Ces données chiffrées permettent au praticien d’identifier les patients à risque et d’adapter ses recommandations préventives.
Applications pratiques pour l’étudiant en odontologie
Dans la pratique clinique quotidienne
Évaluation du risque carieux individuel
En utilisant les connaissances épidémiologiques, le futur praticien peut identifier les patients à haut risque :
- Consommation fréquente de sucre (> 4 prises/jour)
- Hygiène insuffisante (< 2 brossages/jour)
- Antécédents de caries multiples
- Xérostomie (médicamenteuse ou pathologique)
- Faible exposition au fluor
Évaluation du risque parodontal
Facteurs de risque cumulatifs :
- Tabagisme actif
- Diabète
- Stress chronique
- Antécédents familiaux
- Absence de soins réguliers
Personnalisation de la prévention
Les connaissances épidémiologiques permettent d’adapter les recommandations :
- Fréquence des rappels (3, 6 ou 12 mois selon le risque)
- Applications topiques de fluor pour patients à haut risque carieux
- Prescription de bains de bouche antiseptiques pour patients à risque parodontal
- Éducation renforcée à l’hygiène pour populations vulnérables
Dans la santé publique et la prévention collective
Programmes de dépistage
L’épidémiologie guide l’organisation des dépistages :
- Ciblage des populations à risque (zones défavorisées, écoles primaires)
- Choix du moment optimal (avant l’éruption des premières molaires permanentes)
- Évaluation de l’efficacité des programmes
Campagnes de prévention
Les données épidémiologiques permettent de :
- Identifier les comportements à modifier en priorité
- Mesurer l’impact des campagnes de sensibilisation
- Ajuster les messages préventifs selon les publics cibles
Politique de santé
- Justification de la fluoration de l’eau ou du sel
- Réglementation sur la publicité des produits sucrés
- Financement de programmes de prévention ciblés
Pour la formation continue et la recherche
Lecture critique d’articles scientifiques
Comprendre l’épidémiologie permet de :
- Évaluer la qualité méthodologique des études
- Interpréter correctement les résultats
- Identifier les biais potentiels
- Appliquer les résultats à sa pratique (Evidence-Based Dentistry)
Participation à la recherche clinique
Les futurs praticiens peuvent contribuer à :
- La collecte de données épidémiologiques
- L’évaluation de nouvelles techniques de prévention
- L’amélioration des connaissances sur les pathologies bucco-dentaires
Ressources pour approfondir vos connaissances
Pour les étudiants en odontologie souhaitant approfondir leurs connaissances en épidémiologie et biostatistiques, plusieurs ouvrages de référence sont recommandés. Par exemple, le Guide clinique d’odontologie offre une excellente synthèse des connaissances actuelles incluant les aspects épidémiologiques de nombreuses pathologies bucco-dentaires.
Pour ceux qui préparent l’internat, les Annales corrigées de l’internat en odontologie 2022-2024 constituent une ressource précieuse avec de nombreux QCM portant sur l’épidémiologie et la santé publique dentaire.
Conclusion : l’épidémiologie, un outil indispensable pour le chirurgien-dentiste moderne
L’épidémiologie ne se limite pas à des calculs statistiques abstraits. C’est un outil puissant qui permet au praticien de comprendre la distribution des maladies, d’identifier les facteurs de risque, d’évaluer ses pratiques et d’optimiser la prévention.
En maîtrisant ces concepts, l’étudiant en odontologie développe une approche scientifique de la santé bucco-dentaire, fondée sur les preuves plutôt que sur l’intuition. Il devient capable de :
- Identifier les patients à haut risque nécessitant un suivi rapproché
- Personnaliser les stratégies de prévention selon les profils individuels
- Évaluer l’efficacité de ses interventions par des indicateurs objectifs
- Participer à des actions de santé publique ciblées
- Contribuer à l’amélioration continue des connaissances par la recherche clinique
Dans un contexte où la dentisterie évolue vers une approche de plus en plus préventive et personnalisée, l’épidémiologie constitue un pilier essentiel de la formation du chirurgien-dentiste. Elle permet de passer d’une pratique réactive (traiter les pathologies) à une pratique proactive (prévenir leur apparition).
Points clés à retenir
- L’épidémiologie étudie la distribution et les déterminants des maladies dans les populations
- Les indicateurs de morbidité (prévalence et incidence) mesurent la fréquence des maladies
- Les facteurs de risque peuvent être identifiés et quantifiés par le risque relatif
- La standardisation permet de comparer équitablement des populations différentes
- Les données épidémiologiques guident les décisions cliniques et de santé publique
- La prévention ciblée basée sur l’épidémiologie est plus efficace que l’approche universelle
Passez à l’action
Pour approfondir ces notions essentielles :
- Consultez régulièrement les enquêtes nationales de santé bucco-dentaire
- Analysez la structure démographique de votre zone d’exercice future
- Identifiez les facteurs de risque prévalents dans votre région
- Participez aux programmes de dépistage pendant votre formation
- Lisez les publications épidémiologiques dans les revues scientifiques
- Appliquez ces connaissances dans votre pratique clinique quotidienne
L’épidémiologie est bien plus qu’une matière académique : c’est un état d’esprit scientifique qui enrichira toute votre carrière professionnelle.
Références bibliographiques
- Bezzaoucha A. Épidémiologie et biostatistique à l’usage des étudiants en sciences médicales. OPU, 1996.
- Ancelle T. Statistique épidémiologie. Collection sciences fondamentales, Maloine, 2e édition, 2008.
- Bourgeois D, Roland E, Desfontaine J. Épidémiologie des maladies bucco-dentaires. Éditions CdP, 2015.
- Organisation Mondiale de la Santé. Méthodes d’enquête de base sur la santé bucco-dentaire. 5e édition, 2013.
- Union Française pour la Santé Bucco-Dentaire (UFSBD). Enquêtes nationales de santé bucco-dentaire.
- Haute Autorité de Santé (HAS). Stratégies de prévention de la carie dentaire. Recommandations en santé publique, 2010.
Ressources externes complémentaires
ResiDentaire™ – Plateforme QCM Médecine Dentaire : https://residentaire.com/
Cette plateforme propose des milliers de QCM pour s’entraîner sur tous les aspects de l’odontologie, y compris l’épidémiologie et la santé publique dentaire.
Note de transparence : Cette page contient des liens d’affiliation. En cliquant dessus, vous n’êtes pas tenu de vous procurer les produits suggérés, mais si vous le faites, cela ne vous coûte rien de plus, et cela m’aide à financer ce site et à continuer à produire du contenu éducatif de qualité pour les étudiants en odontologie.


[…] : Le renforcement induit par l’effet de microrétention augmente la résistance du complexe […]