Propriétés thermique des matériaux à usage dentaire (Biomatériaux Dentaire)
Propriétés thermique des matériaux à usage dentaire (Biomatériaux Dentaire)
Introduction
Dans les tissus dentaires, les liaisons atomiques sont de type primaire avec peu ou pas d’électrons libres, entraînant une faible conductivité thermique. Cela permet d’éviter de ressentir les chocs thermiques ainsi que la douleur qu’ils pourraient provoquer. Une grande sensibilité au chaud ou au froid peut indiquer un état normal ou pathologique. La présence de reconstitutions coronaires, souvent métalliques (comme l’amalgame), introduit des électrons libres, favorisant la conductivité thermique, ce qui peut entraîner des douleurs et parfois des atteintes pulpaires.
Caractéristiques essentielles
Conductibilité thermique
Définition
La conductibilité thermique est la propriété des corps à transporter l’énergie calorifique. Ce transport peut s’effectuer dans les solides selon trois mécanismes :
- Par les électrons (cas des métaux).
- Par les molécules (cas des solides organiques).
- Par vibration (cas des solides ioniques).
Exemples de conductibilité thermique (à titre comparatif)
- Cuivre : 326 W/m·K
- Amalgame : 23 W/m·K
- Dentine : 0,62 W/m·K
- Résine : 0,2 W/m·K
- Hydroxyde de calcium : 0,75 W/m·K
- Eugénate : 0,5 W/m·K
- Phosphate de zinc : 1,3 W/m·K
Dilatation thermique
Lorsqu’un solide est chauffé à une température inférieure à celle nécessaire pour un changement d’état, il augmente de volume. Au niveau atomique, sous l’influence de la chaleur, l’atome se déplace de sa position d’équilibre vers des positions asymétriques. Cette dilatation dépend de la force des liaisons :
- Elle est faible dans les solides ioniques, comme le plâtre et les ciments aux oxyphosphates.
- Elle est plus importante dans les solides métalliques, comme les amalgames.
- Elle est très importante dans les solides moléculaires, comme les résines et les élastomères.
Exemples de dilatation thermique
- Couronnes dentaires : 11,4 × 10⁻⁶/°C
- Amalgame : 25 × 10⁻⁶/°C
- Résines : 81 × 10⁻⁶/°C
Ces deux propriétés, conductibilité et dilatation thermique, sont des paramètres essentiels pour évaluer la tolérance et le comportement des biomatériaux.
Corrosion électrochimique
Les restaurations et prothèses métalliques dans la cavité buccale sont confrontées à un environnement corrosif. Le principal électrolyte est la salive, présente en grande quantité, suivie des fluides extracellulaires au niveau des sillons gingivo-dentaires et du sang dans les zones tissulaires enflammées ou traumatisées, qui constituent également des électrolytes agressifs.
Définition
La corrosion est une réaction chimique ou électrochimique entre un matériau, généralement un métal, et son environnement, entraînant une dégradation du matériau et de ses propriétés. Il existe trois types de corrosion :
- Corrosion chimique
- Corrosion électrochimique
- Corrosion bactérienne
Corrosion électrochimique (corrosion humide)
C’est le type de corrosion le plus courant en biomédical. Elle se produit en cas d’hétérogénéité dans le métal, l’alliage ou le milieu, formant une pile électrochimique avec une anode et une cathode :
- Anode : Électrode où se produit l’oxydation (dissolution du métal), avec passage du courant du métal vers la solution.
- Cathode : Électrode où se produit la réduction, avec passage du courant de la solution vers le métal.
Les réactions électrochimiques sont des réactions d’oxydoréduction avec transfert d’électrons. Toute réaction d’oxydoréduction comprend :
- Une réaction d’oxydation (anodique, pôle négatif) avec perte d’électrons.
- Une réaction de réduction (cathodique, pôle positif) avec gain d’électrons.
Ces deux réactions se produisent simultanément, générant un courant appelé courant de corrosion.
Principales formes de corrosion
Corrosion généralisée ou uniforme
Elle se manifeste sur toute la surface du métal à la même vitesse, entraînant une diminution régulière de l’épaisseur ou un changement de coloration (ternissement).
Corrosion localisée
- Corrosion par piqures : Piqures localisées à certains points de la surface, se développant de manière insidieuse et s’auto-propagant.
- Corrosion par crevasse : Due à une différence d’accessibilité à l’oxygène entre deux zones d’une structure métallique.
- Corrosion galvanique : Attaque de la phase la moins noble d’un alliage ou corrosion entre deux matériaux métalliques dans le même environnement.
Corrosion et dissolution sélective
Oxydation d’un composant de l’alliage, conduisant à une structure métallique poreuse.
Corrosion par frottement
Détérioration à l’interface entre des surfaces de contact.
Corrosion sous contrainte et fatigue-corrosion
Fissuration du métal résultant de l’action combinée d’une contrainte mécanique (force de traction) et d’une réaction électrochimique.
État vitreux des matériaux
Les polymères sont omniprésents en odontologie conservatrice (matériaux de reconstitution) et en prothèse (matériaux d’infrastructure cosmétiques ou à empreinte). Au contact des tissus bucco-dentaires, ces polymères doivent répondre durablement à des conditions cliniques variées.

Définitions
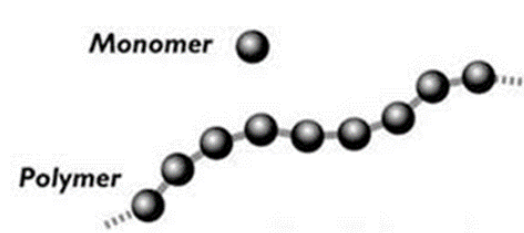
Monomère
Composé constitué de molécules simples pouvant réagir avec d’autres monomères pour former un polymère.
Polymère
Grande molécule constituée d’unités fondamentales appelées monomères, reliées par des liaisons covalentes (partage d’une paire d’électrons entre deux atomes).
Macromolécule
Synonyme de polymère.
Homopolymère
Macromolécule comportant des motifs monomères tous identiques.
Copolymère
Macromolécule comportant des motifs monomères de deux ou trois sortes différentes.
Types de polymères
- Naturels : Caoutchoucs, glycogène, ADN, protéines (d’origine animale ou végétale).
- Synthétiques : Polyéthylène, polypropylène, PVC, polyesters, polycarbonates, etc.
Polymères linéaires
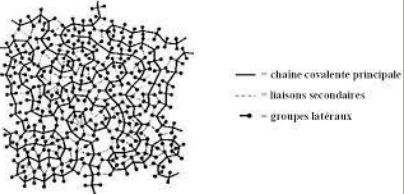
Ils sont constitués de grandes chaînes de monomères reliées par des liaisons covalentes. Ces macromolécules sont liées entre elles par des liaisons secondaires (liaisons de Van der Waals), qui assurent la stabilité du polymère. Lorsque ces liaisons sont présentes, le matériau devient rigide et présente un comportement solide : c’est l’état vitreux.
Si la température augmente, l’agitation moléculaire rompt progressivement ces liaisons secondaires. Le matériau se ramollit et s’écroule sous son propre poids, adoptant le comportement d’un liquide visqueux. La température à laquelle cette transition se produit est appelée température de transition vitreuse.
Structure des polymères
- Chaîne covalente principale
- Liaisons secondaires
- Groupes latéraux
Conclusion
La compréhension des mécanismes de prise et de la chimie des matériaux polymères permet aux praticiens de choisir le matériau le mieux adapté à chaque cas, en connaissant leurs limites et les précautions nécessaires pour obtenir les meilleurs résultats.
Propriétés thermique des matériaux à usage dentaire (Biomatériaux Dentaire)
Voici une sélection de livres:
- “Orthodontie de l’enfant et de l’adulte” par Marie-José Boileau
- Orthodontie interceptive Broché – Grand livre, 24 novembre 2023
- ORTHOPEDIE DENTO FACIALE ODONTOLOGIE PEDIATRIQUE
- Orthopédie dento-faciale en dentures temporaire et mixte: Interception précoce des malocclusions Broché – Illustré, 25 mars 2021
- Nouvelles conceptions de l’ancrage en orthodontie
- Guide d’odontologie pédiatrique: La clinique par la preuve
- Orthodontie linguale (Techniques dentaires)
- Biomécanique orthodontique
- Syndrome posturo-ventilatoire et dysmorphies de classe II, Bases fondamentales: ORTHOPÉDIE ET ORTHODONTIE À L’USAGE DU CHIRURGIEN-DENTISTE



[…] vest un substitut dentinaire inorganique définitif, bioactif, composé par […]