Physiopathologie de la douleur
Physiopathologie de la douleur
Introduction
La douleur est considérée comme un phénomène multidimensionnel, plurifactoriel et non comme une réaction simple, univoque à une stimulation périphérique. Il s’agit d’une manifestation totalement subjective et comportementale en réponse à un stimulus nociceptif physique ou psychologique. L’expérience douloureuse dépend aussi de facteurs socio-culturels, religieux et ethniques.
1. Rappel Anatomique
Le système nerveux est un système biologique responsable de la coordination des actions avec l’environnement extérieur et de la communication rapide entre les différentes parties du corps. Il est composé de deux parties :
1.1. Système Nerveux Central (SNC)
Comprend l’encéphale et la moelle épinière :
- L’encéphale : contrôle la plupart des fonctions du corps, dont la perception, les mouvements, les sensations, les pensées, la parole et la mémoire. Il regroupe le cerveau, le tronc cérébral et le cervelet.
- La moelle épinière : se rattache à l’encéphale au niveau du tronc cérébral.
- Le tronc cérébral : à la jonction entre le cerveau, le cervelet et la moelle épinière, constitué de haut en bas du mésencéphale, du pont de Varole (protubérance) et du bulbe rachidien (moelle allongée).
1.2. Système Nerveux Périphérique (SNP)
Formé de nerfs et de ganglions qui envoient des signaux au SNC et qui reçoivent des signaux du SNC.
2. Définitions
2.1. Définition de la Douleur
La douleur est « une expérience sensorielle et émotionnelle désagréable, associée à une lésion tissulaire réelle ou potentielle, ou décrite dans des termes évoquant une telle lésion ».
Cette définition rappelle le caractère multidimensionnel de cette perception complexe :
- L’atteinte lésionnelle réelle : mise en jeu de récepteurs périphériques spécifiques, par exemple une lésion directe comme se couper le doigt avec un couteau.
- L’atteinte potentielle : absence de lésion périphérique mais présence de lésions centrales, par exemple une brûlure dont la douleur persiste malgré l’absence de la source de chaleur.
- La description par le sujet “en termes d’une telle lésion” : reflet du versant psychogène de la douleur.
La douleur est donc une expérience subjective et comportementale en réponse à un stimulus nociceptif physique ou psychologique.
2.2. Quelques Définitions Sémiologiques
a) Douleur référée ou projetée : douleur perçue à distance du siège de la lésion responsable.
b) Allodynie : douleur en réponse à des stimuli « non douloureux » mécaniques ou thermiques (ex. : effleurement de la peau) due à une diminution du seuil d’activation des nocicepteurs. Un stimulus habituellement non douloureux provoque des sensations douloureuses.
c) Hyperalgésie / Hyperalgie : réponse exagérée à une stimulation nociceptive.
d) Nociception : processus sensoriel qui permet de détecter, percevoir et réagir à des stimulations internes et externes potentiellement nocives pour l’organisme. C’est le processus sensoriel à l’origine du message nerveux qui provoque la douleur.
3. Composantes de la Douleur
De par les paramètres multidimensionnels de l’expression de la douleur, on peut décrire trois principales composantes :
- Sensori-discriminative : liée à la capacité d’analyser la nature, la localisation, la durée et l’intensité de la stimulation douloureuse.
- Affectivo-émotionnelle : toute douleur s’accompagne d’un retentissement sur l’affectivité et l’émotion (angoisse, dépression, peur, anxiété).
- Cognitivo-comportementale : modification du comportement (fuite, etc.), influences culturelles et sociologiques du patient.
4. Types de Douleurs
4.1. Douleur Aiguë
La douleur aiguë survient brusquement, par exemple à la suite d’une blessure ou d’une opération :
- Se traite efficacement par des moyens pharmacologiques (médicaments antidouleur, anesthésie).
- Disparaît généralement une fois la blessure guérie ou l’inflammation résorbée.
De règle : la douleur aiguë est un symptôme qui décroît lorsqu’un traitement de sa cause est institué.
4.2. Douleur Chronique
Persiste sur une période prolongée (> 3 mois) :
- Peut soit se maintenir de façon relativement constante (ex. : douleurs cancéreuses), soit varier d’intensité en fonction des périodes.
- De causes organiques et/ou psychiques.
Fait important à retenir : insuffisamment traités, les états douloureux aigus peuvent dégénérer en douleurs chroniques.
5. Mécanismes Physiopathologiques et Transmission de la Douleur
La transmission douloureuse est un phénomène complexe impliquant des mécanismes électro-physiologiques et neurochimiques, où 3 étapes se succèdent :
- La nociception : élaboration de l’influx nerveux au niveau du nocicecepteur et sa transmission dans la fibre nerveuse périphérique.
- Le relais au niveau de la corne dorsale : relais et modulation au niveau de la corne dorsale de la moelle épinière (transmission, blocage ou amplification, convergence des influx).
- L’intégration au niveau du cerveau : transforme l’influx en message conscient (sensation douloureuse) avec une composante sensori-discriminative (intensité,he localisation, durée) et une composante émotionnelle et affective désagréable.
5.1. Voies de Transmission et de Perception de la Douleur
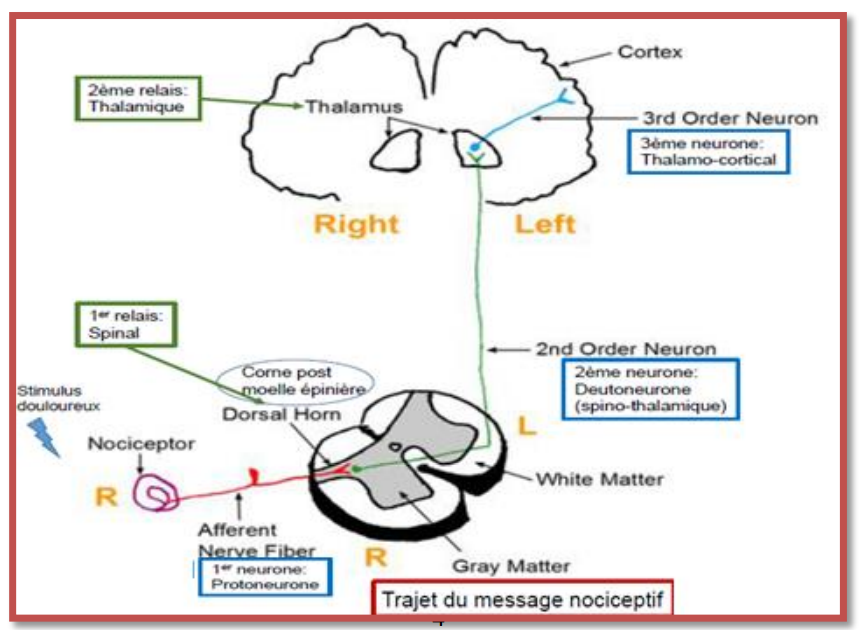
Les voies de transmission de la douleur, de l’agression à l’intégration cérébrale, sont :
- 1er neurone (Proto-neurone) : neurone de premier ordre, de la fibre périphérique à la corne dorsale de la moelle épinière.
- 2ème neurone (Deuto-neurone, Spinothalamique) : neurone de second ordre, de la moelle épinière jusqu’au thalamus.
- 3ème neurone (Thalamo-cortical) : neurone de troisième ordre, du thalamus vers le cortex cérébral.
Relais entre les neurones :
- 1er relais (spinal) : corne postérieure de la moelle épinière.
- 2ème relais (thalamique) : thalamus.
5.2. Mécanismes Physiopathologiques de la Douleur
5.2.1. De la Périphérie à la Moelle Épinière
a) Les nocicepteurs : récepteurs périphériques de la douleur présents dans la peau, les viscères, les muscles, les articulations et les tendons. Tous les organes en sont équipés, sauf le cerveau (seules les méninges en possèdent). Ce sont des terminaisons nerveuses libres capables d’identifier une stimulation nociceptive et de coder son intensité. Reliés à des fibres nerveuses appelées « afférences primaires », leur corps cellulaire se trouve au niveau des ganglions rachidiens.
- Stimulation : activation par action directe (lésion tissulaire) ou indirecte (substances algogènes endogènes libérées par le tissu lésé). Ces médiateurs chimiques forment une « soupe inflammatoire ».
b) Substances algogènes (suite) : Les lésions tissulaires et l’inflammation engendrent la production de nombreux médiateurs qui, directement ou indirectement, contribuent à la sensibilisation des fibres afférentes périphériques. Ces neurotransmetteurs et neuromodulateurs périphériques forment ce qu’on appelle une « soupe inflammatoire ». Ils sont libérés par les tissus lésés, les cellules sanguines (plaquettes, polynucléaires, mastocytes), les macrophages, et les terminaisons des fibres afférentes (ex. : substance P).
Parmi ces substances, on distingue :
- Bradykinine : maillon chimique essentiel, augmente la perméabilité vascul!
aire et provoque une vasodilatation.
- Prostaglandines (PG) : non algogènes en elles-mêmes, mais sensibilisent les nocicepteurs à l’action d’autres substances en abaissant leur seuil d’activation.
- Histamine : prurigineuse puis douloureuse, issue de la dégranulation des mastocytes.
c) Voies afférentes périphériques : Transmission de la sensibilité de la périphérie vers la moelle épinière. Un nerf sensitif contient trois groupes de fibres nerveuses :
- Fibres Aβ : gros calibre, fortement myélinisées, véhiculent la sensibilité tactile et proprioceptive.
- Fibres Aδ : moyennement myélinisées, spécifiques de la douleur (douleur rapide, localisée, type piqûre).
- Fibres C : amyéliniques, spécifiques de la douleur (douleur diffuse, mal localisée, tardive, type brûlure).
Toutes ces fibres passent par le ganglion spinal sur la racine postérieure de la moelle épinière, puis rejoignent la corne dorsale spinale.
Les relais entre les différents neurones se fon
- Après activation des nocicepteurs, le message est véhiculé jusqu’à la corne postérieure par :
- Fibres Aδ : faiblement myélinisées, responsables de la douleur localisée et précise.
- Fibres C : non myélinisées, responsables de la douleur diffuse et tardive.
- Les fibres Aα et Aβ, fortement myélinisées, répondent aux stimulations mécaniques modérées (tact, toucher), mais pas aux stimulations nociceptives.
5.2.2. Au Niveau de la Moelle Épinière
a) La corne dorsale spinale : Après leur trajet dans les nerfs périphériques, les fibres afférentes rejoignent le système nerveux central au niveau de la corne postérieure de la moelle épinière.
- Principaux neuromédiateurs libérés par les fibres Aδ et C dans l’espace synaptique :
- Glutamate : excitateur puissant.
- Substance P : neurotransmetteur principal de la douleur.
b) Voies spinales ascendantes :
Les neurones nociceptifs de la corne dorsale spinale décussent (croisement en X) au niveau de la commissure grise ventrale et gagnent le cordon antérolatéral controlatéral de la moelle épinière pour constituer le faisceau spinothalamique (substance blanche).
- Le message nociceptif emprunte des voies ascendantes jusqu’au thalamus :
- Voie de la composante sensorielle discriminative : emplacement, intensité, nature de la douleur.
- Voie de la composante émotionnelle et affective : caractère désagréable, déclenche la fuite ou la défense.
5.2.3. Au Niveau du Cerveau
C’est au niveau du cortex cérébral que l’organisme prend conscience du caractère douloureux de l’information et devient capable de discerner la localisation de la douleur.
6. Mécanismes de Contrôle de la Douleur
Les voies nociceptives afférentes sont régulées en permanence par des systèmes, essentiellement inhibiteurs, au niveau de leurs divers relais centraux (spinaux et thalamiques) :
a) Au niveau spinal : Deux mécanismes de contrôle :
- Théorie du « Gate Control » (contrôle de la porte) :
- Les messages nociceptifs des fibres Aδ et C peuvent être bloqués à leur entrée dans la corne postérieure de la moelle épinière par une action inhibitrice des fibres de gros calibre Aα et Aβ, qui véhiculent des messages tactiles non nociceptifs.
- Système opioïde :
- Au niveau de la corne dorsale, des récepteurs aux endorphines (opiacés) dont l’activation entraîne une inhibition. Les endorphines sont des peptides endogènes qui miment l’action de la morphine et se fixent sur les récepteurs opiacés.
b) Au niveau supraspinal :
- Les voies descendantes modulent l’intensité de la douleur en diminuant l’activité des neurones nociceptifs de la moelle (contrôle inhibiteur descendant).
- Contrôle des centres supérieurs du SNC : modulent surtout l’aspect désagréable de la douleur via la gestion de la composante émotivo-affective.
- Principaux neurotransmetteurs : sérotonine et norépinéphrine, dont l’augmentation provoque la libération d’opioïdes endogènes par les interneurones inhibiteurs de la corne dorsale.
La douleur survient lorsqu’il y a un déséquilibre entre la transmission de la douleur et le système d’inhibition, soit par :
- Excès de nociception : douleurs nociceptives dues à une augmentation de la stimulation douloureuse (ex. : brûlure, plaie, migraine).
- Défaut d’inhibition : douleurs neuropathiques par lésion nerveuse périphérique ou centrale, caractérisées par :
- Douleurs à type de décharges électriques.
- Associées à des zones cutanées d’anesthésie ou d’allodynie.
- Psychogène : souffrance morale liée à une psychopathologie ou à la gravité de la maladie.
La transmission des messages nociceptifs est réglée par un effet de balance entre diverses influences.
7. Examen du Patient Douloureux et Évaluation de la Douleur
- L’examen du patient douloureux est essentiel pour préciser les caractéristiques sémiologiques de la douleur. L’évaluation constitue une part de cet examen.
- Quel que soit le site de la douleur, l’examen doit préciser au moins 7 items :
- Profil évolutif : ancienneté (plus de 3 à 6 mois ?), mode de début (accident, effort, repas, etc.), horaire.
- Topographie : siège de la douleur, irradiations.
- Type de douleur : décharges électriques, brûlure, etc.
- Intensité.
- Facteurs d’aggravation.
- Manifestations associées.
- Impact sur la qualité de vie.
Conclusion
La transmission de la douleur passe par un parcours complexe impliquant plusieurs centres nerveux, avec des relais, des modulations, et la participation de multiples neurotransmetteurs et neuromodulateurs. Ce processus aboutit à un système d’inhibition qui atténue l’expression de la douleur, créant un équilibre naturel.
Physiopathologie de la douleur
Voici une sélection de livres:
Parodontologie Relié – 1 novembre 2005
Guide pratique de chirurgie parodontale Broché – 19 octobre 2011
Parodontologie Broché – 19 septembre 1996
MEDECINE ORALE ET CHIRURGIE ORALE PARODONTOLOGIE
Parodontologie: Le contrôle du facteur bactérien par le practicien et par le patient
Parodontologie clinique: Dentisterie implantaire, traitements et santé
Parodontologie & Dentisterie implantaire : Volume 1
Endodontie, prothese et parodontologie
La parodontologie tout simplement Broché – Grand livre, 1 juillet 2020

Leave a Reply