Patients irradiés de la région cervicofaciale
Patients irradiés de la région cervicofaciale
Introduction
Nous disposons, à l’heure actuelle, d’un arsenal thérapeutique relativement large et varié pour le traitement des cancers de la sphère cervico-faciale. La compréhension des principes de ces différents traitements est essentielle à tout praticien spécialiste en odontostomatologie pour assurer au patient une prise en charge bucco-dentaire optimale.
La radiothérapie cervico-faciale expose le patient à de multiples effets secondaires au niveau de la sphère oro-faciale. Ces séquelles peuvent par ailleurs être aggravées par l’existence de pathologies bucco-dentaires, ou encore par la réalisation d’extractions ou de traitements dentaires intempestifs.
La prise en charge odonto-stomatologique intervient donc à toutes les étapes de la radiothérapie :
- Avant le traitement : la mise en œuvre de la radiothérapie cervico-faciale est impérativement précédée par une mise en état bucco-dentaire ;
- Pendant le traitement : elle concerne la prise en charge des effets indésirables liés à la radiothérapie ;
- Après le traitement : la prise en charge intervient en assurant le suivi du patient, la prévention et le traitement de l’ostéoradionécrose.
L’Ostéoradionécrose (ORN) ou l’ostéite post-radique (OPR) est la complication la plus redoutable. Des précautions particulières doivent être prises par le médecin dentiste, quelle que soit l’ancienneté de la radiothérapie.
I. Généralités sur la radiothérapie
I.1. Définition
La radiothérapie est l’utilisation des radiations ionisantes à des fins thérapeutiques. Qu’elle soit exclusive ou associée à d’autres moyens (chirurgie/chimiothérapie), elle reste l’une des principales armes thérapeutiques des cancers.
Les objectifs sont :
- Curatifs : traiter la tumeur ou les résidus tumoraux post-chirurgicaux et/ou post-chimiothérapies ;
- Palliatifs : à visée antalgique, par exemple pour des métastases vertébrales.
I.2. Indications
La radiothérapie sera proposée en fonction :
- Du type de cancer ;
- De sa localisation ;
- De son stade d’évolution ;
- De l’état général du patient.
On parle de :
- Radiothérapie néo-adjuvante ou pré-opératoire : réalisée avant la chirurgie, elle a pour but de réduire la taille de la tumeur, faciliter l’intervention et/ou minimiser le risque de récidive locale du cancer ;
- Radiothérapie adjuvante ou post-opératoire : réalisée après la chirurgie, elle complète la chirurgie en détruisant les éventuelles cellules cancéreuses résiduelles dans le but de diminuer le risque de récidive locale ;
- Radiothérapie per-opératoire : réalisée au cours d’une intervention chirurgicale, elle expose directement la tumeur résiduelle ou la zone où se trouvait la tumeur à une dose unique élevée de rayons, réduisant l’irradiation des tissus sains ;
- Radio-chimiothérapie concomitante : association de radiothérapie et chimiothérapie, où certains médicaments de chimiothérapie (radio-sensibilisants) rendent les cellules cancéreuses plus sensibles aux rayons et augmentent leur efficacité.
I.3. Principe de la radiothérapie des VADS
Le principe de base consiste à altérer l’ADN cellulaire, provoquant des lésions cellulaires létales. Les cellules saines ont une capacité de régénération plus importante que les cellules tumorales.
Les doses de radiations sont mesurées en gray (Gy), unité internationale de dose absorbée (1 Gy = 1 joule/kg). Dans le cadre du traitement des tumeurs de la tête et du cou :
- La dose totale d’irradiation est comprise entre 60 et 70 Gy ;
- Les doses de radiothérapie complémentaire postopératoire varient de 45 à 55 Gy.
Le traitement est appliqué de manière itérative pour permettre la réplication des cellules saines et non des cellules tumorales :
- Fractionnement : répartition des doses ;
- Étalement : sur plusieurs semaines.
Ainsi, classiquement, pour un carcinome épidermoïde des VADS, le patient bénéficie de 5 séances hebdomadaires d’irradiation pendant 5 à 7 semaines, chaque séance délivrant environ 2 Gy.
I.4. Les modalités d’irradiation des cancers de la sphère Oro-Faciale
A. La radiothérapie externe (transcutanée)
Dans le cas de la radiothérapie externe, les rayons sont émis à partir d’une source externe à l’organisme. Elle consiste à irradier la tumeur à l’aide d’un ou de plusieurs faisceaux. Les appareils modernes utilisés sont les accélérateurs linéaires de particules. L’utilisation des appareils au cobalt-60 (« bombes au cobalt ») disparaît progressivement.
- Radiothérapie conformationnelle 3D : technique la plus employée actuellement, elle permet de faire correspondre le volume irradié au volume de la tumeur le plus précisément possible.
- Radiothérapie conformationnelle en modulation d’intensité (RCMI) : évolution de la radiothérapie conformationnelle 3D, elle constitue le standard actuel de la radiothérapie des cancers ORL. Elle délivre des doses optimales dans un volume cible tumoral tout en préservant les organes à risque (OAR : nerfs optiques, tronc cérébral, parotides). Le principal bénéfice clinique est la réduction du risque de séquelles tardives pour les glandes salivaires.
Cependant, cet objectif peut être impossible à atteindre dans les cas où le volume tumoral est important (T3/T4), une partie des OAR à proximité pouvant être incluse dans l’irradiation.
En Algérie, au service de radiothérapie CPMC d’Alger, la RCMI a été adoptée en 2017. Le déroulement du traitement passe par plusieurs étapes :
- Scanner dosimétrique : avec réalisation des systèmes de contention pour éviter que le positionnement du patient soit différent d’un jour à l’autre ;
- Calcul de la balistique : par le radiothérapeute et le radiophysicien (dose totale à délivrer, nombre de faisceaux d’irradiation, organes nobles « contournés » autant que possible épargnés) ;
- Séances d’irradiation.
B. Curiethérapie
La curiethérapie est une technique particulière de radiothérapie qui consiste à introduire la source d’irradiation directement au contact ou à l’intérieur de la tumeur. Il existe deux types :
- Curiethérapie interstitielle : introduction de fils radioactifs à l’intérieur de tissus ;
- Curiethérapie endocavitaire : introduction de la source radioactive dans les cavités naturelles de l’organisme touchées par le cancer (vagin, utérus, etc.).
La curiethérapie concerne les tumeurs de faible volume, sans envahissement osseux, parfaitement localisées et accessibles. Elle permet de délivrer une dose d’irradiation elevated dans un volume tissulaire limité, épargnant les tissus sains de voisinage grâce à la décroissance rapide de la dose à mesure que l’on s’éloigne de la source radioactive. Cela limite les effets secondaires et, dans certains cas, permet de conserver l’organe atteint.
Les éléments radioactifs les plus souvent utilisés sont :
- Iridium ;
- Césium ;
- Iode.
Ces sources peuvent se présenter sous forme de grains, de fils ou de micro-sources selon la nature du radio-élément. Les traitements sur 24 heures sont à privilégier, à raison d’une séance toutes les heures avec un débit idéal de 0,5 Gy/h (pouvant varier de 0,3 à 0,7 Gy/h). Pour la curiethérapie de haut débit de dose, il est préconisé deux séances par jour, espacées de plus de six heures, en dix séances.
II. Les effets secondaires de la radiothérapie
Toute radiothérapie est appliquée de manière à détruire au maximum les tissus néoplasiques sans dépasser la tolérance des tissus normaux. La véritable limite de l’efficacité de la radiothérapie à visée curative est sa toxicité pour les tissus sains.
Théoriquement, les effets de la radiothérapie se manifestent uniquement dans le volume irradié. Les tissus de la cavité buccale directement touchés par la radiothérapie de la tête et du cou sont :
- Les glandes salivaires ;
- La muqueuse ;
- Les dents ;
- Les muscles masticateurs ;
- Le tissu osseux.
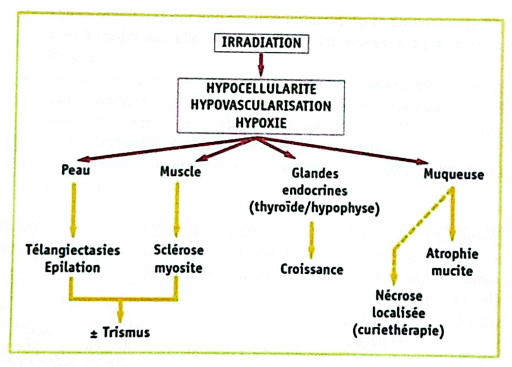
II.1. Facteurs influençant les effets des traitements
- La dose délivrée ;
- Le volume irradié et la localisation ;
- Le type de rayonnement ;
- La technique utilisée ;
- Les thérapeutiques associées.
II.2. Complications immédiates (ou précoces)
Deux formes très différentes d’effets secondaires existent, sans relation obligatoire entre elles :
- Effets précoces ou aigus : pendant et juste après la radiothérapie, obligatoires, transitoires, guérissant dans les semaines suivant le traitement, mais parfois potentiellement graves ;
- Effets tardifs.
II.2.1. La mucite
Elle s’installe rapidement et entraîne des difficultés alimentaires pour le patient. Ce sont des manifestations aiguës, douloureuses, transitoires, pouvant être très invalidantes, survenant pendant et juste après la radiothérapie. Elles s’expliquent par la diminution brutale du renouvellement cellulaire physiologique de la muqueuse, de la peau et des phanères. Pendant l’irradiation, on assiste à une mort cellulaire massive et à un trouble de la réparation de ces pertes, ce qui entraîne une fragilité considérable des tissus et une diminution de leur épaisseur.
Cliniquement :
- Elle se manifeste par une atteinte inflammatoire douloureuse de la muqueuse buccale non kératinisée, touchant surtout les lèvres, les joues et la face ventrale de la langue ;
- Outre une douleur intolérable rendant l’alimentation impossible, la radiomucite s’accompagne de dysphagie, dysgueusie et xérostomie ;
- Le degré de sévérité est directement corrélé à la dose délivrée, au type de fractionnement et à la surface des tissus irradiés.
Méthode d’évaluation (score de l’OMS) :
| Degré | Symptomatologie |
|---|---|
| Degré 0 | Aucune altération |
| Degré 1 | Dysesthésie, Érythème |
| Degré 2 | Érythème, Ulcération, Alimentation solide possible |
| Degré 3 | Érythème, Alimentation liquide seulement |
| Degré 4 | Aucune prise d’aliments per os n’est possible |
II.2.2. La radiodermite
C’est une affection devenue plus rare depuis l’avènement, à partir des années 1970, des accélérateurs de haute et moyenne énergies. Elle survient vers la 3ème semaine du traitement, à partir d’une dose de 20 Gy (selon un fractionnement conventionnel de 2 Gy sur 5 séances). Elle prédomine au niveau des plis et des zones fragiles de la peau, favorisant la macération, et peut être associée à un œdème cutané.
Degrés de sévérité :
- Érythème simple (grade I) ;
- Dermite sèche prurigineuse (grade II) ;
- Dermite exsudative (grade III) ;
- Nécrose cutanée (grade IV) – entité rare.
II.2.3. La xérostomie post-radique
L’hyposialie se manifeste dès que la dose d’irradiation dépasse 15 Gy. Elle survient vers la 2ème à 3ème semaine du traitement et devient définitive et irréversible au-delà de 60 Gy. L’hyposialie est due à la destruction des acini glandulaires par la radiothérapie. La possibilité de récupération dépend du pourcentage de glandes salivaires atteintes et de la dose reçue. Une amélioration clinique peut être observée après de nombreux mois lorsque les glandes salivaires accessoires épargnées (ex. : glandes palatines) prennent partiellement le relais. Lorsque les glandes principales sont détruites, l’amélioration reste très mineure.
Sur le plan clinique :
- La muqueuse buccale prend une teinte rouge, un aspect lisse et vernissé, parfois recouverte d’un enduit mucoïde blanchâtre ;
- La langue est fissurée, voire dépapillée ;
- Contraintes liées à la sécheresse buccale : inconfort, halitose, sensation de cuisson, intolérance au port de prothèses amovibles, troubles de l’élocution ;
- Conséquences : infections fongiques, dysphagies, caries dentaires multiples dues à l’altération de la fonction salivaire (nettoyage, régulation de l’acidité, neutralisation des toxines bactériennes et enzymes, lubrification, protection des muqueuses, reminéralisation de l’émail, maintien de l’intégrité des dents et tissus environnants) ;
- Impact significatif sur l’état physique et psychique des patients et leur qualité de vie.
II.2.4. Les infections buccales
En raison des lésions actiniques du parenchyme des glandes salivaires et de la xérostomie qui en résulte, toute radiothérapie de la sphère cervico-faciale est susceptible d’entraîner une prolifération des bactéries cariogènes, notamment Streptococcus mutans et lactobacilles. Cependant, parmi ces effets secondaires délétères, l’infection par Candida albicans représente la complication la plus sévère.
Les candidoses consécutives à l’irradiation peuvent se présenter sous diverses formes :
- Forme pseudo-membraneuse ;
- Forme chronique hyperplasique ;
- Forme érythémateuse ;
- Chéilite angulaire (dans certains cas).
II.2.5. Les troubles du goût
Trois formes peuvent être décrites :
- Agueusies : perte totale du goût ;
- Hypogueusies : perte de reconnaissance et difficultés à mesurer le goût avec préservation de la détection ;
- Dysgueusies : distorsion de la fonction gustative avec aversions alimentaires et perception de saveurs fantômes.
Habituellement temporaires, ils commencent à se faire ressentir vers la 2ème semaine de la radiothérapie et progressent jusqu’à la fin du traitement. Le retour à la normale survient après 4 mois, mais ils peuvent demeurer permanents dans certains cas. Ils sont influencés par la dose d’irradiation :
- Apparaissent entre 20-40 Gy ;
- Dysgueusie atteint 90 % de pertes relatives du goût au-delà de 60 Gy.
II.3. Complications tardives
II.3.1. Le trismus post-radique
La limitation d’ouverture buccale s’installe 3 à 6 mois après la radiothérapie, au-delà d’un seuil supérieur à 60 Gy.
- Très précoce, il peut traduire une gêne consécutive à la radiothérapie (ex. : attitude antalgique due à une mucite réactionnelle) ;
- Tardive, son apparition ne doit pas exclure une récidive tumorale ou une ostéonécrose dans le diagnostic différentiel.
Conséquences cliniques :
- Dénutrition importante avec perte pondérale et carences multiples ;
- Restrictions de la vie quotidienne : troubles de l’alimentation, difficultés à maintenir une hygiène buccale correcte, dégradation de l’état bucco-dentaire, soins dentaires difficiles.
II.3.2. Odontoradionécrose
Les caries subséquentes à la radiothérapie prennent des allures caractéristiques extrêmement sévères et se distinguent des caries banales par :
- Leur plus grande agressivité ;
- La rareté de l’hyperesthésie dentinaire ;
- Leur rapidité d’évolution.
Elles s’installent après 3 à 6 mois du traitement sur des dents auparavant intactes. Leur évolution peut être fulgurante en l’absence de prise en charge, entraînant des fractures coronaires multiples. La région cervicale est atteinte de façon préférentielle.
- Facteur principal : la xérostomie, dont l’effet est plus significatif que le rayonnement lui-même ;
- Effets directs de l’irradiation : à la limite émail-dentine, oblitération des tubuli dentinaires due à la dégénérescence des prolongements des odontoblastes. L’émail devient moins résistant aux attaques acides, entraînant souvent la perte du recouvrement améliaire des structures sous-jacentes.
II.3.3. Troubles de la croissance et du développement
Chez les enfants subissant une radiothérapie pour des tumeurs malignes, les rayons ionisants entraînent des problèmes concernant le développement ultérieur des tissus durs et mous, en raison de leur croissance active. Chez l’enfant, toute irradiation d’une région en activité ostéogénique et odontogénique à un âge inférieur à 10 ans entraîne des troubles de croissance osseuse. Les radiations atteignent les centres de croissance, modifiant la croissance du complexe cranio-facial :
- 10 Gy : ralentit ou arrête temporairement la croissance ;
- 10-20 Gy : retard de croissance avec déficit final ;
- >20 Gy : risque d’arrêt définitif du cartilage de croissance (risque de 100 % si >30 Gy).
Troubles observés :
- Asymétries des structures oro-faciales ;
- Trismus ;
- Nombreuses anomalies dentaires.
II.3.4. Les anomalies dentaires
Elles apparaissent après une dose de 4 Gy et peuvent être sévères chez l’enfant à partir de 18-24 Gy. Elles concernent uniquement les dents situées dans le champ d’irradiation, avec une dose maximale en plein champ et décroissante de façon concentrique. Les anomalies sont plus sévères au centre qu’en périphérie. Elles dépendent du stade de développement dentaire au moment de l’irradiation (TBI) et de leur position dans le champ. Elles sont irréversibles et d’autant plus sévères que l’irradiation est précoce (âge < 5 ans).
- Nanisme corono-radiculaire : observé en territoire irradié ; en périphérie, troubles de l’édification radiculaire ;
- Anomalies de structure : perturbations du développement de l’émail selon l’histogénèse et la dose. Les dents sont plus sensibles avant leur histodifférenciation ;
- Anomalies du nombre : une irradiation à forte dose atteint le germe dentaire en formation, entraînant une dégradation du bourgeon et une agénésie de la dent définitive (germes les plus touchés : 2èmes prémolaires, maturation tardive) ;
- Effets sur la pulpe et le ligament : stimulation de la formation d’ostéodentine dans la papille dentaire, provoquant un rétrécissement canalaire. Les odontoblastes sont sévèrement touchés, avec diminution de leur activité sécrétoire (plus liée à un défaut de nutrition qu’à une atteinte directe). Élargissement du ligament alvéolo-dentaire.
II.3.5. L’Ostéoradionécrose (ORN)
L’ostéoradionécrose (ORN) est la complication tardive la plus grave et la plus redoutée de la radiothérapie. Elle se définit comme une nécrose osseuse secondaire aux radiations utilisées à des fins thérapeutiques, entraînant une altération des capacités de défense et de cicatrisation du tissu osseux mandibulaire ou maxillaire.
Expression Clinique
L’expression clinique varie selon les patients, mais inclut généralement :
- Douleur (présente dans la majorité des cas),
- Expositions osseuses,
- Fistules,
- Orostomes,
- Fractures pathologiques au cours de l’évolution.
Signes Radiologiques
Les signes radiologiques n’apparaissent pas immédiatement. Une déminéralisation significative (30 à 50 %) est nécessaire pour les observer.
Délai d’Apparition et Risque
- Le délai d’apparition varie de quelques mois à plusieurs années (jusqu’à 30 ans).
- Le risque ne diminue pas avec le temps, mais s’intensifie.
Facteurs de Risque
La survenue de l’ORN dépend de plusieurs facteurs :
- Dose d’irradiation : > 65 Gy augmente le risque.
- Complications buccodentaires ultérieures.
- Traitements chirurgicaux sur l’os irradié.
- Traumatismes.
- Seulement 35 % des ORN sont spontanées.
Localisation Préférentielle
L’ORN touche principalement :
- Mandibule :
- Branche horizontale (86 %),
- Angle (42 %),
- Symphyse (24 %).
- Maxillaire : rarement atteint, en raison des variations architecturales et vasculaires.
Facteurs Déclenchants
- Dose totale d’irradiation (> 65 Gy).
- Modalités de radiothérapie (RCMI, hypo- ou hyperfractionnement).
- Association de curiethérapie ou irradiation supplémentaire post-curage ganglionnaire.
- Site et stade tumoral (langue, plancher buccal, mur alvéolaire, amygdale, voile du palais, palais dur, larynx, lèvres, glandes salivaires).
- Non-respect du délai de 21 jours entre extractions dentaires et radiothérapie.
- Traumatismes mécaniques (gestes chirurgicaux, prothèses dentaires, brossage, alimentation).
- Soins ou avulsions dentaires sans précautions.
- Biopsies dans le cadre de la surveillance ou dépistage d’un second cancer.
- Mauvaise hygiène buccodentaire (caries multiples, parodontopathies).
- Absence ou non-respect de la fluoration dentaire.
- Persistance de l’intoxication tabagique.
Physiopathologie de l’Ostéoradionécrose
Deux théories principales expliquent la physiopathologie : les « 3 H » de Marx et les « 2 I » de Dambrain.
Théorie des « 2 I » de Dambrain
- Ischémie et Infection :
- L’infection est limitée à l’os exposé, absente dans les zones profondes non exposées.
- L’ischémie est indéniable mais n’explique pas tout.
Théorie des « 3 H » de Marx
- Hypocellularité, Hypoxémie, Hypovascularisation :
- Bases de la physiopathologie, fondées sur des séries cliniques et preuves histologiques.
- Réduction des capacités métaboliques, de cicatrisation et de réparation.
- Hypovascularisation démontrée par des mesures de teneur en oxygène (tissus irradiés vs sains).
- Fondement du traitement par oxygénothérapie hyperbare.
Processus Histologiques (Marx et Johnson, 1987)
- Hyperhémie,
- Inflammation (avec endartérite),
- Thrombose,
- Hypocellularité,
- Hypovascularisation,
- Fibrose.
Complémentarité des Théories
- Les deux théories sont partiellement complémentaires mais ne résolvent pas totalement la physiopathologie.
- Point commun : l’ischémie/hypovascularisation, liée à une atteinte vasculaire.
Classifications de l’Ostéoradionécrose
Classification de Store (2000)
- Stade 0 : Ulcération muqueuse seule (stade « latent » évoluant vers une nécrose osseuse).
- Stade I : Lyse osseuse radiologique sans atteinte muqueuse.
- Stade II : Lyse osseuse radiologique + dénudation muqueuse buccale.
- Stade III : Exposition intrabuccale d’os nécrotique, lyse radiologique, fistule cutanée, infection.
- Définition : Signes radiologiques de nécrose osseuse dans un champ d’irradiation, récidive tumorale exclue.
Classification de He et al. (2015)
- B : Bone necrosis (nécrose osseuse).
- S : Soft tissue defect (défaut des tissus mous).
- Stade 0 :
- B0S0 : Aucun signe évident ou ostéolyse radiographique, avec symptômes (douleur, exposition osseuse).
- Stade I :
- B1S0 : Lésion < 2 cm, sans défaut muqueux/cutané.
- B1S1 : Lésion < 2 cm, avec effraction muqueuse ou fistule cutanée.
- B1S2 : Lésion < 2 cm, avec orostome.
- Stade II :
- B2S0 : Lésion > 2 cm, sans défaut muqueux/cutané.
- B2S1 : Lésion > 2 cm, avec effraction muqueuse ou fistule cutanée.
- B2S2 : Lésion > 2 cm, avec orostome.
- Stade III :
- B3S0 : Fracture pathologique, sans défaut muqueux/cutané.
- B3S1 : Fracture pathologique, avec effraction muqueuse ou fistule cutanée.
- B3S2 : Fracture pathologique, avec orostome.
III. Prise en Charge Stomatologique des Patients sous Radiothérapie Cervico-Faciale
III.1. Avant la Radiothérapie
Collaboration entre radiothérapeute et dentiste pour prévenir l’ORN via la mise en état de la cavité orale :
- Thérapeutique parodontale : Détartrage sus/sous-gingival, polissage.
- Traitement conservateur : Soins des caries débutantes.
- Traitement endodontique : Dents à pulpe mortifiée (minimum 1 semaine avant radiothérapie).
- Reprise de traitements endodontiques : Dents mal traitées sous bridges.
- Avulsions :
- Dents irrécupérables (délabrées, mobiles, atteintes de furcation, lésions apicales, poches > 6 mm).
- Molaires et dents de sagesse en linguo/vestibulo-version.
- Délais de cicatrisation :
- 15 jours après extractions simples.
- 4 à 6 semaines après extractions délabrantes.
- Actes non traumatiques : Sutures hermétiques.
- Dents incluses : Peuvent rester en place.
- Dents enclavées : Avulsion si infections récentes ou potentiel éruptif avec obstacle.
- Conservation : Dents utiles pour réhabilitation prothétique.
- Hygiène stricte : Sensibilisation du patient.
Prophylaxie Fluorée
- Fluor quotidien à vie : 5 minutes/jour via gouttières thermoformées (Fluocaril Bifluoré 2000, Fluodontyl 1350).
- Brossage fluoré : Réservé aux enfants, soins dentaires, patients nauséeux.
- Gouttières : Dépassent la gencive de 2-3 mm pour couvrir la zone cervicale.
Curiethérapie
- Gouttière plombée pour protéger les dents, portée durant l’irradiation.
- Pas de fluorothérapie (absence d’hyposialie).
III.2. Pendant la Radiothérapie
- Pas d’actes chirurgicaux sauf urgences (discussion avec oncologue, traitement conservateur, antibiothérapie).
III.2.1. Prise en Charge des Complications Immédiates
- Mucites :
- Bains de bouche :
- Alcalins (bicarbonate de sodium, 4-6 fois/jour).
- Antiseptiques sans alcool (chlorhexidine 0,12 %, 3 fois/jour).
- Hygiène : Brosse douce/chirurgicale.
- Antalgiques : Xylocaine visqueuse (3 fois/jour), Aspégic 1000 (3 fois/jour).
- Nutrition : Conseils diététiques, aliments liquides, sonde si nécessaire.
- Bains de bouche :
- Hyposialie :
- Substituts salivaires : Aequasyal, BioXtra, carboxyméthylcellulose.
- Sialogogues : Pilocarpine, Jaborandi (peu prescrits : mauvaise tolérance).
- Stimulation : Substances acides/amères, chewing-gums sans sucre.
- Infections Buccales :
- Candidose : Bains de bouche fongicides (Fungizone, chlorhexidine, bicarbonate).
- Infections graves : Fluconazole, amphotéricine B (précaution hépatotoxicité).
III.3. Après la Radiothérapie
III.3.1. Traitement du Trismus Post-Radique
- Préventif : Exercices d’ouverture/fermeture (20 fois, 3 fois/jour).
- Curatif : Kinésithérapie, aides prothétiques (Therabite, abaisse-langue, pince à linge).
III.3.2. Traitement de l’Odontoradionécrose
- Préventif : Hygiène biquotidienne, fluoration quotidienne.
- Curatif :
- Restaurations (composite, verre ionomère).
- Extractions sous antibiothérapie (non traumatiques, suture gingivale, suivi jusqu’à cicatrisation, > 6 mois post-irradiation).
III.3.3. Prise en Charge de l’Ostéonécrose
A. Traitement Médical
- Antibiothérapie : Réservée aux gestes chirurgicaux (faible diffusion dans tissus ischémiés).
- Anti-inflammatoires : Avec antibiothérapie lors des poussées (AINS ou stéroïdiens).
- Bains de bouche antiseptiques : En cas d’exposition osseuse.
- Antalgiques : Morphiniques possibles.
- Oxygénothérapie Hyperbare (OHB) :
- Augmentation de la pression d’oxygène (2-3 atm, 100 % O₂).
- Effets : bactéricide, angiogenèse, prolifération fibroblastique, synthèse de collagène.
- Efficacité controversée.
B. Traitements Chirurgicaux
- Conservateurs : Séquestrectomie, curetage (tissus nécrotiques retirés, fermeture sans tension).
- Radicaux : Résection interruptrice + reconstruction par lambeau libre ostéocutané (ex. fibula, 25 cm max).
- Indications : Échec médical, douleur ≥ 5 (EVA), fracture, fistule, trismus invalidant.
C. Indications Thérapeutiques par Stade
| Stade | B/S | Traitement |
|---|---|---|
| Stade 0 | B0S0 | Traitement conservateur |
| Stade I | B1S0, B1S1, B1S2 | Séquestrectomie |
| Stade II | B2S0, B2S1, B2S2 | Résection marginale ou segmentaire + lambeau ostéocutané (± tissus mous) |
| Stade III | B3S0, B3S1, B3S2 | Résection segmentaire + lambeau ostéocutané (± tissus mous pour orostome) |
III.3.4. Extractions Après Irradiation
- Évaluation :
- Localisation (mandibule > maxillaire).
- Technique d’irradiation (2D, 3D, RCMI).
- Dose reçue (< 40 Gy : 6 % risque ; 40-60 Gy : 14 % ; > 60 Gy : ≥ 20 %).
- Facteurs de risque (diabète, parodontopathie).
- OHB : Si risque élevé.
- Antibiothérapie : Jusqu’à cicatrisation.
- Vasoconstricteurs : Éviter sur os irradié > 40 Gy.
III.3.5. Réhabilitation Dentaire
- Options : Prothèses amovibles, bridges, implants.
- Implants :
- Dose reçue, délai post-irradiation, localisation.
- Mise en charge : 3-24 mois post-irradiation.
- OHB : Réduit le risque d’ORN (RR 0,15) pour doses > 45 Gy.
- Sites favorables : Symphyse mandibulaire, prémaxillaire.
Conclusion
L’irradiation cervico-faciale, essentielle pour les cancers des voies aérodigestives supérieures, entraîne des séquelles salivaires et osseuses impactant la qualité de vie. La prise en charge multidisciplinaire, incluant le dentiste, vise la prévention (mise en état buccal) et le traitement des complications pour améliorer le confort des patients.
Références Bibliographiques
- J. Thariat et al., Dent et irradiation : prévention et traitement des complications dentaires de la radiothérapie y compris l’ostéoradionécrose, Cancer/Radiothérapie 14 (2010) 137-144.
- G. Raoul et al., Ostéoradionécroses des maxillaires (maxillaire et mandibulaire), EMC stomatologie, 22-062-D-20, 2008.
- P. Piret, J.M. Deneufbourg, L’ostéoradionécrose Mandibulaire : Épée de Damoclès de la Radiothérapie Cervico-Faciale ?, Rev Med Liege 2002; 57:6:393-399.
- Y. He et al., Retrospective analysis of osteoradionecrosis of the mandible: proposing a novel clinical classification and staging system, Int. J. Oral Maxillofac. Surg. 2015; 44:1547-1557.
- S. Delanian, J.L. Lefaix, Radionécrose de l’os mature : connaissance physiopathologique récente motrice d’une thérapeutique médicale innovante, Cancer/Radiother 2002; 6:1-9.
- Michael B. Ornstein, Andreas Filippi, Daniel Buser, Radiothérapie de la région cervico-faciale : conséquences intra-orales précoces et tardives, Information dentaire n°34, 10 octobre 2001.
- Michael Bornstein et al., Concepts de prophylaxie et de traitement des effets secondaires de la radiothérapie de la région cervico-faciale, Rev Mens Suisse Odontostomatol, Vol 111:8/2001.
Patients irradiés de la région cervicofaciale
Voici une sélection de livres en français sur les prothèses dentaires:
Prothèse fixée, 2e Ed.: Approche clinique Relié – Illustré, 4 janvier 2024
Prothèse Amovible Partielle : Clinique et Laboratoire
Collège National des Enseignants en Prothèses Odontologiques (CNEPO), Michel Ruquet, Bruno Tavernier
Traitements Prothétiques et Implantaires de l’Édenté Total 2.0
Conception et Réalisation des Châssis en Prothèse Amovible Partielle
Prothèses supra-implantaires: Données et conceptions actuelles
Prothèse complète: Clinique et laboratoire Broché – Illustré, 12 octobre 2017



Leave a Reply