INFLUENCE DES MALADIES PARODONTALES SUR L’ÉTAT GÉNÉRAL
INFLUENCE DES MALADIES PARODONTALES SUR L’ÉTAT GÉNÉRAL
1. Les maladies parodontales pendant la grossesse et leurs conséquences sur l’organisme
On peut distinguer deux grandes catégories de maladies parodontales : la gingivite et la parodontite.
Gingivite
Des signes cliniques essentiels sont parfois très discrets :
- La rougeur plus ou moins vive de la gencive libre et son œdème localisé (fréquemment au niveau des papilles seulement),
- L’aspect lisse et distendu de la gencive attachée,
- Le saignement provoqué et/ou spontané,
- L’absence de migration de l’épithélium de jonction le long de la surface radiculaire et pas de perte osseuse.
Le saignement gingival sensibilise et alerte les patientes et reste un critère majeur de l’intensité de l’inflammation gingivale. Les modifications hormonales de la grossesse peuvent conduire à une nette augmentation de la réponse inflammatoire gingivale. La progestérone, notamment :
- Augmente l’exsudation plasmatique,
- Altère l’intégrité des cellules endothéliales des capillaires gingivaux,
- Interfère dans la synthèse des prostaglandines et dans le métabolisme du collagène.
Parodontite
Les parodontites sont des maladies immuno-inflammatoires plurifactorielles et infectieuses qui présentent une alternance de phases aiguës et chroniques et qui ont un impact sur le parodonte profond. La destruction de ces tissus de soutien des dents est irréversible et est influencée par l’hyper-réactivité immunitaire vis-à-vis de la flore parodontale pathogène.
Les bactéries du biofilm parodontal produisent des enzymes protéolytiques susceptibles d’endommager les tissus parodontaux. Leurs facteurs chimotactiques sont capables de recruter des polynucléaires du réseau circulatoire dans les tissus en activant la réponse immunitaire cellulaire ou humorale. Cette réponse est habituellement protectrice mais, du fait de la présence de divers facteurs de risque, peut devenir hyper-réactive avec une synthèse accrue de molécules pro-inflammatoires qui endommagent les tissus.
Histologie
- Le foyer inflammatoire non actif est préférentiellement composé de lymphocytes T et de macrophages, qui témoignent d’une réponse cellulaire capable de contrôler la pathologie.
- Les lésions destructrices présentent une augmentation du nombre de cellules plasmatiques et de lymphocytes B.
Impact systémique
Parfois, la réponse inflammatoire ne se limite pas aux tissus parodontaux. Il a été évoqué que les épisodes quotidiens de bactériémie ou la dissémination des endotoxines des bactéries parodontopathogènes peuvent induire l’activation systémique de la réponse inflammatoire. Les bactéries ou les endotoxines dans la circulation systémique peuvent entraîner la production de cytokines pro-inflammatoires. Ces cytokines maintiennent la réponse inflammatoire avec comme résultat une up-régulation chronique systémique de basse qualité impliquant :
- L’interleukine 6 (IL-6),
- La C-réactive protéine (CRP).
Cette up-régulation, comprenant également l’activation des cellules inflammatoires et endothéliales, conduit à la dysfonction endothéliale. De nombreuses études rapportent que la parodontite chronique peut être associée à des manifestations pathologiques à distance et/ou à une aggravation de pathologies systémiques, par l’augmentation dans la circulation sanguine de la C-réactive protéine (CRP) et d’autres biomarqueurs inflammatoires.
Étude de Tonetti et al.
Tonetti et al. ont mesuré la fonction endothéliale 6 mois après un traitement parodontal effectué chez des patients atteints de parodontite. Ils ont observé une augmentation significative de la dilatation liée au flux dans l’artère brachiale, c’est-à-dire une amélioration de la fonction vasculaire.
Conséquences cliniques
Les conséquences des parodontites sont à la fois :
- Fonctionnelles,
- Esthétiques,
- Sociales.
Interactions entre maladies parodontales et complications de la grossesse
Les interactions à distance entre les bactéries parodontopathogènes et les organes, notamment le placenta, peuvent se faire par deux voies :
- Directe : Par la bactériémie systémique suite à l’altération de la barrière tissulaire.
- Indirecte : Par le passage dans la circulation sanguine des toxines et produits bactériens, ce qui active la production par l’organisme maternel de cytokines pro-inflammatoires. Ces cytokines provoquent la dysfonction vasculaire et tissulaire, notamment dans le réseau fœto-placentaire (une des causes de la pré-éclampsie).
Études et méta-analyses
- Scannapieco et al. suggèrent une association positive entre les maladies parodontales (MP) au cours de la grossesse et la survenue de diverses complications de la grossesse.
- Vergnes et al. (2007) ont publié une méta-analyse observationnelle qui a montré une augmentation significative des accouchements prématurés et/ou des nouveau-nés de faible poids de naissance. Ils ont établi une relation entre la présence des maladies parodontales gravidiques et la survenue des naissances prématurées. Cependant, ils suggèrent que, même s’il existe un lien entre les maladies parodontales sévères et le risque accru de certaines complications de la grossesse, il n’est pas possible de conclure que le traitement des parodontites au cours de la grossesse diminue la fréquence des complications. En utilisant des critères de recherche qualitative, les mêmes auteurs démontrent que le traitement des maladies parodontales au deuxième trimestre de la grossesse améliore de façon significative l’état du parodonte et ne présente pas de risque pour la mère ni pour le fœtus.
- Étude de 2010 : Un groupe de chercheurs a publié un travail sur les liens entre les parodontites maternelles et l’expression du récepteur soluble de Tyrosine Kinase-1 (sFlt-1), dont le rôle est avéré dans la pathogénèse de la pré-éclampsie. L’effet positif du traitement parodontal sur la diminution de la quantité des facteurs systémiques de l’inflammation dans la circulation sanguine pourrait également influencer les niveaux des facteurs angiogéniques circulants dans le cas de la pré-éclampsie.
2. De la maladie parodontale au diabète
Ces dernières années, des études ont rapporté que la sévérité de la maladie parodontale influencerait un mauvais contrôle de la glycémie.
Mécanismes
Dans les parodontites chroniques, les cellules de la gencive au contact des lipopolysaccharides des bactéries à Gram négatif présentes dans le biofilm vont libérer de grandes quantités de cytokines pro-inflammatoires, notamment :
- TNF-α,
- IL-1β,
- IL-6,
- PGE2 (prostaglandines E2).
Ces cytokines, libérées dans le sang :
- Augmentent l’insulinorésistance et perturbent le contrôle de la glycémie en empêchant l’action de l’insuline sur la graisse et les cellules musculaires,
- Favorisent la dégranulation des polynucléaires, augmentant ainsi la synthèse de plaque dentaire,
- Activent les lymphocytes B et T, qui libèrent du TNF-α, lequel active les ostéoclastes et la métalloprotéinase, responsables de la destruction des tissus parodontaux.
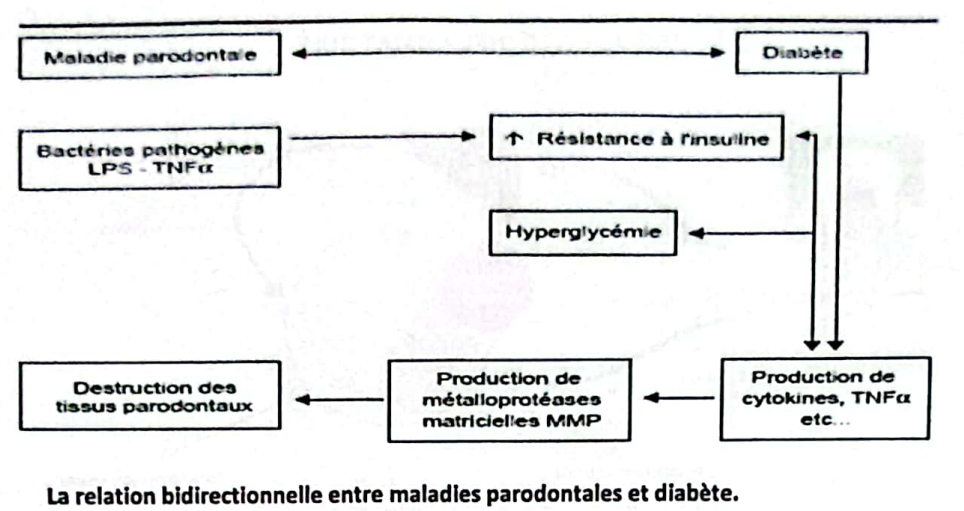
Relation bidirectionnelle entre maladies parodontales et diabète
On remarque que le taux de médiateurs pro-inflammatoires, comme la prostaglandine E2 (PGE2), augmente fortement quand le patient est atteint à la fois de diabète et de maladie parodontale. La production excessive de PGE2 altère à la fois l’équilibre du diabète et augmente la sévérité de la maladie parodontale. Les PGE2 sont révélatrices de la perte d’attache.
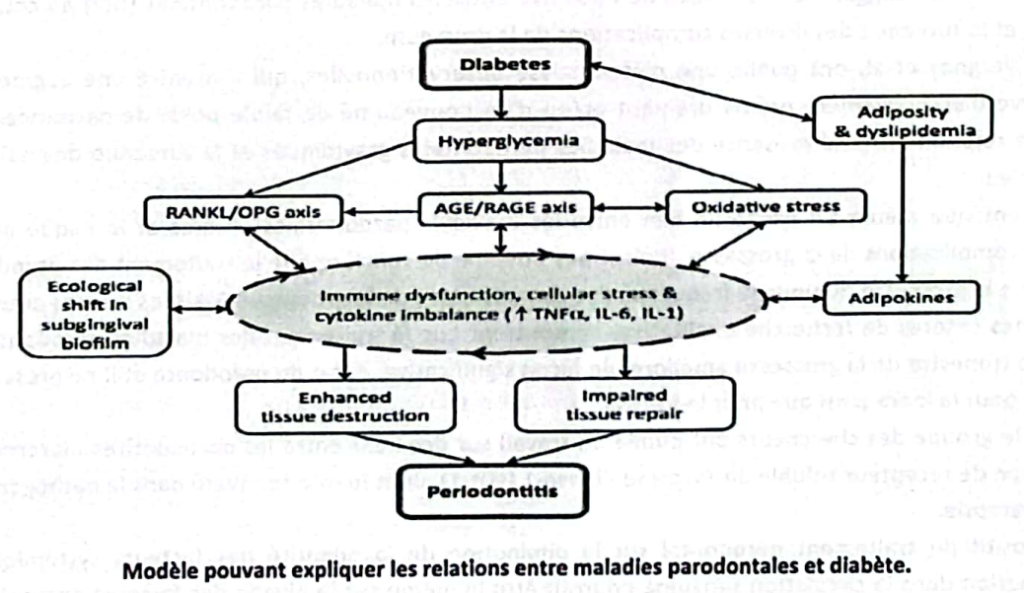
Modèle explicatif
Les preuves d’une association entre le diabète et la parodontite sont les suivantes :
- Plausibilité : Le diabète de type 2 est précédé d’une inflammation systémique entraînant une réduction de la fonction des cellules β pancréatiques, leur apoptose et une résistance à l’insuline. De plus en plus d’évidences montrent qu’une inflammation systémique élevée (phase aiguë et biomarqueurs de stress oxydatif) résulte de la pénétration des organismes parodontaux et de leurs facteurs de virulence dans la circulation, expliquant des mécanismes biologiquement plausibles des effets négatifs de la parodontite sur le diabète et ses complications.
- Données épidémiologiques : Des preuves fiables et concordantes démontrent qu’une parodontite grave affecte négativement le contrôle de la glycémie chez les patients diabétiques et non diabétiques. Chez les patients diabétiques, il existe une relation directe et dose-dépendante entre la gravité de la parodontite et les complications liées au diabète. Des données récentes indiquent que les patients souffrant d’une parodontite grave risquent de développer du diabète.
- Études interventionnelles : Des études cliniques ont montré qu’une thérapie parodontale mécanique est associée à une réduction significative de l’HbA1c après trois mois, ce qui représente un impact clinique équivalent à la prescription d’un second médicament destiné à traiter le diabète.
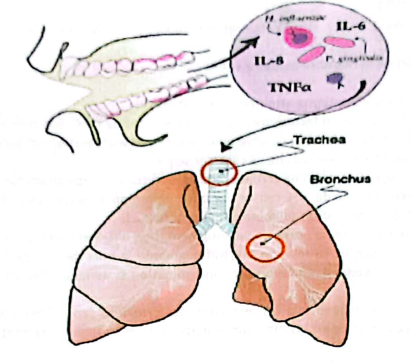
3. Maladies parodontales et maladies respiratoires
Les maladies respiratoires concernent les voies nasales, les bronches et les poumons. On distingue :
- Maladies aiguës : Pneumonies et bronchites,
- Maladies chroniques : Asthme et BPCO (Broncho-Pneumopathies Chroniques Obstructives).
Caractéristiques
- Les pneumonies peuvent être nosocomiales ou présentes chez des patients immunodéprimés et sont des infections du parenchyme pulmonaire.
- Un patient présentant de l’asthme peut être atteint de dyspnée sévère.
- Les BPCO se caractérisent par une obstruction respiratoire avec excès de sécrétion bronchique, entraînant une bronchite chronique et/ou un emphysème.
Traitements
Les traitements concernent surtout une amélioration de l’hygiène de vie.
Lien avec les maladies parodontales
Même si, à l’heure actuelle, le niveau de preuve reste insuffisant, les maladies parodontales seraient un facteur de risque indépendant pour les BPCO, et les microorganismes oraux et parodontaux seraient impliqués dans la pneumonie bactérienne.
Mécanismes proposés (Bansal et al., 2013)
Les bactéries orales pourraient participer à l’infection respiratoire de la région oropharyngée par plusieurs mécanismes :
- Réaction directe des pathogènes : Par inhalation ou aspiration des pathogènes oraux présents dans la plaque dentaire. La plaque dentaire est une source locale de Porphyromonas gingivalis (Pg) et Aggregatibacter actinomycetemcomitans (Aa), qui peuvent se détacher des sécrétions orales pour contaminer les bronches respiratoires.
- Réaction des enzymes associées aux parodontites : Présentes dans la salive, elles peuvent modifier les surfaces muqueuses pour favoriser l’adhésion et la colonisation des pathogènes respiratoires. Les mucines peuvent être altérées, ce qui réduit leur capacité à éliminer les pathogènes respiratoires.
- Rôle des cytokines : Les cytokines synthétisées et libérées à cause des bactéries parodontopathogènes peuvent altérer l’épithélium respiratoire pour recruter des neutrophiles sur les sites pulmonaires et promouvoir l’infection par des pathogènes respiratoires.
Observations
- Les patients atteints de BPCO sont plus à risque de développer des maladies parodontales que la population générale, et ce risque est proportionnel au contrôle de la BPCO.
- Les patients qui reçoivent un traitement aux corticostéroïdes seraient plus à risque de développer des maladies parodontales.
- L’inflammation systémique induite par les maladies parodontales aggrave les maladies respiratoires, et l’infection des parodontopathogènes favorise les pathogènes respiratoires.
Modèle à deux mécanismes
- Le rôle de l’infection des pathogènes,
- Le rôle de l’inflammation.
Cependant, ce modèle présente un niveau de preuve encore trop faible pour conclure à une relation bidirectionnelle entre les maladies respiratoires et les maladies parodontales.
4. Maladies Rénales
Les maladies parodontales (MP) et l’insuffisance rénale chronique (IRC) présentent une association significative et constante. Les effets de l’IRC sur les tissus oraux incluent :
- Xérostomie (sécheresse buccale),
- Calcification par oblitération de la chambre pulpaire et des canaux radiculaires,
- Modification du pH salivaire.
La prévalence des maladies parodontales chez les patients atteints d’IRC est élevée. De plus, la parodontite chronique est reconnue comme un facteur de risque indépendant de l’IRC, bien que son rôle exact soit difficile à définir en raison de facteurs confondants tels que le diabète ou le tabagisme. Leur relation est bidirectionnelle.
Physiopathologie de la réponse inflammatoire :
- Faible excrétion urinaire, taux élevés d’IL-6 et de cytokines pro-inflammatoires dans le sérum,
- Stress oxydatif et accumulation de produits avancés de glycation (AGE) due à une diminution de la clairance rénale,
- Présence de comorbidités comme le diabète ou l’athérosclérose.
Les maladies parodontales augmentent les niveaux d’IL-6 et de CRP (protéine C-réactive), entraînant une inflammation systémique. Cette relation entre MP et maladies rénales (MR) accroît le taux de CRP de manière synergique, favorisant un état inflammatoire généralisé. Ainsi, les MP peuvent aggraver les MR en exacerbant l’inflammation systémique.
Impact infectieux :
La réponse infectieuse des MR augmente la concentration de cytokines pro-inflammatoires et la charge bactérienne. Une hygiène orale insuffisante peut aggraver le développement des maladies parodontales.
Traitement :
Un traitement parodontal améliore le taux de filtration glomérulaire. Cependant, un suivi régulier est essentiel, car la charge bactérienne peut réapparaître dans le fluide sous-gingival après trois mois chez les patients atteints d’IRC.
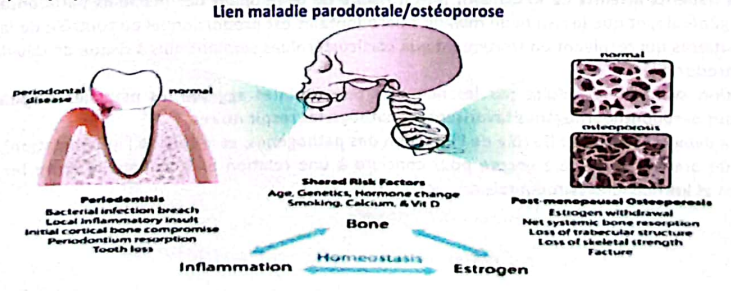
5. Ostéoporose
Selon l’OMS, l’ostéoporose est une maladie systémique du squelette caractérisée par :
- Une faible densité osseuse,
- Des altérations de la microarchitecture osseuse,
- Une fragilité osseuse accrue, augmentant le risque de fractures.
La densité minérale osseuse (DMO) est le principal déterminant de cette fragilité, selon les études biomécaniques. Les fractures, complication majeure de l’ostéoporose, en constituent toute la gravité.
Facteurs de risque communs avec les maladies parodontales :
- Âge,
- Tabac,
- Génétique,
- Changements hormonaux,
- Carences en calcium et vitamine D.
Lien inflammatoire :
Les mêmes cytokines pro-inflammatoires (IL-1, IL-6, TNF) sont impliquées dans l’ostéoporose et les MP, suggérant une association. Chez les femmes, l’œstradiol inhibe l’expression de certaines cytokines. Après la ménopause, la diminution de cette hormone lève cette inhibition, augmentant la libération de cytokines localement et systémiquement.
Effets de la carence en œstrogènes :
- Augmentation de l’expression des cytokines pro-inflammatoires,
- Réduction de la masse osseuse des maxillaires, favorisant la parodontite,
- Possible corrélation entre la DMO des septas interdentaires et la DMO vertébrale.
L’alvéolyse semble augmenter lorsque la densité osseuse des septas interdentaires diminue. Cependant, cette corrélation disparaît en tenant compte de paramètres parodontaux comme le saignement ou la plaque sous-gingivale, sauf chez les sujets âgés. Une étude de 2017 conclut que la carence en œstrogènes post-ménopause réduit la densité osseuse, entraînant une perte osseuse alvéolaire et potentiellement une perte dentaire.
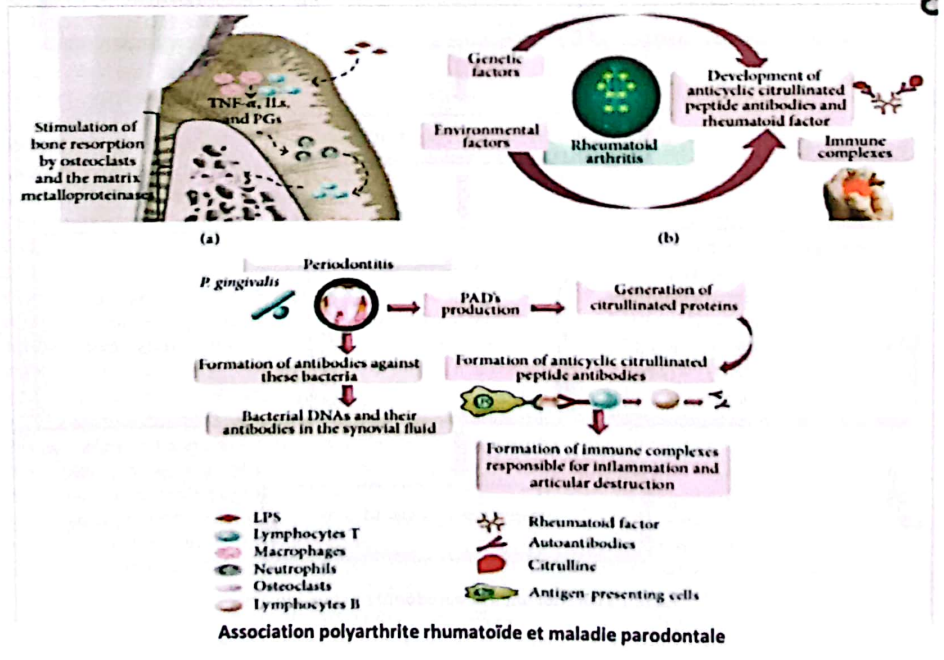
6. Maladie Parodontale et Polyarthrite Rhumatoïde
L’association entre les maladies parodontales (MP) et la polyarthrite rhumatoïde (PR) est significative. Leur physiopathologie repose sur une réponse immunitaire similaire, impliquant :
- Un profil commun de cellules inflammatoires et de cytokines pro-inflammatoires,
- Une relation bidirectionnelle entre la PR et la parodontite.
Facteurs de risque communs :
- Tabac,
- Génétique (notamment l’antigène HLA-DRB1 comme prédisposition partagée).
Rôle du tabac :
Le tabagisme actif augmente le stress oxydatif et la citrullination de protéines, accroissant le risque de PR, surtout chez les sujets génétiquement prédisposés. Ce risque persiste jusqu’à 20 ans après l’arrêt du tabac et est dose-dépendant.
Mécanismes :
La maladie parodontale favorise l’inflammation articulaire via le passage de bactéries (notamment Porphyromonas gingivalis – Pg) et de cytokines pro-inflammatoires dans le sang. Deux hypothèses expliquent ce lien :
- Une réponse immunitaire systémique par la production de cytokines et médiateurs inflammatoires,
- Le rôle spécifique de Pg, qui exprime la peptidyl arginine désiminase (PAD), catalysant la citrullination de l’arginine.
Pg est le seul procaryote connu à posséder cette enzyme. Des antigènes citrullinés sont présents dans le parodonte des patients atteints de MP, et les anticorps anti-Pg sont corrélés aux ACPA (anticorps anti-peptides cycliques citrullinés). Ainsi, Pg pourrait déclencher une réponse auto-immune précédant la PR en augmentant les protéines citrullinées, favorisant la production d’ACPA.
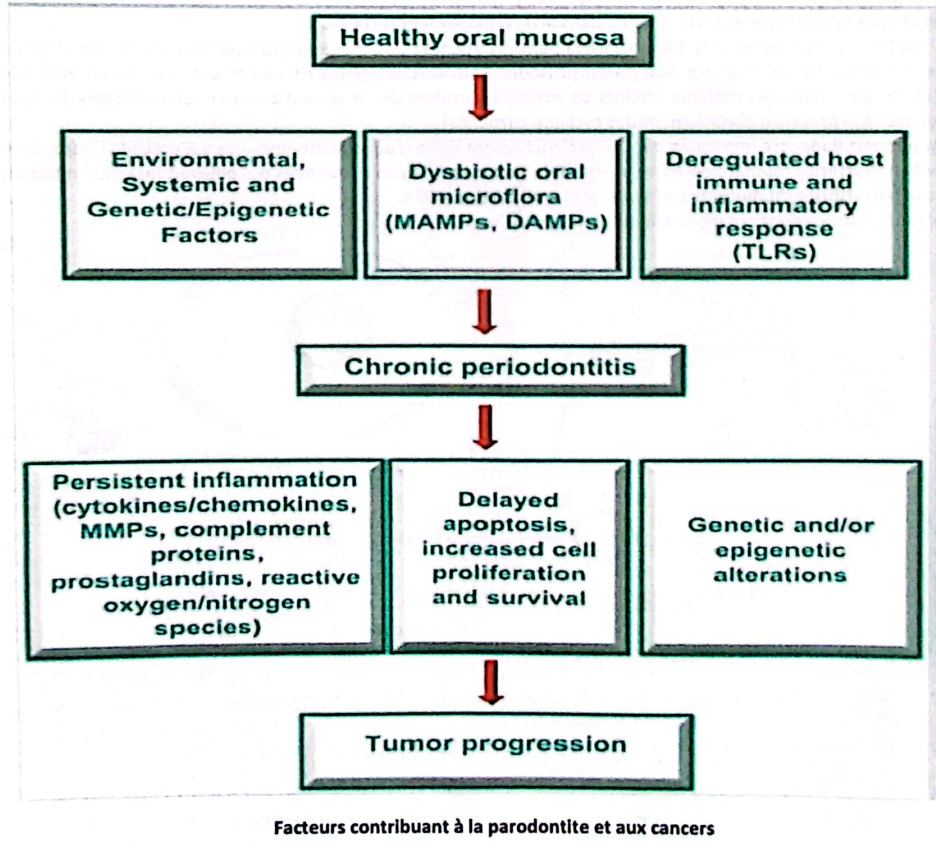
7. Maladies Parodontales et Cancers de la Topographie Gingivale
La parodontite chronique pourrait être liée au risque de cancer buccal par :
- Effets toxiques directs du microbiome oral et de ses produits,
- Effets indirects de l’inflammation buccale chronique.
Physiopathologie :
Les états inflammatoires chroniques et les dérégulations immunitaires dépendantes des cytokines jouent un rôle dans la carcinogenèse orale, modulant le microenvironnement tumoral. Certaines bactéries parodontopathogènes (Porphyromonas gingivalis – Pg, Fusobacterium nucleatum – Fn, Prevotella intermedia – Pi) sont associées aux carcinomes épidermoïdes oraux.
Lien avec le HPV :
Une étude sur les cancers de la base de la langue montre que les patients HPV-positifs présentent une perte osseuse plus importante que les HPV-négatifs, suggérant que la parodontite chronique pourrait influencer l’infection au HPV.
Hygiène orale :
Une mauvaise hygiène buccale est également associée aux carcinomes épidermoïdes oraux (OSCC). Bien que des mécanismes biologiques plausibles existent, l’étiologie exacte reste à établir, et il est incertain si cette relation est purement associative ou causale.
8. Relation Maladies Parodontales et Cardiopathies
Toute infection, quelle que soit sa porte d’entrée, est un facteur de risque de pathologies cardiaques. Les maladies parodontales, en tant qu’infections bactériennes, jouent un rôle non négligeable dans leur pathogenèse.
8.1. Maladies Parodontales et Endocardite Infectieuse
L’endocardite est une infection des parois endothéliales du cœur, précédée par une bactériémie transitoire liée à des actes bucco-dentaires. Les streptocoques (ex. Streptococcus sanguis), présents dans la plaque dentaire lors de gingivites ou parodontites, sont responsables de plus de 50 % des cas (Holmstrup et al., 2000). D’autres pathogènes comme Actinobacillus actinomycetemcomitans (Aa), Eikenella corrodens ou des Haemophilus spp. sont aussi incriminés.
Ces bactéries passent dans le sang après une rupture de la muqueuse gingivale (ex. détartrage, brossage, mastication), pouvant provoquer une endocardite chez les sujets prédisposés. Le risque est davantage lié à une mauvaise hygiène buccale et à des bactériémies chroniques qu’aux actes dentaires eux-mêmes.
Prévention : Antibioprophylaxie avant les actes bucco-dentaires et contrôle de l’inflammation parodontale.
8.2. Maladies Parodontales et Cardiopathies Ischémiques
Les cardiopathies ischémiques, dues à une réduction de l’apport en oxygène au cœur (souvent par athérosclérose coronarienne), sont associées à des facteurs de risque comme :
- Hypertension artérielle,
- Diabète,
- Tabagisme,
- Hypercholestérolémie,
- Infections microbiennes chroniques.
Des études montrent qu’une alvéolyse de 20 % augmente l’incidence des cardiopathies ischémiques de 40 %, et une alvéolyse de plus de 40 % multiplie par 2,7 le risque d’accidents ischémiques mortels.
8.3. Mécanismes Étiopathogéniques
Le rôle des MP dans les cardiopathies peut être :
- Direct : Porphyromonas gingivalis (Pg) favorise l’agrégation plaquettaire et la formation de thrombi, grâce à son pouvoir invasif des cellules épithéliales aortiques. Pg est retrouvé dans les athéromes coronaires et carotidiens.
- Indirect : Libération de lipopolysaccharides et de cytokines pro-inflammatoires (PGE2, IL-1b, TNF-α), entraînant un état hyper-inflammatoire.
La présence de pathogènes parodontaux dans les plaques d’athérome contribue à l’athérogenèse. De plus, les MP sont associées à l’hypertriglycéridémie, l’hypercholestérolémie et des niveaux élevés de CRP, marqueur d’inflammation et facteur de risque cardiovasculaire.
9. Maladie Parodontale et Maladie d’Alzheimer
Une étude américaine récente suggère qu’un déséquilibre des bactéries buccales pourrait augmenter le risque de maladie d’Alzheimer. Les personnes âgées avec plus de bactéries nocives que bénéfiques dans la bouche présentent davantage de bêta-amyloïde, un biomarqueur clé d’Alzheimer, dans le liquide céphalo-rachidien (LCR).
Méthodologie :
Des échantillons bactériens sous-gingivaux et des ponctions lombaires ont été réalisés chez des sujets âgés sains. Une faible concentration de bêta-amyloïde dans le LCR indique une accumulation cérébrale, liée à la formation de plaques amyloïdes et d’enchevêtrements de protéines tau, entraînant une dégénérescence neuronale.
Rôle des bactéries :
- Les bactéries nocives favorisent l’inflammation,
- Les bactéries saines maintiennent l’équilibre microbien et réduisent l’inflammation, potentiellement protectrices contre Alzheimer.
Porphyromonas gingivalis (Pg) et ses lipopolysaccharides ont été détectés dans le cerveau et le LCR de patients décédés d’Alzheimer. Pg pourrait contourner le système immunitaire, traverser la barrière hémato-encéphalique (altérée chez les patients âgés ou atteints d’Alzheimer), et aggraver l’inflammation cérébrale, influençant la progression de la maladie.
Conclusion
Les maladies parodontales (MP), inflammatoires et infectieuses, sont multifactorielle et très répandues. Leurs formes sévères sont la principale cause de perte dentaire chez l’adulte. Les bactéries impliquées contribuent directement ou indirectement à une inflammation systémique. Des études établissent des liens entre les parodontites et diverses maladies systémiques (rénale, osseuse, rhumatoïde, cancéreuse, cardiaque, neurologique). Bien que constituant un facteur de risque faible mais constant, le traitement parodontal et une bonne hygiène bucco-dentaire réduisent leur incidence.
INFLUENCE DES MALADIES PARODONTALES SUR L’ÉTAT GÉNÉRAL
Voici une sélection de livres:
Parodontologie Relié – 1 novembre 2005
Guide pratique de chirurgie parodontale Broché – 19 octobre 2011
Parodontologie Broché – 19 septembre 1996
MEDECINE ORALE ET CHIRURGIE ORALE PARODONTOLOGIE
Parodontologie: Le contrôle du facteur bactérien par le practicien et par le patient
Parodontologie clinique: Dentisterie implantaire, traitements et santé
Parodontologie & Dentisterie implantaire : Volume 1
Endodontie, prothese et parodontologie
La parodontologie tout simplement Broché – Grand livre, 1 juillet 2020


Leave a Reply