Le Collagène en Odontologie : Comprendre sa Structure, sa Synthèse et sa Dégradation
Introduction : Pourquoi le Collagène est Crucial en Dentisterie
Le collagène représente bien plus qu’une simple protéine structurale : c’est le pilier fondamental de tous les tissus dentaires, à l’exception de l’émail. Cette macromolécule protéinique constitue entre 30 et 35% des protéines totales de l’organisme humain, ce qui en fait la protéine la plus abondante du règne animal.
Pour comprendre l’importance du collagène en odontologie, considérez cette statistique : les fibres de collagène représentent 90% des tissus de soutien parodontaux. En France, selon le rapport 2024-2025 sur la santé buccodentaire, 83% des adultes présentent des signes de maladie parodontale, où la dégradation du collagène joue un rôle central.
Sécrété par les fibroblastes, le collagène intervient dans le développement, la structure et la physiologie de la dent et de ses tissus de soutien. Sa compréhension approfondie est donc essentielle pour tout étudiant en odontologie.

Définition et Concept Fondamental
Le terme “collagène” provient du grec et signifie littéralement “producteur de colle”. Cette étymologie reflète parfaitement sa fonction biologique : le collagène agit comme une “colle moléculaire” qui retient et forme l’ensemble des tissus conjonctifs du corps.
Où trouve-t-on le collagène ?
- Os et cartilages
- Muscles, tendons et ligaments
- Peau
- Dentine, gencive et pulpe dentaire
- Ligament alvéolo-dentaire (LAD)
- Cément
En pratique clinique, chaque fois qu’un chirurgien-dentiste travaille sur les tissus mous ou réalise une chirurgie parodontale, il manipule directement des structures riches en collagène.

Structure Moléculaire du Collagène
Le Tropocollagène : L’Unité de Base
Le tropocollagène représente l’unité moléculaire fondamentale du collagène fibreux insoluble. Ses caractéristiques structurales sont précises :
Caractéristiques du tropocollagène :
- Poids moléculaire : 300 000 Da
- Longueur : 2800 à 3000 Angströms (Å)
- Largeur : 14 Å
- Composition : 3 chaînes polypeptidiques (chaînes α) enroulées en triple hélice
- Poids moléculaire de chaque chaîne α : 96 000 Da
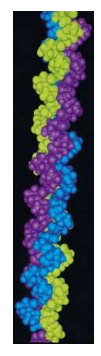
Cette organisation en triple hélice confère au collagène sa remarquable résistance mécanique et son élasticité, propriétés essentielles pour les tissus de soutien dentaire.
Les Différents Types de Chaînes Alpha
En fonction de la répartition des acides aminés, on distingue 5 types de chaînes α :
- 4 chaînes dites α1 (types 1, 2, 3 et 4)
- 1 chaîne dite α2
Exemple concret : Le collagène de type I, le plus abondant dans le parodonte, est constitué de deux chaînes α1 type I et une chaîne α2. Cette composition spécifique lui confère des propriétés mécaniques optimales pour résister aux forces masticatoires.

Typologie et Localisation des Collagènes
La répartition des 5 chaînes α au sein de la molécule détermine plusieurs types de collagène, chacun ayant une localisation et une fonction spécifiques :
| Type | Composition | Localisation | Importance Clinique |
|---|---|---|---|
| Type I | 2 chaînes α1 type I + 1 chaîne α2 | Peau, os, tendons, dentine, gencive, pulpe | Le plus abondant ; essentiel en parodontologie et chirurgie |
| Type II | 3 chaînes α1 type II | Cartilage | Important pour l’ATM (articulation temporo-mandibulaire) |
| Type III | 3 chaînes α1 type III | Vaisseaux sanguins, peau, gencive, pulpe | Impliqué dans la cicatrisation gingivale |
| Type IV | 3 chaînes α1 type IV | Membranes basales | Essentiel pour l’intégrité épithéliale |
| Type V | Chaînes αA et αB | Placenta, muscles lisses | Régulation de la fibrillogenèse |
Application pratique : Lors d’une chirurgie parodontale, la régénération tissulaire fait intervenir principalement les collagènes de types I et III. Les innovations récentes en régénération parodontale utilisent des membranes de collagène biocompatibles pour favoriser la reconstruction des tissus de soutien.

Rôles Biologiques et Fonctions du Collagène
Fonction Structurale
Le collagène sert de matériau de construction pour divers tissus conjonctifs. En tant que protéine fibreuse, il confère aux tissus :
- Une résistance mécanique accrue
- Une élasticité supérieure
- Une cohésion tissulaire optimale
Comparaison clinique : Les tissus riches en collagène (gencive attachée, ligament parodontal) sont beaucoup plus résistants aux forces de traction que les tissus pauvres en collagène. Cette différence explique pourquoi la gencive attachée kératinisée résiste mieux aux agressions mécaniques du brossage.

Double Rôle Biologique
Le rôle du collagène est double :
1. Composant de la matrice extracellulaire Avec l’élastine, les protéoglycanes et les glycoprotéines, le collagène forme la matrice extracellulaire responsable de la cohésion des tissus et des organes.
2. Conféreur de propriétés mécaniques Il assure la résistance, la souplesse et l’élasticité des différents tissus.
Conséquence clinique importante : Les altérations du collagène se répercutent sur le fonctionnement de nombreux tissus et organes. C’est pourquoi les maladies systémiques affectant le métabolisme du collagène (scorbut, syndrome d’Ehlers-Danlos) présentent souvent des manifestations bucco-dentaires.
Pour approfondir vos connaissances sur les pathologies parodontales et le rôle du collagène, le Référentiel internat en parodontologie constitue une ressource incontournable pour les étudiants en odontologie préparant l’internat.
Biosynthèse du Collagène : Un Processus Complexe
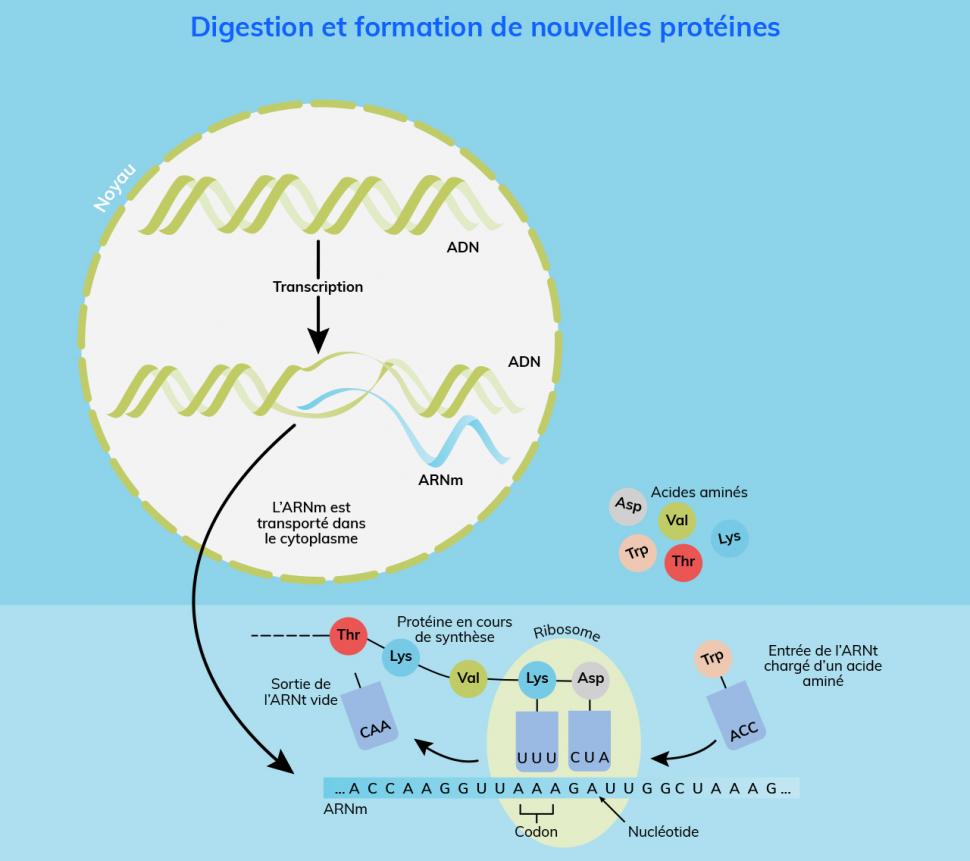
La biosynthèse du collagène se déroule dans les fibroblastes, cellules responsables également de sa dégradation. Au cours de la biosynthèse intracellulaire, le collagène est appelé protropocollagène.
Étape 1 : Synthèse au Niveau du Réticulum Endoplasmique Granuleux
a) Synthèse et assemblage initial Les acides aminés sont synthétisés puis assemblés en chaînes polypeptidiques pro-alpha.
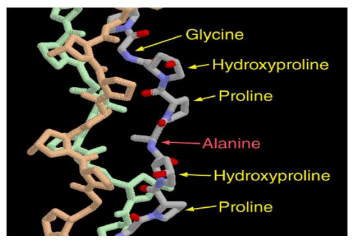
b) Hydroxylation : étape dépendante de la vitamine C Un groupe hydroxyle (OH) est greffé sur certains acides aminés :
- Lysine → Hydroxylysine
- Proline → Hydroxyproline
Cette réaction nécessite deux enzymes spécifiques (lysine hydroxylase et proline hydroxylase) et dépend crucially de l’oxygène et de la vitamine C.
Importance clinique du scorbut : Le scorbut (carence en vitamine C) entraîne une synthèse défectueuse du collagène. Les manifestations bucco-dentaires incluent des gingivites hémorragiques sévères, un déchaussement dentaire et une mauvaise cicatrisation. Ce cas clinique illustre l’importance de la vitamine C dans le métabolisme du collagène.

c) Formation de la triple hélice
- Liaison des chaînes pro-alpha par groupes de trois via des ponts disulfures
- Enroulement de la molécule en triple hélice caractéristique

Étape 2 : Glycosylation au Niveau de l’Appareil de Golgi
La triple hélice quitte le réticulum endoplasmique vers l’appareil de Golgi où elle subit une glycosylation :
- Branchement d’unités monosaccharidiques (galactose)
- Ou disaccharidiques (glucose + galactose)
- Catalysée par l’enzyme glycosyl transférase
Étape 3 : Exocytose
L’appareil de Golgi se fragmente à ses extrémités pour former des vésicules d’exocytose contenant le protropocollagène. Ces vésicules fusionnent avec la membrane cytoplasmique pour libérer leur contenu dans le milieu extracellulaire.
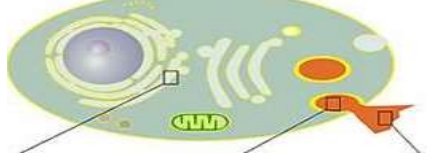
Schéma récapitulatif du processus : REG → Appareil de Golgi → Vésicules d’exocytose → Milieu extracellulaire
Maturation Extracellulaire du Collagène
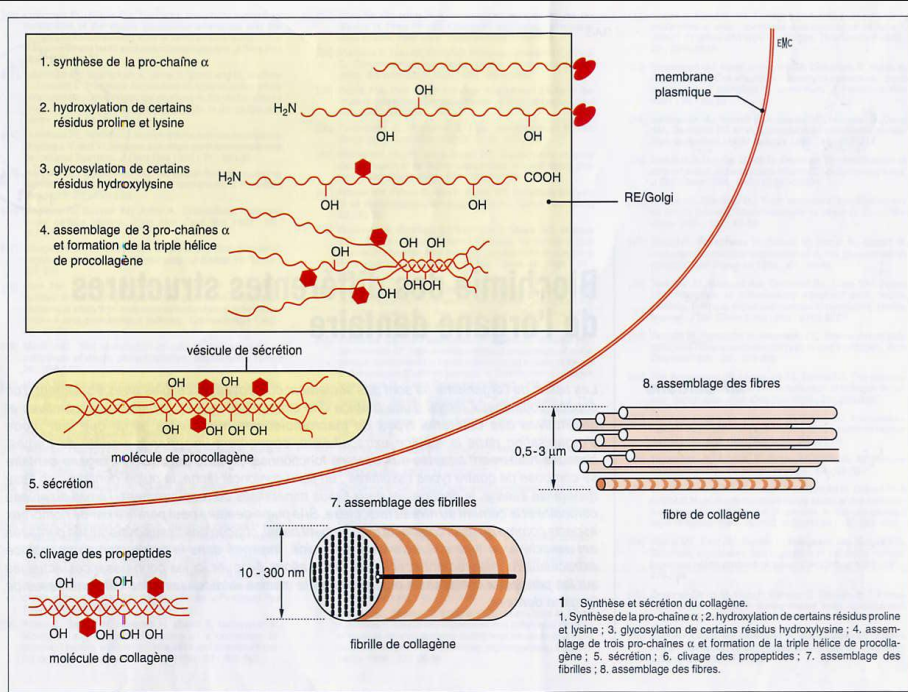
La maturation du collagène s’effectue dans le milieu extracellulaire et transforme le tropocollagène (collagène natif) en collagène mature et insoluble.
Formation des Cross-Links (Liaisons Croisées)
Processus de réticulation :
- Attachement des molécules de tropocollagène entre elles
- Formation de liaisons intermoléculaires (cross-links) via la réaction de Schiff
- Assemblage en fibrilles de 200 à 2000 Å de diamètre

Observation en microscopie électronique : Les fibrilles de collagène présentent des striations transversales caractéristiques avec une périodicité de 640 Å. Cette organisation résulte de l’arrangement décalé des molécules : chaque molécule est décalée de 1/4 de sa longueur par rapport à la molécule adjacente.

Signification clinique : Ces striations permettent l’identification du collagène en microscopie électronique lors d’analyses histologiques de biopsies parodontales.
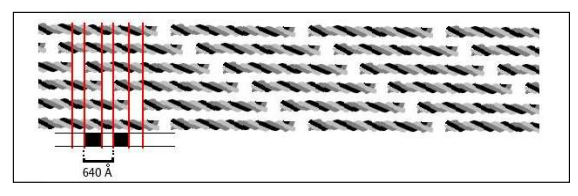
Interaction avec la Substance Fondamentale
Les fibrilles de collagène interagissent avec les composants de la substance fondamentale :
Glycosaminoglycanes (GAG) :
- Polymères d’unités disaccharidiques
- Composés d’acide uronique + hexosamine
- Exemples : acide hyaluronique, chondroïtine sulfate
Protéoglycanes :
- Formation par liaison des GAG avec des protéines
- Attachement aux fibrilles de collagène via leurs chaînes saccharidiques
- Conséquence : Augmentation de la réticulation et de l’insolubilité du collagène
Innovation récente : Les thérapies régénératives parodontales utilisent désormais des hydrogels de collagène combinés à de l’acide hyaluronique pour optimiser la cicatrisation gingivale. Des études récentes montrent une amélioration de 40% de la régénération par rapport aux techniques conventionnelles.
Turn-Over du Collagène : Un Renouvellement Permanent
Le turn-over désigne le renouvellement permanent d’une partie du collagène, consistant en une dégradation suivie d’une synthèse de nouvelles molécules.
Vitesse de renouvellement selon les tissus :
- Ligament alvéolo-dentaire (LAD) : Turn-over le plus rapide
- Gencive et os alvéolaire : 5 fois plus lent que le LAD
- Peau : 15 fois plus lent que le LAD
Facteur d’âge : Ce phénomène diminue progressivement avec l’âge, ce qui explique partiellement la susceptibilité accrue aux maladies parodontales chez les personnes âgées.
Implication clinique : La rapidité du turn-over du LAD explique pourquoi les dents peuvent se déplacer orthodontiquement. C’est aussi pourquoi le LAD répond rapidement aux stimuli inflammatoires dans la parodontite.
Dégradation Physiologique du Collagène
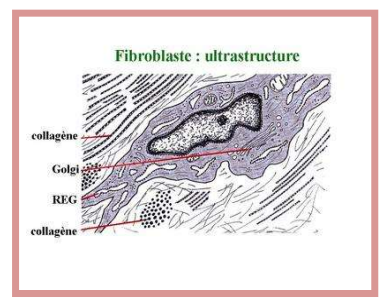
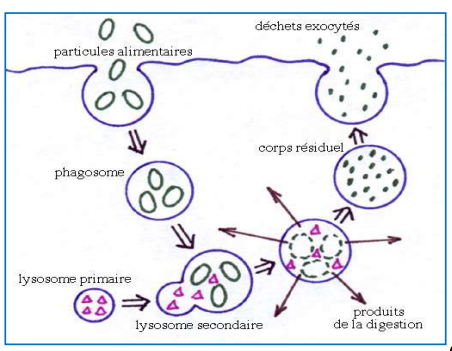
Mécanisme 1 : Dégradation Phagocytaire
La phagocytose permet à une cellule d’absorber un élément extracellulaire solide et de le digérer.
Acteurs de la phagocytose :
- Membrane cytoplasmique : Forme les phagosomes contenant le corps à phagocyter
- Lysosomes : Structures membranaires remplies d’enzymes hydrolytiques
Rôle du fibroblaste : Cette cellule est responsable à la fois de la synthèse et de la dégradation du collagène. Lorsqu’un fibroblaste s’apprête à phagocyter, de la collagénase apparaît sur sa surface membranaire. Cette enzyme fragmente la molécule de collagène, la rendant vulnérable aux enzymes hydrolytiques des lysosomes.
Mécanisme 2 : Dégradation Enzymatique
La collagénase tissulaire : enzyme clé de la dégradation
Dans les conditions physiologiques normales, le collagène peut être détruit par la collagénase tissulaire.
Caractéristiques de la collagénase :
- Poids moléculaire : 25 000 à 100 000 Da
- Présente dans le milieu extracellulaire sous forme inactive (procollagénase)
- Activation par des activateurs spécifiques → collagénase tissulaire active
- Peut être inactivée par des inhibiteurs
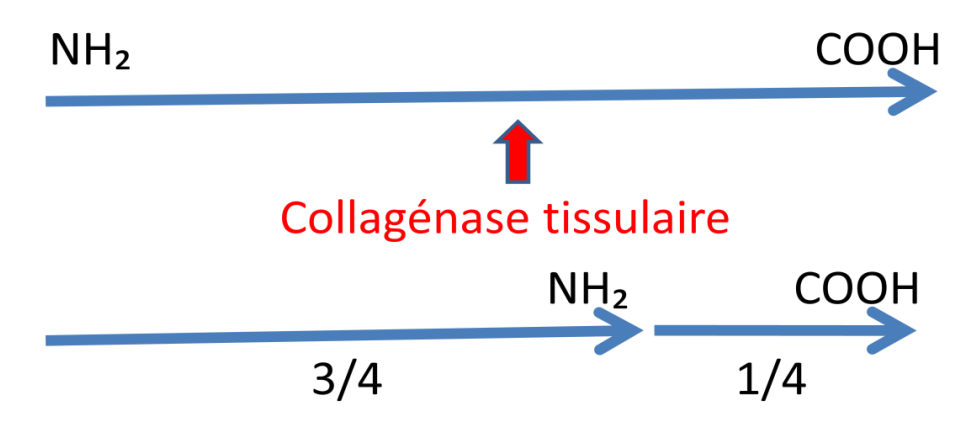
Mécanisme d’action à pH neutre et 37°C : La collagénase coupe la molécule de collagène natif en deux fragments d’inégale longueur :
- Fragment 3/4 : contient l’extrémité NH₂ terminale
- Fragment 1/4 : renferme l’extrémité COOH terminale
Ces fragments sont ensuite métabolisés par les enzymes protéolytiques en peptides, puis en acides aminés.
Facteurs de Régulation de l’Activité Collagénolytique
1. Type de collagène Le collagène de type II est plus résistant que le type I.
2. Âge L’augmentation des cross-links intra et intermoléculaires avec l’âge rend le collagène plus résistant à la dégradation.
3. Conditions physico-chimiques
- Variations du pH
- Variations de température
4. Facteurs biologiques
- Certaines protéines
- Hormones
Signification clinique : La compréhension de ces facteurs permet d’optimiser les conditions de cicatrisation post-chirurgicale et de comprendre pourquoi certains patients répondent mieux aux traitements parodontaux.
Pour une compréhension approfondie des mécanismes physiopathologiques en parodontologie, les Annales corrigées de l’internat en odontologie 2022-2024 offrent des cas cliniques commentés et des QCM corrigés essentiels pour la préparation à l’internat.
Dégradation Pathologique du Collagène

La destruction pathologique du collagène se réalise soit par amplification des mécanismes enzymatiques, soit par accentuation du mécanisme phagocytaire.
Augmentation de la Destruction Enzymatique
A. Augmentation Spontanée de l’Activité Collagénasique Tissulaire
Cette augmentation est liée à :
- Diminution quantitative des inhibiteurs de collagénase
- Augmentation des activateurs
Point crucial : La sécrétion de collagénase tissulaire est particulièrement intense en période inflammatoire. Dans la maladie parodontale, cette hyperactivité enzymatique est un mécanisme pathogénique central.
B. Augmentation par Arrivée d’Éléments Extérieurs
1. Bactéries impliquées
Bacteroides melaninogenicus (Porphyromonas gingivalis) : Cette bactérie parodontopathogène peut agir :
- Directement par sa propre collagénase
- Indirectement par ses endotoxines qui activent la transformation de la procollagénase osseuse en collagénase active
Bactéries de la plaque dentaire : Les bactéries du sillon gingival peuvent activer la réaction pro-enzyme → enzyme. La plupart des bactéries impliquées dans la maladie parodontale sécrètent des enzymes protéolytiques qui dégradent les peptides résultant du fractionnement des chaînes α.
Application clinique : C’est pourquoi le contrôle de la plaque bactérienne par détartrage et surfaçage radiculaire est la pierre angulaire du traitement parodontal. L’élimination des bactéries réduit la production de collagénases exogènes.
2. Cellules inflammatoires
Leucocytes polynucléaires neutrophiles (PNN) :
- Leur nombre augmente considérablement au cours d’une inflammation
- Sécrètent une collagénase tissulaire capable d’hydrolyser le collagène natif (Lazarus et al., 1968)
- Contribuent de manière majeure à la destruction du ligament parodontal
Macrophages : Les macrophages contribuent à la destruction du collagène des tissus parodontaux par le biais de leur collagénase tissulaire lors de la maladie parodontale.
Chiffre clé : Dans une poche parodontale active, on peut observer jusqu’à 100 fois plus de PNN que dans un sillon gingival sain.
Augmentation de l’Activité Phagocytaire
Cette augmentation implique :
- Macrophages : Phagocytose + activité collagénolytique simultanée
- Fibroblastes : N’augmentent pas en nombre durant la maladie parodontale mais phagocytent le collagène en plus grande quantité
Paradoxe clinique : Les fibroblastes, normalement responsables de la synthèse du collagène, deviennent des agents de destruction dans un environnement inflammatoire chronique.
Applications Cliniques et Innovations Récentes
Thérapies Régénératives Basées sur le Collagène
Membranes de collagène résorbables Les membranes en collagène représentent l’approche de référence en régénération tissulaire guidée (RTG). Les nouvelles générations intègrent :
- Des peptides bioactifs
- Des ions (strontium, zinc)
- Des facteurs de croissance
Hydrogels de collagène + FGF-2 Des recherches récentes ont développé des hydrogels de collagène combinés au facteur de croissance des fibroblastes-2 (FGF-2). Ces biomatériaux en forme d’éponge montrent :
- Une excellente biodégradabilité
- Une efficacité supérieure pour régénérer le tissu parodontal (cément, ligament, os alvéolaire)
- Une qualité de tissu régénéré confirmée à l’examen histologique
- Une résistance appropriée aux forces masticatoires
Plasma Riche en Plaquettes (PRP) et PRF
Le plasma riche en fibrine (PRF) et le PRP enrichis en vitamine C montrent des résultats prometteurs. Leur efficacité repose sur la libération progressive de facteurs de croissance qui stimulent :
- La néoangiogenèse
- La différenciation cellulaire
- La synthèse de collagène
Données récentes (2024-2025) : Ces approches régénératives améliorent la cicatrisation de 40% par rapport aux techniques conventionnelles.
Prévention de la Dégradation du Collagène
Contrôle des facteurs de risque :
- Tabac : L’arrêt du tabagisme divise par 5 le risque de parodontite
- Nutrition : Apport adéquat en vitamine C et D
- Hygiène bucco-dentaire : Élimination régulière de la plaque bactérienne
Maintenance parodontale : Des séances de détartrage professionnel tous les 3 à 6 mois réduisent de 70% le risque de récidive parodontale.

Perspectives Futures et Recherche
Médecine Personnalisée
Des tests génétiques peuvent désormais identifier les polymorphismes génétiques prédisposant à une dégradation excessive du collagène. Cette approche permet :
- Une prévention ciblée
- Un ajustement des intervalles de maintenance
- Une identification précoce des patients à risque
Biomatériaux de Nouvelle Génération
La recherche se concentre sur :
- Membranes 3D imprimées sur mesure
- Céramiques bioactives dopées aux ions
- Scaffolds combinant collagène et facteurs de croissance
Objectif : Passer de la stabilisation à la régénération complète des tissus parodontaux.
Thérapies Ciblées Anti-Inflammatoires
Des essais cliniques (2025) testent des molécules ciblant spécifiquement l’interleukine-1β pour moduler la réponse inflammatoire excessive responsable de la destruction du collagène.
Points Clés à Retenir pour les Étudiants
Structure et composition :
- Le tropocollagène = unité de base (3 chaînes α en triple hélice)
- 5 types majeurs de collagène, le type I étant prédominant en parodontie
- 90% des tissus de soutien parodontaux sont constitués de fibres de collagène
Biosynthèse :
- Synthèse intracellulaire (REG) → maturation extracellulaire
- Hydroxylation dépendante de la vitamine C (importance du scorbut)
- Formation de cross-links augmentant la résistance
Turn-over :
- Variable selon les tissus (LAD > gencive > peau)
- Diminue avec l’âge
- Permet le remodelage permanent des tissus
Dégradation :
- Physiologique : phagocytaire + enzymatique (collagénase)
- Pathologique : amplification dans la maladie parodontale
- Médiée par les bactéries et les cellules inflammatoires
Applications cliniques :
- Régénération tissulaire guidée (membranes de collagène)
- PRP/PRF pour stimuler la régénération
- Importance du contrôle de la plaque et des facteurs de risque
Pour consolider vos connaissances et vous préparer efficacement à l’internat, le Guide clinique d’odontologie offre une synthèse complète et pratique des principaux concepts cliniques, incluant des protocoles détaillés en parodontologie.
Conclusion : Le Collagène, Pilier de la Santé Parodontale
Le collagène constitue un composant essentiel et irremplaçable des tissus conjonctifs du parodonte. Il intervient dans tous les aspects de la santé parodontale : développement, maintien structurel, cicatrisation et régénération.
Compréhension clinique essentielle : L’équilibre entre synthèse et dégradation du collagène détermine la santé ou la maladie du parodonte. Une synthèse déficiente (carence en vitamine C, maladies systémiques) ou une dégradation excessive (inflammation, bactéries parodontopathogènes) aboutissent à des pathologies parodontales.
Message pour les futurs praticiens : La maîtrise du métabolisme du collagène est fondamentale pour :
- Comprendre la physiopathologie des maladies parodontales
- Optimiser les protocoles thérapeutiques
- Améliorer le pronostic de vos traitements
- Conseiller efficacement vos patients sur la prévention
Les innovations récentes en thérapie régénérative offrent des perspectives prometteuses. Avec une prévalence de 83% de maladies parodontales chez les adultes français, la compréhension approfondie du métabolisme du collagène devient un enjeu majeur de santé publique.
Conseil pratique : Intégrez systématiquement dans vos consultations l’évaluation des facteurs influençant le métabolisme du collagène : état nutritionnel (vitamine C, D), tabagisme, contrôle glycémique chez les diabétiques, et qualité de l’hygiène bucco-dentaire.

Ressources Complémentaires pour Approfondir
Ouvrages de référence recommandés :
- Référentiel internat en parodontologie – Indispensable pour l’internat
- Annales corrigées de l’internat en odontologie 2022-2024 – Préparation complète
- Guide clinique d’odontologie – Synthèse pratique
- Endodontie, prothèse et parodontologie – Approche multidisciplinaire
Plateforme de QCM en ligne : Pour tester vos connaissances sur le collagène et la parodontologie, consultez ResiDentaire™ – Plateforme QCM Médecine Dentaire, une ressource précieuse pour la préparation à l’internat.
Note de transparence : Cette page contient des liens d’affiliation Amazon. En cliquant dessus, vous n’êtes pas tenu de vous procurer les produits suggérés, mais si vous le faites, cela ne vous coûte rien de plus et cela m’aide à financer ce site et à continuer de créer du contenu pédagogique gratuit pour les étudiants en odontologie.
Dernière mise à jour : Février 2026 | Auteur : Contenu pédagogique destiné aux étudiants en odontologie
Leave a Reply