Cicatrisation parodontale / Parodontologie
Cicatrisation parodontale / Parodontologie
Introduction
Comme tous les organes, le parodonte répond aux agressions d’origine traumatique, bactérienne, virale ou chirurgicale par l’initiation de mécanismes de cicatrisation qui visent à préserver la survie de l’organe concerné. Ces événements se déroulent de manière spécifique et prévisible et sont sous-tendus par de grands principes biologiques.
Rappels
Hémostase
Ensemble des mécanismes physiologiques qui assurent l’obturation de toute rupture du circuit vasculaire et la prévention du saignement spontané.
Comporte plusieurs étapes intégrées et indépendantes :
- Hémostase primaire : Ferme la brèche vasculaire par un “thrombus blanc” (clou plaquettaire).
- Hémostase secondaire (coagulation plasmatique) : Consolide ce premier thrombus en formant un réseau de fibrine emprisonnant des globules rouges (thrombus rouge ou caillot sanguin).
- Fibrinolyse : Permet la destruction du caillot ou la limitation de son extension.
Inflammation
L’inflammation est un processus dynamique constitué par un ensemble de réactions vasculaires, cellulaires et hormonales, déclenché par toute agression qu’elle soit d’origine mécanique, chimique, thermique, infectieuse, etc. Elle permet l’élimination de l’agent agresseur, des débris cellulaires, et la réparation des tissus lésés. La réparation correspond à la cicatrisation.
La réponse inflammatoire comprend :
- La vasodilatation des capillaires.
- L’exsudation des globules blancs.
- La détersion : Élimination des germes, tissus nécrotiques et corps étrangers par les polymorphonucleaires et les macrophages.
- La réparation : Formation d’un bourgeon charnu.
Définitions
Cicatrisation
Processus biologique par lequel un organe ou un tissu lésé se répare pour retrouver sa forme ou sa fonction initiale.
Réparation
Cicatrisation d’une lésion par un tissu qui ne restaure pas entièrement l’architecture ou la fonction du tissu concerné.
Régénération
Reconstitution de l’architecture et de la fonction d’un tissu lésé ou détruit.
Réattache
Réunion du tissu conjonctif à la dent après séparation de ces deux éléments par incision ou blessure.
Nouvelle attache
Réunion du tissu conjonctif à une surface radiculaire exposée en raison de l’évolution d’un processus pathologique (formation d’un nouveau cément et de fibres de collagène insérées dans ce néo-cément).
Classifications de la cicatrisation
Krammer
Relative :
- Aux tissus concernés (épithélium, conjonctif).
- Aux types de cicatrisation (première, deuxième intention).
- Aux types de chirurgie.
Schröder 1982
- Au niveau de l’épithélium :
- Régénération épithéliale (néo-attachement).
- Réattachement épithélial.
- Au niveau du tissu conjonctif :
- Régénération du tissu conjonctif (néo-attachement).
- Réattachement du tissu conjonctif.
Bouchard-Étienne 1993
- Cicatrisation par première intention : En présence d’une incision chirurgicale où les deux berges peuvent être étroitement coaptées par suture.
- Cicatrisation par seconde intention : Lorsque les deux berges de la plaie ne peuvent pas être coaptées et qu’une quantité importante de tissu a été détruite.

Étapes morphologiques de la cicatrisation
Mécanisme de la cicatrisation
Le mécanisme de la cicatrisation se déroule en quatre phases :
- Hémostase
- Inflammation
- Prolifération, granulation
- Remodelage, maturation
Hémostase
Les vaisseaux sanguins abîmés doivent être scellés. Les plaquettes sécrètent des substances vasoconstrictrices, mais leur rôle principal consiste en la formation d’un caillot stable. Elles sécrètent également la thrombine qui déclenche la formation de la fibrine à partir du fibrinogène. Les plaquettes libèrent aussi des cytokines pour initier les prochaines étapes. L’hémostase se produit dans les minutes suivant la blessure initiale.
Inflammation
La réponse inflammatoire cause une fuite dans les vaisseaux sanguins, relâchant du plasma et des polynucléaires (PMN) dans les tissus environnants. Les neutrophiles phagocytent les débris et les microorganismes, offrant une première mesure de prévention de l’infection (détersion). À mesure que la fibrine se décompose, elle libère des produits de dégradation attirant les macrophages, qui phagocytent les bactéries, constituant une seconde mesure de prévention (détersion).
Prolifération, granulation
La réparation tissulaire commence par la formation d’un tissu de granulation (bourgeon charnu), un tissu transitoire mis en place après la détersion, visant à combler une perte de substance tissulaire par un tissu fibreux. Le terme granulation vient de l’apparence granulaire du tissu observée cliniquement, due à la formation de nombreux bourgeons vasculaires.
Le bourgeon charnu est constitué de :
- Fibroblastes : Sécrètent les composants de la matrice extracellulaire.
- Myofibroblastes.
- Vaisseaux capillaires néoformés : Les bourgeons endothéliaux naissent à partir des anses capillaires du tissu non lésé en bordure du granulome inflammatoire. Ces bourgeons colonisent le granulome et forment un réseau vasculaire qui s’organise progressivement.
Juste après la détersion, le bourgeon charnu est un tissu conjonctif jeune, œdémateux, pauvre en collagène et en vaisseaux, riche en fibroblastes et en cellules inflammatoires. Progressivement, il s’appauvrit en cellules inflammatoires, s’enrichit en collagène et en vaisseaux, passant d’un réseau capillaire indifférencié à un réseau proche de la normale.
Remodelage, maturation
La perte de substance se rétracte en raison de la contraction du bourgeon charnu. Cette contracture se produit lorsque les kératinocytes se différencient pour former un nouvel épithélium (épithélialisation). Au terme de ce processus, un tissu fibreux dense cicatriciel s’est constitué et peut se remodeler. Le remodelage consiste en une modification de l’orientation des fibres de collagène, qui tendent à se disposer selon les lignes de plus fortes tensions, comme dans un tissu conjonctif normal.
Cicatrisation par première intention
Se produit lorsque les deux berges d’une plaie (chirurgicale ou traumatique) peuvent être étroitement coaptées et que les tissus sont de même nature (Mattson et Porth, 1990). Exemple : cicatrisation d’une greffe gingivale 8 jours après intervention, rapide car les tissus en contact sont de même nature.

La plaie est fermée par des sutures, et la cicatrisation comprend deux aspects :
Réparation conjonctive
Divisée en trois phases :
- Phase d’inflammation ou de latence :
- Formation d’un caillot de fibrine en 10 minutes.
- Détersion par les neutrophiles et les macrophages (entre la 1ère et 6ème heure).
- Augmentation de la réponse inflammatoire (au bout de 24h).
- Phase de réparation :
- Formation du tissu de granulation (au bout de 3 jours).
- Néoformation capillaire.
- Activité fibroblastique importante.
- Phase de maturation :
- Formation de matrice de collagène (au bout de 7 jours).
- Remodelage fonctionnel des tissus terminé au 14ème jour.
- Formation de néocément au bout de 3 semaines.
Réparation épithéliale
La paroi radiculaire est perçue comme un obstacle à la cicatrisation épithéliale. Les cellules migrent en direction apicale pour former un long épithélium de jonction (dans la plupart des cas).

Cicatrisation par seconde intention
Se produit lorsque les deux berges de la plaie ne peuvent pas être coaptées et qu’une quantité importante de tissus a été détruite (ex. : après gingivectomie, approfondissement vestibulaire, ou exposition osseuse après lambeau). Le tissu de granulation formé est volumineux, et l’épithélium doit couvrir la plaie par migration centripète (de la périphérie vers le centre).

Bien que la réaction inflammatoire suive les mêmes mécanismes que la cicatrisation de première intention, le temps de cicatrisation est plus long et la réaction inflammatoire plus intense en raison de plus grandes quantités de fibrine et de tissus nécrotiques. Après une gingivectomie, cette cicatrisation se fait lentement en 2 à 3 semaines.
Modalités cicatricielles du parodonte
Qu’elle soit due à une destruction par infection ou par plaie chirurgicale, la cicatrisation des plaies parodontales est soumise aux règles générales : les tissus mous vascularisés doivent se réattacher à des tissus durs non vascularisés. En 1976, Melcher postulait que les cellules colonisant la surface radiculaire après une intervention chirurgicale déterminaient la nature de l’attache formée.
Après une incision à biseau interne et l’élimination du tissu de granulation, la surface radiculaire curetée peut être colonisée par quatre types cellulaires : cellules épithéliales, cellules du tissu conjonctif gingival, cellules osseuses, et cellules du desmodonte. La cicatrisation parodontale peut se faire par l’un des quatre processus suivants :
Long épithélium de jonction
Si les cellules de l’épithélium buccal prolifèrent le long de la surface radiculaire pour atteindre le niveau de l’épithélium de la poche avant l’intervention, une attache épithéliale se constitue (épithélium de jonction long). Le contact entre la surface radiculaire et cet épithélium est assuré par des structures cuticulaires et des hémi-desmosomes.
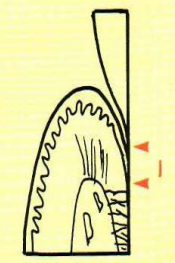
Adaptation conjonctive
Si des cellules conjonctives du tissu conjonctif gingival colonisent la surface radiculaire, une adhésion tissulaire conjonctive ou attache conjonctive s’établit.

Ankylose
Si des cellules osseuses viennent au contact de la surface radiculaire curetée, une résorption radiculaire superficielle et une ankylose peuvent se produire.
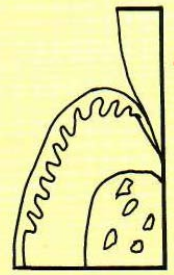
Régénération parodontale
Dans des conditions idéales, des cellules du desmodonte prolifèrent en direction coronaire pour recouvrir la surface radiculaire malade. Ces cellules forment du cément et des fibres desmodontales.

Principes biologiques de la cicatrisation parodontale
- Préparation des surfaces radiculaires : Restituer l’histocompatibilité après ablation des bactéries et toxines.
- Stabilité précoce du caillot sanguin : Potentialisée par le mordançage de la surface radiculaire (acide citrique), qui augmente le relief dentinaire par exposition des fibres collagéniques.
- Respect du volume du caillot sanguin : Maintenu par :
- Matériau de substitution osseuse.
- Membrane implantée.
- Adhésion du caillot sanguin : Assurée par un contact intime de la paroi interne du lambeau à la surface radiculaire et un caillot initial fin.
Cicatrisation consécutive à la thérapeutique parodontale
Le traitement parodontal vise à réduire la profondeur des poches par rétraction tissulaire et attache des tissus gingivaux.
Détartrage

- Immédiatement après : L’attache épithéliale est rompue.
- 2 heures après : Présence de nombreuses cellules polynucléaires parmi les cellules épithéliales sur la surface radiculaire, avec vasodilatation, œdème et nécrobiose.
- 5, 9 et 13 heures après : Manifestations similaires. Les cellules épithéliales restantes montrent une faible activité prémitotique.
- 24 heures après : Activité intense des cellules épithéliales dans les zones résiduelles.

- 2 jours après : Le sillon est entièrement recouvert d’épithélium.
- 4 à 5 jours après : Nouvelle attache épithéliale dans la partie profonde du sillon.

- 1 à 2 semaines : Guérison épithéliale complète.
- 6 à 9 semaines : Maturation du tissu conjonctif.
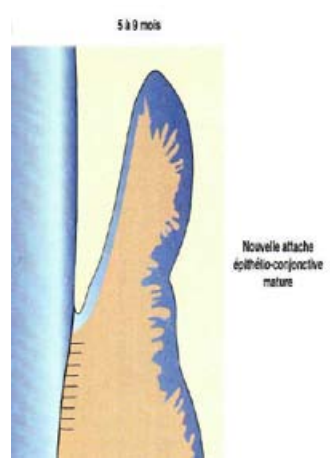
Curetage aveugle et surfaçage radiculaire
- Immédiatement après : Fragments d’épithélium, sang et cellules polynucléaires.
- Dans la journée : Début de la prolifération épithéliale sur les bords, avec recouvrement de la plaie sulculaire par des cellules polynucléaires.
- 7 à 9 jours : Établissement d’un nouveau revêtement du sillon et d’un nouvel épithélium jonctionnel.
- 2 à 3 semaines : Aspect normal de l’épithélium sulculaire et jonctionnel.
- 1 mois : Normalisation de l’attache conjonctive.
Gingivoplastie, gingivectomie
- Après une gingivectomie à biseau externe ou une gingivoplastie, la plaie opératoire est exposée sous le pansement parodontal.
- Le caillot favorise la migration des cellules épithéliales bordant la zone excisée.
- Des fibroblastes du desmodonte interdentaire déclenchent la réparation de l’appareil d’attache conjonctif.
- 14 jours : Cicatrisation superficielle achevée.
Lambeaux
Lambeaux d’épaisseur partielle
- 48 heures : La plaie est pontée par l’épithélium.
- Dès que les macrophages phagocytent le caillot, la fibrogénèse commence.
- Le conjonctif néoformé croît à partir des berges.
- Activité cellulaire et vasculaire au niveau du périoste.
- Cicatrisation de l’attache épithéliale en 4 étapes :
- Stade 1 (12 à 48h) : Migration de 2 à 3 couches de cellules épithéliales sur la fibrine près de la surface radiculaire.
- Stade 2 (5 jours) : Prolifération coronaire de l’attache.
- Stade 3 : Stratification croissante.
- Stade 4 (10 à 14 jours) : Migration apicale des kératinocytes avec formation d’un épithélium jonctionnel long.
- 2 mois : Les fibres collagènes néoformées, initialement verticales, puis parallèles à la surface osseuse, adoptent l’orientation des fibres épargnées.
Lambeaux d’épaisseur totale
- La rapidité de cicatrisation dépend de l’épaisseur du caillot.
- 3 à 4 jours : Début de la résorption du caillot.
- 6 à 7 jours : Remplacement du tissu de granulation par un tissu conjonctif.
- 2 à 3 semaines : Résorption osseuse et apposition tissulaire.
- 3 semaines : Début de la formation osseuse (ostéoblastes).
- 1 mois : Phase de maturation et de réparation.
Lambeaux de Widman modifié
- 48 heures : Séparation de l’épithélium et des fibres gingivales de l’os par un caillot dans un exsudat inflammatoire aigu.
- 1 semaine : Remplacement de l’infiltrat inflammatoire aigu par un infiltrat chronique. La partie coronaire de la plaie est recouverte par un épithélium provenant de l’épithélium sulculaire.
- 3 semaines : Achèvement de l’attachement des fibres conjonctives et de l’épithélium de jonction.
- En cas d’exposition osseuse, nécrose superficielle de l’os alvéolaire dès les deux premières heures.
Greffes
Greffes gingivales pédiculées
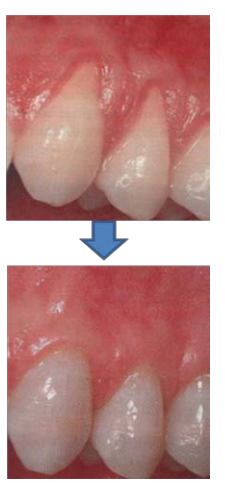
- 4 premiers jours : Fixation du lambeau à la dent et à l’os par un mince caillot fibrineux. Prolifération du tissu conjonctif du lambeau vers le caillot, comblant l’interface avec les structures dures.
- 8 à 10 jours : Poussée épithéliale accentuée vers le bas le long de la surface dentaire.
- 18 à 21 jours : Lambeau fermement attaché à la dent.
- 6 mois : Orientation fonctionnelle évidente des nouvelles fibres conjonctives fixées sur la racine.
Greffes gingivales libres
- Problème principal : Établissement d’une circulation plasmatique adéquate pour nourrir le tissu greffé.
Greffes épithélio-conjonctives

- Cicatrisation du site donneur :
- Cicatrisation par seconde intention.
- Remplacement du caillot sanguin par un tissu de granulation, puis transformation en tissu conjonctif.
- 10 à 15 jours : Plaie complètement recouverte par un nouvel épithélium.
- 4 semaines : Cicatrisation totale.
- Cicatrisation du site receveur :
- Phase initiale (1er à 2ème jour) : Exsudat plasmatique entre le greffon et le site receveur, nourrissant le greffon. Épaisseur minimale du caillot.
- Phase de revascularisation (2ème à 10ème jour) : Rétablissement de la circulation sanguine par connexion des vaisseaux du greffon et du site receveur.
- Phase de maturation tissulaire (11ème à 42ème jour) : Résorption progressive des capillaires néoformés à partir du 14ème jour. Rétablissement de la densité vasculaire. Maturation de l’épithélium avec kératinisation complète à la fin.
Greffes conjonctives enfouies
- Cicatrisation du site donneur : Par première intention.
- Cicatrisation du site receveur : Similaire à la greffe épithélio-conjonctive, sauf pour l’épithélium. La membrane basale est reconstituée, et le nouvel épithélium provient des cellules épithéliales avoisinantes migrant sur cette membrane, formant un tissu intermédiaire entre le donneur et le receveur.
Greffes osseuses et matériaux de substitution osseuse
- Les greffes osseuses participent à la cicatrisation par leur capacité inductrice.
- Les matériaux de comblement servent de remplissage et de mainteneur d’espace cicatriciel.
- Formation d’un long épithélium de jonction entre le produit de la greffe osseuse et la surface radiculaire.
Régénération tissulaire guidée (RTG)
- 6 mois : Formation minimale d’os.
- 6 à 12 mois : Cicatrisation incluant l’os alvéolaire, selon certains auteurs.
- 3 mois : Présence d’os, de cément cellulaire, et de desmodonte avec fibres d’attache bien orientées.
Ostéoplastie/ostéoectomie
- Ostéoplastie : Perte au niveau de l’attache conjonctive. Exposition de l’os suivie d’un remodelage physiologique pouvant entraîner une perte de 1 mm d’os (Moghaddas et Stahl, 1980).
- Ostéoectomie : Similaire à l’ostéoplastie. Le niveau de la nouvelle attache conjonctive est au mieux au niveau initial (fond de la poche), mais souvent une perte d’attache conjonctive survient par résorption postopératoire.
Mise en place implantaire
- Stabilité mécanique : Plus la stabilité est élevée, plus le tissu osseux subit de nécrose.
- Contact os-implant : Plus il est important, plus il y a de nécrose des canaux vasculaires et de tissu osseux.
- Mise en charge des implants : Dépend de l’occlusion :
- Occlusion sans force excessive : Mise en charge immédiate possible.
- Occlusion avec forces excessives : Risque de fibro-ostéointégration.
- Occlusion adaptée passivement : Mise en charge immédiate possible.
- Processus de cicatrisation :
- Os cortical :
- Saignement par compression lors de la pose de l’implant, collapsus des vaisseaux sanguins.
- Nécrose, résorption, puis néoformation osseuse.
- Assure la stabilité primaire de l’implant.
- Os médullaire :
- Saignement sans collapsus osseux.
- Reformation osseuse dès le premier jour.
- Os cortical :
Vestibuloplastie
- Cicatrisation par seconde intention en deux étapes :
- Remplissage de la plaie par un tissu de granulation proliférant à partir des bords.
- Recouvrement par l’épithélium migrant des berges.
- Résultat : Gencive néoformée à texture lisse, similaire à la muqueuse alvéolaire. L’attache au périoste, indirectement à l’os, est fonctionnellement semblable à la gencive attachée.
- Fenestration : Retard de cicatrisation formant une bande fibreuse (limite entre la nouvelle gencive attachée et la muqueuse alvéolaire).
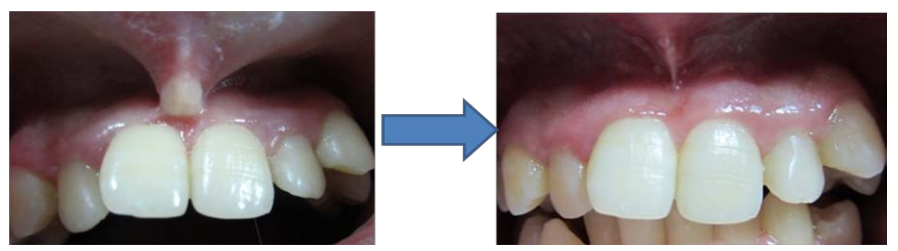
Frénotomie, frénectomie
- Cicatrisation rapide par première intention : Au fond du vestibule.
- Fenestration au niveau du triangle d’insertion du frein : Cicatrisation par seconde intention.
- Phase de réparation : Retardée par une détersion importante, durée dépendante de la profondeur de la plaie.
- Épithélialisation : Complète en une semaine.
Facteurs influençant la cicatrisation
Facteurs favorisants
Facteurs locaux
- Motivation à l’hygiène buccodentaire pour éviter les surinfections postopératoires.
- Élimination parfaite des éléments nécrotiques et dégénérés.
- Caillot sanguin le plus réduit possible.
- Immobilisation de la plaie pendant la cicatrisation.
- Suture bien coaptée.
- Chlorhexidine à 0,1 % : Excellent adjuvant pour la cicatrisation de la muqueuse buccale.
Facteurs généraux
- Facteurs hormonaux : La progestérone augmente la vasodilatation du tissu de granulation.
- Antibiotiques : Protègent la cicatrisation contre les microorganismes.
Facteurs retardant
Facteurs locaux
- Plaque bactérienne.
- Caillot sanguin épais.
- Suture mal coaptée.
- Trauma occlusal.
- Fautes thérapeutiques : Manipulations excessives.
- Pansement chirurgical : Excès ou pression sévère sur les tissus.
- Tabac.
- Irradiation (diminution de l’irrigation sanguine).
Facteurs généraux
- Âge : Pouvoir cicatriciel diminue avec l’âge.
- Race : Cicatrisation plus rapide chez les personnes à peau richement vascularisée (ex. : noirs).
- Troubles métaboliques (ex. : diabète).
- Malnutrition alimentaire.
- Médicaments immunodépresseurs.
- Stress.
- Troubles hématologiques.
Conclusion
La cicatrisation des plaies est un événement cellulaire et moléculaire très complexe, dont le résultat final est une architecture cicatricielle de tissu pouvant partiellement ressembler au tissu d’origine. Le clinicien doit connaître les mécanismes de cicatrisation de tous les tissus, en particulier ceux du parodonte, avant d’entreprendre une thérapie.
Cicatrisation parodontale / Parodontologie
La santé bucco-dentaire est essentielle pour le bien-être général, nécessitant une formation rigoureuse et continue des dentistes. Les étudiants en médecine dentaire doivent maîtriser l’anatomie dentaire et les techniques de diagnostic pour exceller. Les praticiens doivent adopter les nouvelles technologies, comme la radiographie numérique, pour améliorer la précision des soins. La prévention, via l’éducation à l’hygiène buccale, reste la pierre angulaire de la pratique dentaire moderne. Les étudiants doivent se familiariser avec la gestion des urgences dentaires, comme les abcès ou les fractures dentaires. La collaboration interdisciplinaire avec d’autres professionnels de santé optimise la prise en charge des patients complexes. La santé bucco-dentaire est essentielle pour le bien-être général, nécessitant une formation rigoureuse et continue des dentistes.


Leave a Reply