Biochimie de la Salive : Composition, Fonctions et Rôle en Parodontologie
Résumé rapide : La salive est bien plus qu’un simple liquide buccal. Composée à 99 % d’eau mais enrichie de centaines de protéines, d’enzymes, d’immunoglobulines et d’électrolytes, elle joue un rôle central dans la protection des tissus parodontaux, la reminéralisation dentaire et même le diagnostic de maladies systémiques. Ce guide vous propose une synthèse complète, indispensable pour vos révisions et votre pratique clinique.
1. Définition et Origines de la Salive
La salive est la première sécrétion digestive. C’est un liquide physiologique incolore, alcalin et légèrement visqueux, sécrété par les glandes salivaires majeures et mineures (Ganong, 2005).
Ces glandes déversent dans la cavité buccale une salive spécifique, comprenant trois types distincts : la salive parotidienne, la salive sous-maxillaire et la salive sublinguale.
L’ensemble de ces salives, mélangé au mucus buccal et aux produits de sécrétion des glandes de la muqueuse buccale, forme la salive totale ou salive mixte. C’est cette salive mixte que l’on retrouve in vivo dans la bouche du patient.
Point clé pour l’examen : On distingue la salive primaire (produite dans les acini, isotonique) de la salive définitive (modifiée dans les canaux striés, hypotonique).
2. Composition Biochimique de la Salive
La sécrétion salivaire se compose de constituants inorganiques (anioniques et cationiques) et de constituants organiques, qui confèrent à la salive ses nombreuses propriétés biologiques.
2.1 Eau
L’eau représente 99 % de la salive. Elle joue un rôle clé dans :
- L’humidification du bol alimentaire
- La solubilisation des substances pour la détection des goûts
- L’influence sur le pH du flux salivaire, qui varie de 5,3 (faible débit) à 7,8 (débit de pointe)
2.2 Constituants inorganiques
Gaz dissous
Les gaz dissous dans la salive incluent principalement :
- Le dioxyde de carbone (CO₂) : 20 à 30 % du volume salivaire basal
- L’azote (N₂) : 0,9 %
- Le dioxygène (O₂) : environ 0,2 % (Liebaut, 2011)
Éléments minéraux
Les constituants inorganiques comprennent les ions H⁺, Na⁺, K⁺, Ca²⁺, Cl⁻, PO₄³⁻, HCO₃⁻, SCN⁻, les halogènes (iode, fluor) et les métaux traces (cuivre, fer). Ces composants sont issus d’un transport actif depuis le plasma.
Concentrations comparées plasma / salive mixte :
| Ion | Plasma (mmol/L) | Salive non stimulée (mmol/L) | Salive stimulée (mmol/L) |
|---|---|---|---|
| Na⁺ | 143,3 | 1,5 | 20–80 |
| K⁺ | 4,1 | 24 | 20 |
| Ca²⁺ | 2,2 | 1–4 | 1–4 |
| Cl⁻ | 100,9 | 22 | 30–100 |
| HCO₃⁻ | 27,5 | 11 | 5–80 |
| PO₄ inorg. | 1,2 | 6 | 4 |
| Mg²⁺ | <0,2 | 0,2 | 0,2 |
| SCN⁻ | 0,05 | 2,5 | 2 |
| NH₃⁺ | — | 2–7 | 6–3 |
(Na⁺ : ion sodium ; K⁺ : ion potassium ; Ca²⁺ : ion calcium ; Cl⁻ : chlorure ; HCO₃⁻ : bicarbonate)
Ions sodium, Potassium et Chlorure (Na⁺, K⁺, Cl⁻)
Le retrait de ces ions rend la salive hypotonique, facilitant la discrimination des saveurs salées (Proctor et coll., 2014).
Bicarbonate (HCO₃⁻)
Les ions bicarbonate sont essentiels pour le pouvoir tampon salivaire, prévenant la déminéralisation dentaire. Ils facilitent également la solubilité des macromolécules et modifient les propriétés d’écoulement des mucines (Proctor et coll., 2014).
Rappel clinique : Le pouvoir tampon est directement corrélé au débit salivaire. Un patient en hyposialie (débit réduit) présente un pouvoir tampon affaibli et donc un risque carieux augmenté.
Thiocyanate (SCN⁻), Iode et Nitrates
Le thiocyanate exerce une action antibactérienne en association avec les enzymes peroxydases, tout comme l’iode et les nitrates. Les nitrates salivaires influencent probablement la pression sanguine, car 25 % des nitrates circulants sont filtrés par les glandes salivaires.
Ions Calcium et Phosphates (Ca²⁺, PO₄³⁻)
Ces ions jouent un rôle central dans les mécanismes pH-dépendants de dissolution et de reminéralisation de l’hydroxyapatite. Le calcium influence également l’agencement et la réticulation des mucines (Proctor et coll., 2014).
2.3 Constituants organiques
Les substances organiques représentent 0,30 à 0,34 % de la salive, les protéines étant le principal composant (Pellat, 2010). Environ 2,5 g de protéines sont présents par litre de salive, avec plus de 3000 protéines identifiées (Kaczor-Urbanowicz et coll., 2017).
On distingue deux catégories :
Protéines extrinsèques
Plus de 2000 composants issus du sang par diffusion ou transport actif, incluant des hormones (cortisol, testostérone, déhydroépiandrostérone, mélatonine) et des molécules immunologiques (immunoglobuline A, protéine C-réactive) (Bosch, 2014).
Protéines intrinsèques
Environ 400 composants synthétisés localement par les glandes salivaires :
Enzymes salivaires
- Alpha-amylase salivaire (ptyaline) : Sécrétée à 70 % par les glandes parotides, elle hydrolyse les liaisons glucidiques des amidons, produisant maltose, glucose, maltotriose et dextrines (Pellat, 2010).
- Lipase salivaire : Synthétisée principalement par les glandes sublinguales de Von Ebner, elle hydrolyse triglycérides, phospholipides, esters de cholestérol et autres esters (Devoize et coll., 2010).
- Lysozyme : Représentant 10 % des protéines totales, il possède une activité antiseptique (muramidase) contre les bactéries Gram-positif et les champignons, bien que son efficacité en milieu oral soit encore débattue (Pellat, 2010).
- Peroxydases salivaires : Actives contre bactéries, virus et levures. Elles oxydent le thiocyanate pour produire du peroxyde d’hydrogène. On distingue la lactoperoxydase (LPO-SH) et la myéloperoxydase (MPO, 30–75 % des peroxydases) (Devoize et coll., 2010).
- Autres enzymes : Collagénases, gélatinases, élastases, protéases, cholinestérases et ribonucléases, aux rôles antimicrobiens et digestifs.
Protéines riches en proline (PRP)
Ces protéines représentent près des deux tiers des protéines de la salive submandibulaire et 70 % de la salive parotidienne. On distingue :
- Les PRP acides : participent à la formation de la pellicule exogène acquise, maintiennent l’homéostasie du calcium, servent de récepteurs à certaines bactéries
- Les PRP basiques glycosylées : rôle potentiel de lubrifiant (Devoize et coll., 2010)
Mucines
Glycoprotéines ramifiées (75 % protéines, 25 % glucides), représentant 16 % des protéines totales de la salive mixte, principalement sécrétées par les glandes sublinguales. Deux types :
- MG1 (Glycoprotéines muqueuses 1) : Haut poids moléculaire (>1 MDa), fortement glycosylées, elles forment les films recouvrant l’émail et les surfaces épithéliales (Pellat, 2010).
- MG2 (Glycoprotéines muqueuses 2) : Bas poids moléculaire (200–250 kDa), solubles, elles piègent les micro-organismes via leurs adhésines, facilitant leur élimination par déglutition.
Les mucines polymérisent en milieu aqueux, formant un gel visqueux lubrifiant et protecteur. Leur production augmente avec les stimulations gustatives et masticatoires.
Lactoferrines
Protéines de transport du fer, produites par les neutrophiles des glandes salivaires. Leur clivage libère la lactoferricine, aux propriétés bactériostatiques, bactéricides, virucides, fongicides, anti-inflammatoires et antitumorales (Pellat, 2010 ; Devoize et coll., 2010).
Histatines
Petites protéines (3–5 kDa) riches en histidine, sécrétées par les glandes parotidienne et submandibulaire. Elles ont une activité antifongique (candidacide), participent à la pellicule exogène acquise et stimulent la cicatrisation buccale (Pellat, 2010).
Stathérines
Phosphoprotéines (5 kDa) riches en tyrosine, sécrétées par les glandes parotides et submandibulaires. Elles inhibent la précipitation des phosphates de calcium, empêchant les accrétions minérales et les calculs salivaires, tout en contribuant à la lubrification et à la pellicule exogène acquise (Pellat, 2010).
Cystatines
Sécrétées par les glandes salivaires, elles inhibent les protéases à cystéine bactériennes, protégeant les muqueuses et participant à la pellicule exogène acquise (Devoize et coll., 2010 ; Pellat, 2010).
Défensines
Peptides antimicrobiens (3–5 kDa) :
- Alpha-défensines : produites par les leucocytes du fluide gingival
- Béta-défensines : synthétisées par les cellules épithéliales et les glandes salivaires, actives contre bactéries, champignons et certains virus (Pellat, 2010)
Immunoglobulines sécrétoires
Principalement l’immunoglobuline A (IgA), produite par le tissu lymphoïde associé aux muqueuses (MALT), notamment les glandes salivaires. Très glycosylée, elle résiste à la dégradation protéolytique et neutralise les micro-organismes sans provoquer de réponse immunitaire inflammatoire (Van’t Hof et coll., 2014).
Facteurs de croissance
Incluent le facteur de croissance nerveux (NGF) et le facteur de croissance épithéliale (EGF), associés à certaines maladies parodontales. Leur origine est probablement sanguine, avec une possible synthèse locale dans la glande submandibulaire.
Autres composantes organiques
- Urée : environ 2 mmol/L, utilisée pour synthétiser de l’ammoniac, augmentant le pH
- Glucose : 0,056 mmol/L
- ARN : plus de 3000 types différents
- Cytokines : TNF, IL-2, 4, 6, 10, IFN-γ, TGF-β
- Hormones : androgènes, insuline, hormones thyroïdiennes sécrétées par la glande submandibulaire (Pellat, 2010 ; Streckfus et coll., 2002)
3. Caractéristiques Physico-chimiques de la Salive
3.1 Débit salivaire
Le débit salivaire varie de 500 à 1200 ml par 24 heures, avec 70 % d’origine parotidienne et 20 % submandibulaire.
- Sécrétion de repos : environ 100 ml/jour
- Sécrétion stimulée : environ dix fois supérieure (0,1–0,5 ml/min, moyenne de 0,3 ml/min)
Clinique : Une sécrétion de repos inférieure à 0,1 ml/min définit la xérostomie pathologique. Elle est fréquente sous irradiation cervico-faciale, sous antidépresseurs, antihistaminiques et diurétiques.
3.2 Viscosité
La viscosité dépend de la proportion de mucines produites par les cellules muqueuses par rapport aux cellules séreuses.
| Glande salivaire | Viscosité (centipoise) | Consistance |
|---|---|---|
| Parotide | 1,5 | Aqueuse |
| Submandibulaire | 3,4 | Filante |
| Sublinguale | 13,4 | Très visqueuse |
(Szpirglas et Ben Slama, 1999)
3.3 pH salivaire
Le pH varie de 5,3 à 7,8, avec une moyenne de 6 à 7 au repos. Il est influencé par :
- L’apport en ions H⁺
- Le débit salivaire
- L’âge du patient
- Les pathologies associées (diabète, insuffisance rénale)
- Le pouvoir tampon salivaire
4. Mécanisme de Formation de la Salive
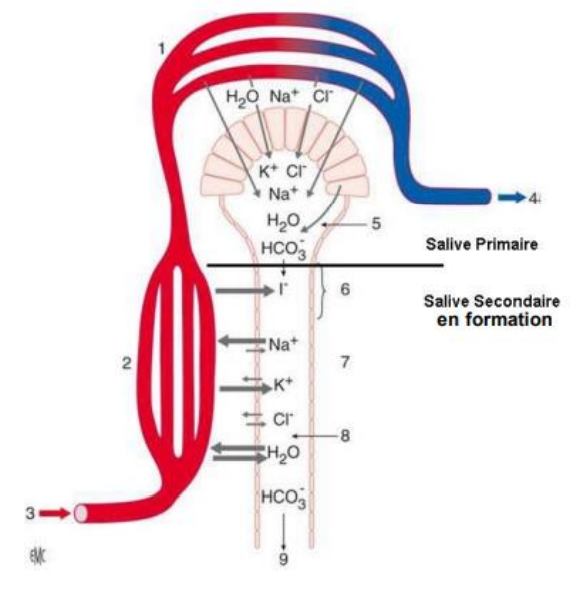
Production de la salive primaire
La salive primaire est formée dans les cellules acineuses. Sa composition est proche du plasma (isotonique). Elle résulte de gradients osmotiques et de mouvements ioniques (Na⁺, K⁺, Cl⁻) via des canaux ioniques et des aquaporines.
Modification en salive définitive
Dans les canaux striés, les ions Na⁺ et Cl⁻ sont réabsorbés, tandis que K⁺ et HCO₃⁻ sont sécrétés, rendant la salive hypotonique (salive secondaire). Ces mécanismes dépendent du débit salivaire, certains systèmes étant saturables à haut débit.
Retenez : Plus le débit est élevé, moins le temps de transit dans les canaux est long, et donc moins la modification est complète → la salive stimulée est donc plus riche en sodium et en bicarbonate que la salive de repos.
5. Commande de la Sécrétion Salivaire
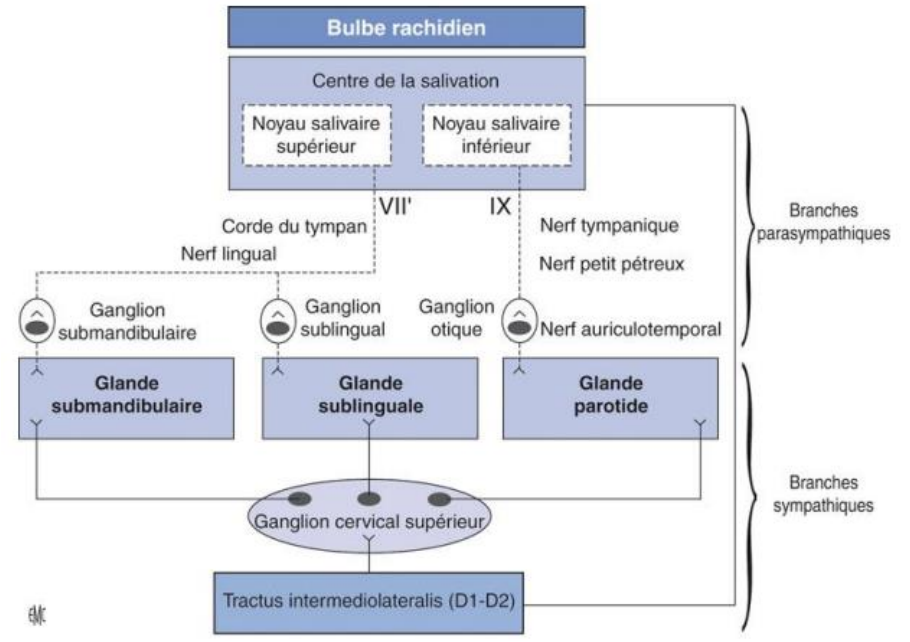
Centre de la salivation
Les centres salivaires (supérieur et inférieur) sont situés dans les noyaux gris centraux du tronc cérébral.
Afférences
Les centres reçoivent deux types d’informations :
Informations descendantes issues du cortex cérébral :
- Inhibitrices : stress, émotions violentes
- Stimulatrices : goût, vision d’aliments appétissants
Informations périphériques provenant de la région bucco-pharyngienne et de l’œsophage, via des mécanorécepteurs (mastication) ou des chémorécepteurs, véhiculées par les nerfs crâniens V (trijumeau), IX (glosso-pharyngien) et XII (grand hypoglosse).
Efférences
Voie parasympathique
- Noyau salivaire supérieur : Les axones empruntent le nerf VII (facial), libérant de l’acétylcholine au niveau des ganglions sous-maxillaires → augmentation de l’activité sécrétoire des glandes submandibulaires et sublinguales.
- Noyau salivaire inférieur : Les axones empruntent le nerf IX (glosso-pharyngien), projetant vers le ganglion otique → stimulation des glandes parotides.
Voie sympathique
Les neurones préganglionnaires, issus du centre sympathique médullaire cervical, libèrent de l’acétylcholine. Les neurones postganglionnaires projettent vers les glandes salivaires, libérant noradrénaline et dopamine → augmentation de la sécrétion de mucus mais inhibition de la sécrétion globale via vasoconstriction.
Retenir pour l’examen : Le parasympathique = salive fluide et abondante. Le sympathique = salive épaisse, visqueuse et réduite (d’où la bouche sèche lors du stress).
6. Physiologie Salivaire : Les Quatre Grandes Fonctions
La salive remplit quatre fonctions principales : digestive, protectrice, excrétrice et endocrinienne.
6.1 Fonction digestive
La salive facilite la formation et la déglutition du bol alimentaire grâce aux mucines lubrifiantes. Elle participe à la gustation en solubilisant les substances sapides pour leur fixation sur les récepteurs gustatifs.
Elle assure également la digestion chimique via :
- L’amylase (parotides et submandibulaires) → hydrolyse des glucides complexes
- Les protéases et lipases (glandes linguales séreuses) → pré-digestion des lipides et protéines
6.2 Fonction protectrice
Protection muqueuse : Les mucines, résistantes à la dégradation, protègent contre le dessèchement, les substances toxiques et les enzymes bactériennes, tout en lubrifiant pour la déglutition et la phonation.
Action antibactérienne : Assurée principalement par les peroxydases, les défensines, les histatines et le lysozyme.
Cicatrisation : Renforcée par l’EGF salivaire — ce qui explique la rapidité de cicatrisation des plaies buccales comparées aux plaies cutanées.
Protection dentaire :
- Inhibition de la déminéralisation grâce aux ions phosphates et bicarbonates (maintien de la neutralité du pH)
- Renforcement de l’émail par diffusion de calcium, phosphates et fluor
- Nettoyage mécanique des surfaces par le flux salivaire, amplifié par les mouvements des lèvres et de la langue
Lien clinique : Pour renforcer la protection des gencives au quotidien, l’utilisation d’un dentifrice adapté comme le Parodontax à l’acide hyaluronique peut compléter l’action naturelle des composants salivaires protecteurs.
6.3 Fonction excrétrice
La salive secrète de 0,6 à 1,5 L d’eau par jour, contribuant à l’hydratation globale. Elle assure aussi l’excrétion de substances (iode, graisses, hormones, anticorps) selon leur concentration plasmatique et le débit salivaire. L’excrétion salivaire est notable pour certains médicaments, comme les antibiotiques.
6.4 Fonction endocrinienne
Les glandes salivaires, principalement les glandes submandibulaires, contiennent et sécrètent des hormones : NGF, EGF, insuline, kallicréine, rénine. Leur origine est probablement sanguine, avec une possible synthèse locale pour les stéroïdes, l’insuline et la parotine.
7. La Salive comme Marqueur Biologique : Un Outil Diagnostique d’Avenir
Grâce à sa composition riche en électrolytes et en protéines, la salive pourrait remplacer les prises de sang pour certains diagnostics. Le protéome salivaire, avec 1166 protéines identifiées, est impliqué dans les voies de signalisation activées lors d’infections ou de lésions.
Les analyses salivaires sont déjà utilisées pour détecter :
- Les stupéfiants (tests de dépistage routier)
- L’ADN (analyses médico-légales)
- Le cortisol (biomarqueur de stress)
- Les cancers buccaux (via biomarqueurs spécifiques)
- L’infection par le VIH (via anticorps spécifiques, sans contamination sauf en cas de plaie buccale)
À l’avenir, la salive pourrait permettre de diagnostiquer des cancers et des maladies cardiovasculaires, offrant ainsi un outil non invasif, économique et adapté aux dépistages à grande échelle ou à la médecine humanitaire.
Perspective clinique : La sialométrie (mesure du débit salivaire) est déjà utilisée en consultation pour évaluer le risque carieux et parodontal. Elle peut être intégrée au bilan initial de tout patient.
Pour approfondir ce sujet passionnant et les applications cliniques en parodontologie, le Guide clinique d’odontologie est une référence incontournable.
8. Tableau Comparatif : Quelle Glande Salivaire Produit Quoi ?
Pour bien comprendre la répartition des fonctions selon les glandes, voici un récapitulatif synthétique.
| Critère | Parotide | Submandibulaire | Sublinguale |
|---|---|---|---|
| Type de sécrétion | Séreuse | Mixte (séro-muqueuse) | Muqueuse |
| Part du débit total | 70 % | 20 % | 5–10 % |
| Viscosité | Aqueuse (1,5 cp) | Filante (3,4 cp) | Très visqueuse (13,4 cp) |
| Richesse en amylase | Très élevée (70 %) | Modérée | Faible |
| Richesse en mucines | Faible | Modérée | Élevée |
| PRP produits | Oui (70 % des PRP) | Oui (67 % des protéines) | Non |
| Lipase | Non | Non | Oui (Von Ebner) |
| Histatines / Stathérines | Oui | Oui | Non |
| Innervation principale | Nerf IX → ganglion otique | Nerf VII → ganglion sous-maxillaire | Nerf VII → ganglion sous-maxillaire |
| Localisation du canal | Canal de Sténon | Canal de Wharton | Canaux de Rivinus |
9. Erreurs Fréquentes à Éviter en Biochimie Salivaire
Erreur 1 — Confondre salive primaire et salive définitive
Problème : Beaucoup d’étudiants croient que la salive produite dans les acini est directement celle retrouvée dans la bouche. Cette confusion entraîne des erreurs sur les concentrations ioniques et le caractère isotonique ou hypotonique de la salive.
Bonne pratique : Retenez que la salive primaire (acinaire) est isotonique au plasma. Elle devient hypotonique après modification dans les canaux striés (réabsorption de Na⁺ et Cl⁻, sécrétion de K⁺ et HCO₃⁻). Ce n’est qu’à ce stade qu’elle acquiert ses propriétés tampons definitives.
Erreur 2 — Négliger le rôle du débit salivaire sur la composition ionique
Problème : Ignorer que la composition de la salive varie selon le débit conduit à des erreurs d’interprétation clinique. Un examinateur peut poser une question sur la composition en bicarbonate de la salive stimulée vs. non stimulée.
Bonne pratique : À débit élevé, les canaux sont moins efficaces pour modifier la salive primaire → la salive stimulée contient donc plus de sodium et de bicarbonate que la salive de repos. Le pH est plus élevé, le pouvoir tampon est renforcé.
Erreur 3 — Attribuer uniquement un rôle digestif à l’amylase salivaire
Problème : L’amylase est souvent réduite à sa seule fonction digestive dans les révisions, ce qui passe à côté de son rôle de biomarqueur et de ses interactions avec le microbiome oral.
Bonne pratique : L’amylase participe également à la formation de la pellicule exogène acquise et influence l’adhésion de certaines bactéries à la surface de l’émail. En clinique, son dosage salivaire peut être élevé en cas de stress ou de pathologies des glandes salivaires.
Erreur 4 — Confondre les fonctions des MG1 et MG2
Problème : Les deux sous-types de mucines ont des rôles distincts et complémentaires. Les confondre peut fausser la compréhension des mécanismes de protection muqueuse et de l’élimination bactérienne.
Bonne pratique : Les MG1 (haut PM) forment des films protecteurs sur l’émail et les épithéliums. Les MG2 (bas PM) piègent les bactéries via leurs adhésines pour faciliter leur déglutition et leur élimination. Ces deux fonctions sont complémentaires, pas interchangeables.
Erreur 5 — Sous-estimer l’importance clinique de la xérostomie
Problème : Considérer la bouche sèche comme un simple inconfort fonctionnel, alors qu’elle est un facteur de risque majeur de caries, de parodontite et de candidose orale.
Bonne pratique : En présence d’une xérostomie, évaluez systématiquement le pouvoir tampon et le débit salivaire. Conseillez au patient un brossage minutieux et l’utilisation d’un dentifrice remineralisant comme le Biomed Calcimax 97 % naturel, qui compense en partie la perte de la protection naturelle assurée par la salive. Dans les cas sévères, renvoyez vers un spécialiste.
Erreur 6 — Ignorer le potentiel diagnostique de la salive
Problème : Beaucoup d’étudiants abordent la biochimie salivaire comme un sujet purement fondamental, sans lien avec la pratique clinique future.
Bonne pratique : La salive est un outil diagnostique émergent. Intégrez dès maintenant la notion de salivodiagnostic dans votre réflexion clinique : biomarqueurs de stress, dépistage du VIH, biomarqueurs du cancer buccal. C’est un axe de recherche en pleine expansion.
10. Cas Cliniques Commentés
Cas clinique n°1 — Patient sous antidépresseurs avec caries cervicales multiples
Présentation : Homme, 47 ans, traité depuis 18 mois par paroxétine (antidépresseur ISRS) pour épisode dépressif majeur. Consultation pour douleurs dentaires multiples. Bilan révèle 6 caries cervicales actives et une gingivite généralisée.
Problématique identifiée : Les antidépresseurs ISRS sont connus pour leur effet xérostomiant (hyposialie médicamenteuse). La réduction du débit salivaire entraîne une diminution du pouvoir tampon (moins de bicarbonate), une baisse de l’action antimicrobienne (lysozyme, IgA, peroxydases) et une perte de l’effet de lavage mécanique. Résultat : environnement favorable à la prolifération de Streptococcus mutans et au développement de caries cervicales.
Prise en charge :
- Information du patient sur le lien médicament-xérostomie-risque carieux
- Prescription d’un dentifrice fluoré et remineralisant
- Recommandation d’un brossage après chaque repas avec une brosse à dents électrique Oral-B Pro 3 à capteur de pression pour éviter les traumatismes cervicaux
- Hydratation orale régulière et substituts salivaires si nécessaire
- Réévaluation à 3 mois
Évolution attendue : Stabilisation des lésions sous contrôle de plaque rigoureux. Si l’hyposialie persiste, adaptation du traitement médical à envisager avec le médecin traitant.
Cas clinique n°2 — Adolescente avec candidose orale récidivante
Présentation : Fille, 16 ans, traitée par corticothérapie inhalée pour asthme persistant modéré. Consultation pour brûlures et taches blanchâtres de la langue et du palais mou, récidivant plusieurs fois par an.
Problématique identifiée : La corticothérapie inhalée non rincée après utilisation favorise la colonisation par Candida albicans dans une cavité buccale dont les défenses naturelles sont localement abaissées. La réduction de l’activité des histatines (antifongiques naturels) et des défensines salivaires dans ce contexte facilite la prolifération fongique.
Prise en charge :
- Éducation à rincer la bouche et se gargariser à l’eau immédiatement après chaque inhalation de corticoïde
- Prescription d’un antifongique local (miconazole gel buccal) pour l’épisode en cours
- Vérification de la technique de brossage et conseil d’un bain de bouche adapté tel que le Listerine Total Care 0 % alcool pour maintenir l’hygiène sans agresser les muqueuses
- Suivi rapproché
Évolution attendue : Résolution des lésions sous traitement et prévention de la récidive par la modification du comportement post-inhalation. Le contrôle de l’activité antifongique naturelle de la salive est rétabli dès lors que le microenvironnement n’est plus altéré.
Cas clinique n°3 — Patient en cours de radiothérapie cervico-faciale
Présentation : Homme, 62 ans, suivi pour carcinome épidermoïde de l’oropharynx, en cours de radiothérapie externe (dose cumulée 50 Gy au moment de la consultation). Se plaint d’une sécheresse buccale sévère, de difficultés à déglutir et d’une douleur à la mastication.
Problématique identifiée : La radiothérapie cervico-faciale provoque une sialadenite radique avec destruction progressive du parenchyme glandulaire, principalement au niveau des glandes parotides. Le résultat est une hyposialie irréversible si les doses atteignent ou dépassent 40 Gy sur les glandes parotides. Toutes les fonctions protectrices de la salive sont donc compromises : lubrification, tamponnage, antimicrobien.
Prise en charge :
- Bilan pré-radiothérapique dentaire systématique (extractions préventives des dents non conservables)
- Substituts salivaires à base de carboxyméthylcellulose ou de mucine
- Fluorothérapie intensive locale (gouttières fluorées)
- Conseil d’irrigation buccale quotidienne avec un hydropulseur Waterpik WF-660EU à pression modérée pour maintenir l’hygiène interdentaire sans traumatiser les muqueuses fragilisées
- Suivi mensuel en cabinet
Évolution attendue : La xérostomie post-radique est souvent définitive. L’objectif est la prévention des caries radio-induites et la préservation des muqueuses pour maintenir la qualité de vie.
11. Foire Aux Questions (FAQ)
Pourquoi la salive est-elle dite hypotonique alors qu’elle est produite à partir du plasma qui est isotonique ?
La salive primaire, produite dans les acini, est effectivement proche de la composition du plasma (isotonique). Mais lors de son passage dans les canaux striés, les cellules canalaires réabsorbent activement Na⁺ et Cl⁻ et sécrètent K⁺ et HCO₃⁻. Comme l’épithélium canalaire est peu perméable à l’eau, cette modification ionique n’est pas compensée osmotiquement : la salive devient donc hypotonique.
Quel est le rôle exact du bicarbonate dans la protection dentaire ?
Les ions bicarbonate (HCO₃⁻) constituent le principal système tampon salivaire. Ils neutralisent les acides produits par le métabolisme bactérien (notamment l’acide lactique produit par Streptococcus mutans), maintenant le pH buccal au-dessus du seuil critique de dissolution de l’émail (pH 5,5). Un débit salivaire réduit = moins de bicarbonate = pH plus acide = risque carieux accru.
Quelle est la différence entre la salive de repos et la salive stimulée ?
La salive de repos (non stimulée) présente un débit faible (0,1–0,3 ml/min), est plus riche en protéines, plus visqueuse et a un pouvoir tampon limité. La salive stimulée, produite lors de la mastication ou de stimulations gustatives, a un débit bien supérieur (jusqu’à 0,5–1 ml/min), est plus riche en bicarbonate et en sodium, a un pH plus élevé et un meilleur pouvoir tampon. Elle joue donc un rôle protecteur accru pendant les repas.
Pourquoi les plaies buccales cicatrisent-elles plus vite que les plaies cutanées ?
Plusieurs facteurs salivaires expliquent cette cicatrisation accélérée. D’une part, l’EGF (Epidermal Growth Factor) salivaire stimule la prolifération cellulaire épithéliale et la migration des kératinocytes sur la plaie. D’autre part, le milieu humide maintenu par la salive est optimal pour la cicatrisation. Enfin, les propriétés antimicrobiennes de la salive (IgA, lysozyme, défensines) réduisent le risque d’infection locale.
Comment la salive peut-elle être utilisée pour le diagnostic médical ?
La salive contient des biomarqueurs spécifiques de nombreuses pathologies : le cortisol comme marqueur de stress, des anticorps anti-VIH détectables dès la primo-infection, des marqueurs de cancer buccal (cytokines, ADN tumoral circulant), et des biomarqueurs de maladies cardiovasculaires. Son principal avantage est d’être un prélèvement non invasif, indolore et peu coûteux, ce qui en fait un outil de dépistage de masse très prometteur pour la médecine du futur.
Qu’est-ce que la pellicule exogène acquise et comment la salive participe-t-elle à sa formation ?
La pellicule exogène acquise (PEA) est un film protéique acellulaire qui se dépose sur l’émail en quelques minutes après le brossage. Elle est constituée principalement de protéines salivaires : les stathérines, les cystatines, les PRP acides, les histatines et certaines mucines. Elle joue un double rôle : elle protège l’émail contre la dissolution acide ET sert de matrice d’adhésion aux premières bactéries colonisatrices, initiant ainsi la formation du biofilm (plaque dentaire).
Quelles glandes salivaires sont les plus touchées par la radiothérapie cervico-faciale et pourquoi ?
Les glandes parotides sont les plus radiosensibles car elles sont composées majoritairement de cellules acineuses séreuses, plus vulnérables aux radiations ionisantes que les cellules muqueuses. Dès 25–30 Gy de dose cumulée, une réduction significative du débit parotidien est observée. À partir de 40 Gy, la destruction peut devenir irréversible. Les glandes submandibulaires et sublinguales sont également touchées mais de façon moindre en raison de leur contenu plus riche en cellules muqueuses.
Comment expliquer la sécheresse buccale ressentie lors d’un stress intense ?
Lors d’un stress, la stimulation du système nerveux sympathique provoque une libération de noradrénaline et de dopamine au niveau des glandes salivaires. Cela entraîne une vasoconstriction locale (réduction de l’apport sanguin aux glandes) et une augmentation de la sécrétion de mucus épais, tout en réduisant le volume global de salive produite. Résultat : bouche sèche, collante et difficultés à déglutir — une manifestation parfaitement explicable par la biochimie salivaire.
Conclusion : La Salive, un Liquide Biologique Fondamental en Odontologie
La salive résulte du mélange des sécrétions des glandes parotides, submandibulaires, sublinguales et accessoires, excrétées via leurs canaux respectifs. Composée de mucus, d’enzymes (amylase, lysozyme), d’immunoglobulines (IgA), d’eau et d’électrolytes, elle est profondément modifiée par les cellules canalaires.
En tant que futur(e) chirurgien-dentiste, comprendre la biochimie salivaire vous permettra de :
- Mieux expliquer les mécanismes carioprotecteurs et parodontoprotecteurs à vos patients
- Identifier rapidement les situations cliniques d’hyposialie et adapter la prise en charge
- Anticiper les complications buccales liées aux médicaments sialopéniques
- Intégrer les données émergentes du salivodiagnostic dans votre pratique
Pour approfondir votre formation, les ouvrages de référence comme les Annales corrigées de l’internat en odontologie 2022-2024 ou le Référentiel internat en parodontologie constituent des outils précieux pour consolider vos connaissances et préparer sereinement vos examens.
ResiDentaire™ | Plateforme de QCM Médecine Dentaire ResiDentaire
https://residentaire.com/
Références bibliographiques
- Bosch JA (2014). Saliva as a source of biomarkers. Frontiers in Psychology.
- Devoize L, Dallel R (2010). Salivation. EMC Médecine buccale, 28-150-M-10.
- Ganong WF (2005). Review of Medical Physiology, 22nd ed.
- Kaczor-Urbanowicz KE et coll. (2017). Salivary biomarkers of systemic disease. Experimental Biology and Medicine.
- Liebaut C (2011). Physiologie salivaire et applications cliniques.
- Pellat B (2010). Salives et milieu buccal. EMC Médecine buccale, 28-150-H-10.
- Proctor GB et coll. (2014). Salivary secretion : Mechanisms and neural regulation. Monographs in Oral Science.
- Szpirglas H, Ben Slama L (1999). Pathologie de la muqueuse buccale.
- Van’t Hof W et coll. (2014). Antimicrobial peptides : Properties and applicability. Biological Chemistry.
Cette page contient des liens d’affiliation Amazon. En cliquant dessus, vous n’êtes pas tenu de vous procurer les produits suggérés, mais si vous le faites, cela ne vous coûte rien de plus et cela m’aide à financer ce site.



[…] maladies héréditaires du collagène ou collagénopathies regroupent les maladies par mutation d’un des gènes codant […]