Anesthésiques Locaux – Anesthésiologie Dentaire
Introduction
Définition : Les anesthésiques locaux (AL) entraînent une perte de sensibilité au niveau du lieu d’administration.Mécanisme : Ils bloquent de façon réversible la transmission nerveuse.Utilisation : Largement utilisés en odontologie, anesthésiologie et dans de nombreuses spécialités médicales et chirurgicales.Indications principales : Prévention de la sensation de douleur.
Indications
Anesthésie locale ou régionale.
Actes chirurgicaux.
Gestion des douleurs aiguës ou chroniques.
Utilisation thérapeutique ou diagnostique.
Remarque : L’anesthésie locorégionale comporte des risques et des accidents.
Historique
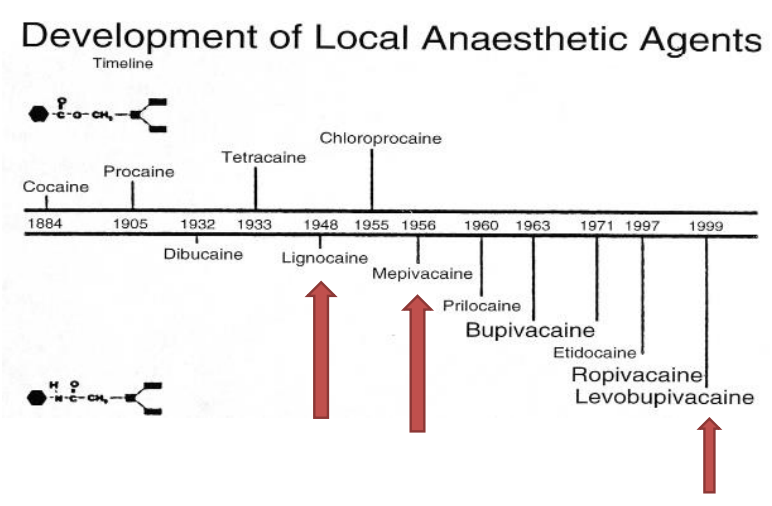
Développement des anesthésiques locaux
Timeline du développement des agents anesthésiques locaux.
Physiologie
Principe : L’anesthésie locale entraîne une perte de sensibilité par interruption de la conduction nerveuse.Mécanisme : La conduction de l’influx nerveux est liée aux modifications du gradient électrique via les canaux sodiques.Effet des AL : Inhibition réversible de la conduction nerveuse sans altération du nerf.Types de fibres affectées : Fibres sensitives, motrices et végétatives.Ordre de disparition des sensations :
Sensation douloureuse.
Sensation thermique.
Sensation tactile.
Classification des fibres nerveuses
Type de fibre Myélinisation Diamètre (µm) Vitesse de conduction (m/s) Fonction Aα ++ 10-25 60-100 Fibres motrices et proprioceptrices Aβ, Aγ ++ 4-12 20-100 Fibres sensitives et proprioceptrices Aδ + 1-6 3-25 Douleur, température, toucher B + <3 3-15 SNA préganglionaire C 0 0,3-2 0,2-2,5 SNA postganglionaire, douleur, température, toucher
Propriétés physicochimiques
Mécanisme d’action primaire : Blocage des canaux sodiques voltage et temps dépendant.Propriétés essentielles :
Solubilité lipidique.
Fixation aux protéines.
Degré d’ionisation.
Solubilité lipidique
Les fibres nerveuses sont composées à 70 % de lipides.
Une grande liposolubilité favorise une diffusion importante.
Mesurée par le coefficient de partage huile/eau.
Fixation aux protéines
Conditionne la durée d’action des AL.
Une forte fixation protéique entraîne une durée d’action prolongée.
Degré d’ionisation
Influence la capacité de l’AL à traverser les membranes.
Mécanisme d’action
Action principale : Blocage des canaux sodiques voltage et temps dépendant.Impact : Stabilisation des membranes nerveuses par inhibition des flux sodiques entrants.
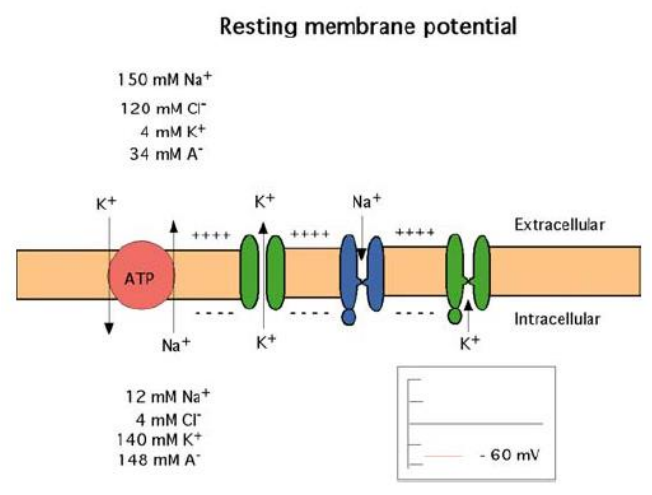
Potentiel de membrane au repos
Maintien de l’équilibre électrique de la membrane nerveuse.
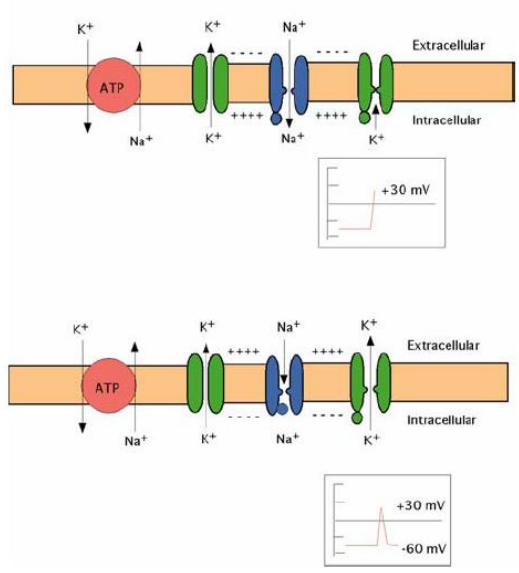
Potentiel d’action
Modifications électriques permettant la conduction nerveuse, bloquées par les AL.
Classification des anesthésiques locaux
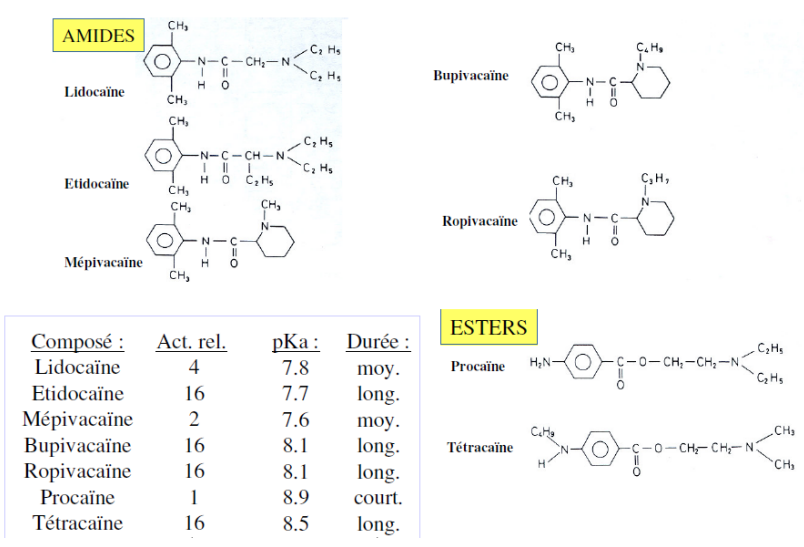
Structure moléculaire : Tous les AL possèdent une molécule composée de trois parties :
Cycle aromatique (acide benzoïque ou para-amino-benzoïque) : pôle lipophile, rôle dans la diffusion et la fixation.Pôle hydrophile : Dérivé amine tertiaire (rarement secondaire) de l’alcool éthylique ou de l’acide acétique.Chaîne intermédiaire : Influence la liposolubilité, l’hydrosolubilité, la puissance et la toxicité.
Types de liaisons
Liaison ester :
Instable, dégradation rapide par hydrolyse enzymatique.
Liaison amide :
Plus stable, dégradation hépatique plus lente, durée d’action prolongée.
Pharmacologie
Structure commune : Tous les AL partagent une structure moléculaire similaire et un mode d’action comparable.Différences entre molécules :
Puissance.
Délai d’action.
Durée d’action.
Toxicité.
Bloc anesthésique
Délai d’action :
Dépend de la fraction libre disponible pour traverser la fibre nerveuse.
AL à faible pKa (lidocaïne, mépivacaïne) : 50 % non ionisés, diffusion rapide.
AL à pKa élevé (tétracaïne, bupivacaïne) : Plus ionisés, diffusion plus lente.
Puissance et durée d’action :
Déterminées par le degré d’hydrophobie et le poids moléculaire.
Solubilité lipidique élevée (bupivacaïne, étidocaïne) : Puissance et durée d’action supérieures.
Solubilité faible (procaïne, chloroprocaïne) : Puissance et durée d’action réduites.
Tableau des propriétés pharmacologiques
Agent pKa % Ionisé (Plasma, pH 7,40) % Ionisé (Tissu, pH 7,10) Procaïne 8,9 97 99 Chloroprocaïne 8,7 95 98 Tétracaïne 8,5 93 96 Lidocaïne 7,9 76 86 Prilocaïne 7,9 76 86 Mépivacaïne 7,6 61 76 Bupivacaïne 8,1 83 91 Étidocaïne 7,7 66 80 Ropivacaïne 8,1 83 91
Comparaison des anesthésiques locaux
Agent Poids moléculaire pKa Coefficient de partage Fixation protéique Délai d’action Durée d’action Puissance Esters Procaïne 236 8,9 0,02 6 % Long 1h-1h30 0,5 Chloroprocaïne 271 8,7 0,14 ? Court 1h 1 Tétracaïne 264 8,5 4,1 80 % Long 3-4h 4 Amides Lidocaïne 234 7,9 2,9 65 % Court 1h30-2h 1 Prilocaïne 220 7,9 0,9 55 % Court 1h30-2h 1 Mépivacaïne 246 7,6 0,8 75 % Court 2-3h 1 Bupivacaïne 288 8,1 27,5 95 % Intermédiaire 3h-3h30 4 Étidocaïne 276 7,7 141 95 % Court 3h-4h 4 Ropivacaïne 274 8,1 6,1 94 % Intermédiaire 2h30-3h 3,3
Autre tableau comparatif
Agent Poids moléculaire pKa Coefficient de partage Liaison protéique Délai d’installation relatif Puissance relative Durée d’action relative Amino-esters Procaïne 272 8,9 0,6 5,80 % 1 1 1 Chloroprocaïne 271 8,7 – – – – – Tétracaïne 301 8,5 80 75 % 2 16 8 Articaine 321 7,8 40 95 % 0,8 6 2 Amides Lidocaïne 271 7,9 2,9 64 % 0,8 4 1,5 Mépivacaïne 283 7,6 0,8 78 % 1 2 1,5 Bupivacaïne 325 8,1 27,5 95 % 0,6 16 vinosine 8 Prilocaïne 257 7,9 0,8 55 % 1 3 1,5 Étidocaïne 313 7,7 141 94 % 0,4 16 8 Ropivacaïne 274 8,1 6,1 94 % 1 8 8
Durée d’action
Varie de 30 à 180 minutes selon les agents.
L’adjonction d’adrénaline prolonge l’effet de l’AL.
Indications détaillées
Applications : Endoscopies, chirurgies, soins dentaires.Types d’anesthésie locale :
Infiltration : Injection dans la zone concernée.Conduction : Ciblage des nerfs et du territoire innervé.Spinale et péridurale : Anesthésie au niveau de la colonne vertébrale.
Métabolisme
Esters :
Hydrolysés dans le plasma, les globules rouges et le foie par des pseudocholinestérases.
Amides :
Métabolisés exclusivement par le foie via le cytochrome P450.
Contre-indications absolues
Hypersensibilité aux anesthésiques locaux.
Porphyrie.
Anémie hémolytique.
Troubles de la conduction cardiaque.
Hypertension artérielle sévère.
Épilepsie non contrôlée.
Formes biopharmaceutiques en odontostomatologie
Transmuqueuse : Anesthésie de surface ou de contact.Sous-muqueuse : Anesthésie par infiltration via injection parentérale.
Voie transmuqueuse
Application : Topique.Formes :
Solides imprégnés d’AL (coton, disque de papier).
Formes colloïdales (gels, pâtes).
Formes gazeuses (spray).
Voie sous-muqueuse
Objectif : Insensibilisation d’un territoire limité (une ou plusieurs dents).Conditionnements :
Flacon : 10 à 50 ml, utilisé en milieu hospitalier.Cartouche : 1,7 à 1,8 ml, forme biopharmaceutique de choix.
Conservateurs : Parabens, sulfites, éthylène-diamine-tétra-acétate (EDTA).
Indications principales des molécules
Molécule Indications principales Articaine Anesthésie locale ou locorégionale en odontostomatologie Lévobupivacaïne Anesthésies locale et de conduction (chirurgies des membres inférieurs, urologique, gynécologique, abdominale sous-ombilicale, césarienne) Mépivacaïne Anesthésie locale d’infiltration et régionale (blocs plexiques et tronculaires, anesthésie péridurale et caudale) Lidocaïne Anesthésies locale et péridurale Prilocaïne Anesthésie locale de la peau saine Procaïne Anesthésie locale d’infiltration et de conduction (blocs plexiques et tronculaires) Ropivacaïne Anesthésies locale et péridurale Tétracaïne Kératite pour forme collyre, anesthésie locorégionale
Lidocaïne (Xylocaïne®)
Caractéristiques
Anesthésique local de type aminoamide.
Stabilisation des membranes nerveuses par blocage des flux sodiques entrants.
Indications
Anesthésies locales ou locorégionales.
Anesthésies locales par infiltration.
Contre-indications absolues
Allergie aux aminoamides.
Porphyrie.
Troubles de conduction intracardiaque.
Épilepsie non contrôlée.
Antécédent d’hyperthermie maligne.
Contre-indications liées aux formes adrénalinées
Insuffisance coronarienne.
Troubles du rythme ventriculaire.
Injection intraveineuse.
Hypertension artérielle sévère.
Cardiomyopathie obstructive.
Hyperthyroïdie.
Injection au niveau des extrémités.
Traitement par IMAO ou antidépresseurs tricycliques.
Posologie et mode d’administration
Concentrations : 0,5 % (5 mg/ml), 1 % (10 mg/ml), 2 % (20 mg/ml).
Effets secondaires
Cardiovasculaires : Hypotension, bradycardie, troubles du rythme, fibrillation ventriculaire.Respiratoires : Dépression respiratoire, apnée.Neurologiques : Bourdonnements d’oreille, dysphorie, surdité, convulsions.Allergiques : Risque faible.
Surdosage
Convulsions généralisées, arrêt cardiorespiratoire.
Articaine
Caractéristiques
Chlorhydrate d’articaine, AL à fonction amide.
Souvent associé à l’adrénaline pour :
Ralentir le passage dans la circulation générale.
Maintenir une concentration tissulaire active prolongée.
Réduire les saignements au champ opératoire.
Cinétique
Installation de l’anesthésie : 2 à 3 minutes.
Durée de l’anesthésie : Environ 60 minutes (2 à 3 fois plus courte pour une anesthésie pulpaire).
Formulations
Ubistestin 4 %, Ultracaïn 4 %.
Bupivacaïne (Marcaïne®)
Indications
Anesthésies locales ou locorégionales.
Blocs centraux et périphériques.
Infiltrations locales.
Posologie et mode d’administration
Concentrations : 0,25 % (2,5 mg/ml), 0,5 % (5 mg/ml).
Effets secondaires
Cardiovasculaires : Hypotension, bradycardie, troubles du rythme, fibrillation ventriculaire, arrêt cardiaque.Respiratoires : Dépression respiratoire, apnée.Neurologiques : Bourdonnements d’oreille, dysphorie, surdité, convulsions.Allergiques : Risque faible.
Surdosage
Convulsions généralisées, arrêt cardiorespiratoire, troubles du rythme.
Mépivacaïne (Carbocaïne®)
Caractéristiques
Anesthésique local de type aminoamide.
Stabilisation des membranes nerveuses par blocage des flux sodiques entrants.
Indications
Anesthésies locales ou locorégionales.
Blocs centraux et périphériques.
Infiltrations locales.
Contre-indications absolues
Allergie aux aminoamides.
Porphyrie.
Troubles de conduction intracardiaque.
Épilepsie non contrôlée.
Antécédent d’hyperthermie maligne.
Injection intravasculaire.
Nourrisson de moins de 1 mois.
Contre-indications relatives
Femme enceinte (fœtotoxicité observée chez l’animal).
Pas d’AMM en France pour les rachianesthésies.
Posologie et mode d’administration
Concentrations : 1 % (10 mg/ml), 2 % (20 mg/ml).
Effets secondaires
Cardiovasculaires : Hypotension, bradycardie, troubles du rythme, fibrillation ventriculaire.Respiratoires : Dépression respiratoire, apnée.Neurologiques : Bourdonnements d’oreille, dysphorie, surdité, convulsions.Allergiques : Risque faible.
Surdosage
Convulsions généralisées, arrêt cardiorespiratoire.
Autres anesthésiques
Doses maximales recommandées
Anesthésique Dose maximale Articaine 4 % + Adrénaline 7 mg/kg (500 mg) adulte, 5 mg/kg enfant Bupivacaïne 0,5 % + Adrénaline 2 mg/kg (90 mg) Lidocaïne 2 % + Adrénaline 7 mg/kg (500 mg) Mépivacaïne 2 % + Lévonordéfrine 6,6 mg/kg (400 mg) Mépivacaïne 3 % sans vasoconstricteur 6,6 mg/kg (400 mg) Prilocaïne 4 % avec/sans adrénaline 8 mg/kg (500 mg)
Concentrations et contenu des cartouches
Concentration (%) mg/mL mg dans une cartouche de 1,8 mL 2 % 20 36 mg 3 % 30 54 mg 4 % 40 72 mg
Exemple de calcul pour un enfant de 15 kg
Anesthésique Dose maximale Concentration Volume maximal Nombre maximal de cartouches (1,8 mL) Lidocaïne 105 mg 20 mg/mL 5,25 mL 2,9 Prilocaïne 120 mg 40 mg/mL 3 mL 1,67 Mépivacaïne 99 mg 30 mg/mL 3,3 mL 1,8 Articaine 75 mg 40 mg/mL 1,88 mL 1
Tableau des doses maximales
Anesthésique local Dose maximale Quantité maximale de cartouches Lidocaïne 7 mg/kg (500 mg) 13 Mépivacaïne 6,6 mg/kg (500 mg) 11 Prilocaïne 8 mg/kg (500 mg) 7 Bupivacaïne 2 mg/kg (200 mg) 8 Articaine 7 mg/kg (500 mg), 5 mg/kg enfant 10 (7 enfant)
Spécificités en chirurgie dentaire
Risques :
Passage intravasculaire possible.
Surdosage si grande quantité nécessaire.
Proximité du système nerveux central (SNC).
Vascularisation importante du site.
Adjonction d’adrénaline.
Complications de l’anesthésie locorégionale (ALR)
Risque d’intoxication grave : Tous les AL peuvent provoquer des intoxications sévères.Mécanismes :
Passage massif dans la circulation par injection directe (survenue précoce).
Résorption d’une quantité importante.
Toxicité relative (par ordre croissant) : Lidocaïne = Mépivacaïne < Ropivacaïne < Lévobupivacaïne << Bupivacaïne.
Causes du surdosage
Terrain du patient : Insuffisance hépatique.Âge et poids : Enfants de 2 à 6 ans (15 à 40 kg).Nature de l’AL : Concentration, dose, présence de vasoconstricteurs.Quantité administrée .État inflammatoire : Vasodilatation et résorption rapide.Injection intravasculaire : Absence de test d’aspiration.
Toxicité
Facteurs influençant la toxicité :
Type d’agent : Lidocaïne, procaïne, mépivacaïne et ropivacaïne moins toxiques que bupivacaïne.
Vitesse d’injection.
Adjonction d’adrénaline : Ralentit la résorption, réduisant la toxicité.
Nombre maximal de cartouches selon le poids
Poids (kg) Lidocaïne 2 % Mépivacaïne 2 % Mépivacaïne 3 % Articaine 4 % 10 1,9 1,8 1,2 1 20 3,8 3,6 2,4 1,9 30 5,8 5,5 3,6 2,9 40 7,7 7,3 4,8 3,8 50 9,7 9,1 6,1 4,8 60 11,6 11 7,3 5,8 65 12,6 11,1 7,4 6,3 70 13,8 11,1 7,4 6,8 ≥80 13,8 11,1 7,4 6,9
Toxicité locale
Vasodilatation.
Toxicité neurologique.
Toxicité musculaire.
Toxicité systémique
Toxicité neurologique
Signes précoces :
Paresthésies linguales et péribuccales.
Lipothymies, acouphènes, vision trouble.
Agitation, nervosité, paranoïa.
Troubles de l’élocution, troubles de la conscience.
Convulsions, dépression respiratoire.
Toxicité cardiaque
Formes :
Toxicté neurologique via le système sympathique.
Toxicité directe.
Manifestations :
Troubles de la conduction (bloc auriculo-ventriculaire).
Troubles du rythme graves, asystolie.
Dépression myocardique, vasodilatation périphérique, hypotension, collapsus.
Arrêt cardiocirculatoire.
Allergie
Rareté : Allergie aux AL exceptionnelle.Cause fréquente : Conservateurs (ex. : méthylparaben).Terrain allergique : N’est pas une contre-indication absolue.
Traitement des complications
Mesures initiales
Évaluer la conscience et la ventilation.
Libérer les voies aéro-digestives supérieures.
Allonger le patient et surélever les pieds.
Contacter les secours.
Prise en charge médicale
Oxygénation.
Intubation trachéale et ventilation assistée si nécessaire.
Administration de benzodiazépine ou thiopental pour convulsions.
Perfusion d’intralipide (20 %, 100-200 ml sur 2 min, répétée si nécessaire).
Atropine en cas de bradycardie.
Adrénaline et réanimation cardiopulmonaire en cas d’arrêt.
Précautions d’emploi
Surveillance de base
Respecter les doses maximales.
Éviter l’injection dans une zone infectée.
Respecter les règles d’asepsie pour les formes injectables.
Injection lente avec test d’aspiration.
Respecter le site d’injection.
Utiliser la forme galénique adaptée.
Mesures complémentaires
Disposer d’un matériel d’anesthésie-réanimation (monitoring de la pression artérielle, ECG).
Avoir des médicaments appropriés (anticonvulsivants, atropine, myorelaxants).
Conclusion
Efficacité : Les AL constituent un arsenal analgésique varié et efficace.Risques : Nécessité de connaître les complications potentielles.Bonnes pratiques : Une maîtrise de la pharmacologie et des règles cliniques est essentielle pour une utilisation sécurisée.
Anesthésiques Locaux – Anesthésiologie Dentaire
Voici une sélection de livres:
Anesthésiques Locaux – Anesthésiologie Dentaire



Leave a Reply