La Cicatrisation Parodontale : Guide Complet pour Étudiants en Médecine Dentaire
Introduction
La cicatrisation parodontale représente l’un des processus biologiques les plus complexes et fascinants de la médecine dentaire. Contrairement à d’autres tissus corporels, le parodonte doit cicatriser dans un environnement hostile, constamment exposé aux agressions bactériennes et aux forces mécaniques.
Comme tous les organes du corps humain, le parodonte répond aux agressions d’origine traumatique, bactérienne, virale ou chirurgicale par l’initiation de mécanismes de défense. En cas de destruction tissulaire, il déclenche des processus de cicatrisation visant à préserver la survie de l’organe concerné.
Ces événements se déroulent de manière spécifique et prévisible, sous-tendus par de grands principes biologiques qu’il est essentiel de maîtriser pour tout praticien.
La particularité du parodonte ? Il cicatrise dans un système ouvert, contaminé en permanence et soumis à une charge bactérienne considérable. Cette réalité explique pourquoi les résultats de la guérison sont si variables lors de chaque traitement des poches parodontales.
Le clinicien se doit donc de connaître parfaitement les mécanismes de cicatrisation avant d’entreprendre toute thérapeutique. C’est l’objectif de ce guide complet.
I. Généralités sur le Parodonte
Anatomie et Composition du Parodonte
Le parodonte sain fournit le soutien nécessaire pour maintenir les dents en fonction. Il constitue une unité fonctionnelle complexe composée de quatre éléments principaux qui travaillent en synergie.
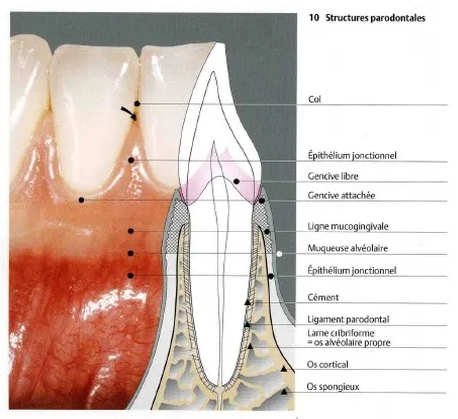
Les quatre composants du parodonte :
- La gencive : tissu muqueux protecteur
- Le ligament parodontal (desmodonte) : structure de suspension
- Le cément : tissu minéralisé recouvrant la racine
- L’os alvéolaire : structure de soutien osseux
Chacun de ces composants parodontaux possède une localisation, une architecture et une composition biochimique distinctes. Néanmoins, ils fonctionnent ensemble comme une seule unité intégrée.
Rôles Fondamentaux du Parodonte
Le parodonte assure plusieurs fonctions vitales :
Fonction mécanique : Insertion de la dent dans l’alvéole et résistance aux forces générées par la mastication, la déglutition et la phonation.
Fonction adaptative : Adaptation continue aux changements structurels associés aux stimuli et au vieillissement par remodelage et régénération permanents.
Fonction protectrice : Défense contre les influences nocives du milieu buccal.
La recherche scientifique a révélé que les composants de la matrice extracellulaire d’un compartiment parodontal peuvent influencer les activités cellulaires des structures adjacentes.
Par conséquent, les changements pathologiques qui surviennent dans un des composants du parodonte peuvent avoir des conséquences importantes pour la maintenance, la réparation ou la régénération des autres composants. Cette interdépendance est cruciale à comprendre.
II. Le Turn-Over Tissulaire : Comprendre le Renouvellement Parodontal
Le temps de renouvellement (turn-over) diffère considérablement d’un tissu parodontal à l’autre. Cette connaissance est essentielle pour anticiper les délais de cicatrisation.
Renouvellement Épithélial
Épithélium jonctionnel (EJ) : 4 à 6 jours
Épithélium oral sulculaire (EOS) : 4 à 10 jours
Épithélium oral gingival (EOG) : 7 à 15 jours
L’épithélium se renouvelle donc très rapidement, ce qui explique sa capacité de réparation accélérée.
Renouvellement du Chorion Gingival
Le renouvellement des fibres collagéniques du chorion gingival est plus rapide que celui de l’os alvéolaire : 10 à 15 jours.
Cette rapidité relative permet une adaptation tissulaire efficace aux agressions mineures.
Renouvellement de l’Os Alvéolaire
Le remaniement de l’os alvéolaire se manifeste dans un os mature par l’apparition d’ostéons ou BMU (Basic Multicellular Unit).
Durée du cycle de remodelage : 4 mois chez l’adulte
La phase de formation est significativement plus longue que celle de résorption. Le processus comprend quatre phases distinctes : activation, résorption, inversion et formation.
Le Périoste
La couche interne du périoste est capable de développer une forte activité ostéogénique au bout de 21 jours. Cette propriété est particulièrement exploitée en chirurgie reconstructrice.
Le Cément
L’apposition du cément secondaire cellulaire est permanente et maintenue tout au long de la vie d’une dent, qu’elle soit pulpée ou dépulpée, malgré l’absence de vascularisation et d’innervation.
Comment est-ce possible ? Grâce aux :
- Prolongements cytoplasmiques orientés vers le desmodonte
- Connexions entre les cémentoblastes par le biais des canalicules
En cas de résorption ou de destruction, une réparation cémentaire est possible. Elle se caractérise par un dépôt de cément cellulaire à fibres intrinsèques, puis de cément acellulaire à fibres extrinsèques. Ce processus prend 6 à 8 semaines.
Le Desmodonte (Ligament Alvéolo-Dentaire)
Le collagène du ligament alvéolo-dentaire (LAD) présente un turn-over remarquablement rapide :
- 5 fois plus rapide que celui de la gencive et de l’os alvéolaire
- 15 fois plus rapide que celui de la peau
Ce phénomène diminue progressivement avec l’âge, expliquant pourquoi la cicatrisation parodontale est généralement plus efficace chez les patients jeunes.
III. Les Mécanismes Fondamentaux de la Cicatrisation
L’Hémostase : Premier Acte de la Cicatrisation
L’hémostase représente l’ensemble des mécanismes physiologiques qui assurent l’obturation de toute rupture du circuit vasculaire et la prévention du saignement spontané.
Elle comporte plusieurs étapes intriquées et interdépendantes :
1. Hémostase primaire : Fermeture de la brèche vasculaire par un « thrombus blanc » (clou plaquettaire)
2. Hémostase secondaire (coagulation plasmatique) : Consolidation de ce premier thrombus en formant un réseau de fibrine emprisonnant des globules rouges (thrombus rouge ou caillot sanguin)
3. Fibrinolyse : Destruction du caillot ou limitation de son extension
Le caillot sanguin joue un rôle fondamental dans la cicatrisation parodontale. Il constitue la matrice provisoire qui guidera la régénération tissulaire.
L’Inflammation : Processus de Nettoyage et de Préparation
L’inflammation est un processus dynamique constitué par un ensemble de réactions vasculaires, cellulaires et hormonales, déclenché par toute agression qu’elle soit d’origine mécanique, chimique, thermique ou infectieuse.
Objectifs de l’inflammation :
- Élimination de l’agent agresseur
- Élimination des débris cellulaires
- Préparation à la réparation des tissus lésés
La réaction inflammatoire comprend quatre phases intriquées dans le temps :
Phase 1 : Phase vasculo-exsudative initiale
- Congestion active des vaisseaux
- Formation d’un œdème (exsudat inflammatoire)
- Migration des leucocytes à partir des veinules post-capillaires jusqu’au lieu de l’inflammation (diapédèse leucocytaire)
Phase 2 : Constitution du granulome inflammatoire
- Organisation du tissu de défense
- Préparation à la détersion
Phase 3 : Phase de détersion
- Élimination des tissus nécrotiques, des germes et des corps étrangers éventuels
- Détersion interne : action phagocytaire des macrophages
- Détersion externe : naturelle (fistulisation) ou artificielle (drainage chirurgical)
Phase 4 : Phase de cicatrisation
- Phase finale de l’inflammation
- Transition vers la réparation tissulaire proprement dite
IV. Terminologie Essentielle en Cicatrisation Parodontale
La compréhension précise de la terminologie est fondamentale pour différencier les différents types de cicatrisation.
La Plaie
Définition : Rupture de la continuité anatomique et fonctionnelle des tissus vivants (Krawczyk, 1978).
Les plaies peuvent trouver leur origine dans :
- Les destructions pathologiques
- Les agressions chimiques, physiques ou thermiques
- Les incisions chirurgicales
La Régénération : L’Idéal Thérapeutique
Définition : Processus biologique par lequel il y a une restauration « ad integrum » des quatre tissus parodontaux avec rétablissement complet de la fonction (Stahl, 1979).
La régénération implique la restauration complète de l’anatomie (l’architecture) et de la fonction des tissus lésés sur une surface radiculaire préalablement exposée à la maladie parodontale.
Caractéristiques de la cicatrisation par régénération :
- Formation d’un court épithélium de jonction
- Nouveau cément
- Nouveau desmodonte
- Nouvel os alvéolaire
- Attache épithéliale insérée au niveau le plus coronaire possible (idéalement au niveau de la jonction émail-cément)
Important : La régénération complète reste l’objectif idéal, mais elle est difficile à obtenir de manière prévisible en pratique clinique.
La Réparation : La Réalité Clinique
Définition : Processus biologique au cours duquel la continuité tissulaire est rétablie par des néoformations. Cependant, ce processus restaure de façon partielle l’architecture et/ou la fonction des tissus lésés.
Caractéristiques de la cicatrisation par réparation :
- Formation d’un long épithélium de jonction
- Restauration de la continuité tissulaire sans régénération complète
- Fonction partiellement restaurée
Dans la majorité des cas cliniques, on obtient une réparation plutôt qu’une régénération véritable.
La Nouvelle Attache
Définition : Nouveau lien d’attache entre le tissu conjonctif et la surface radiculaire auparavant dénudée en raison de la pathologie.
Cela implique une nouvelle formation de cément avec ancrage de fibres desmodontales, caractérisée par la formation d’os avec des fibres de Sharpey distinctes.
La Ré-attache
Définition : Rétablissement du lien entre le tissu conjonctif et les tissus vitaux restants sur la surface radiculaire, comme le cément et des parties du ligament parodontal.
Note importante : Il n’existe pas de ré-attache épithéliale. L’épithélium est constamment renouvelé par les cellules basales.
L’Attache Rampante (Creeping Attachment)
Phénomène inconstant observé dans les mois qui suivent une chirurgie mucogingivale (greffe libre épithélio-conjonctive et lambeaux déplacés d’épaisseur partielle).
Elle correspond à la migration coronaire de la gencive marginale le long d’une racine dentaire présentant une récession et traitée chirurgicalement.
Ce phénomène favorable ne peut être systématiquement prédit mais constitue un bonus thérapeutique apprécié.
Le Pontage Fibreux
Il s’agit d’une liaison du tissu conjonctif avec les fibres de collagène persistant à la surface radiculaire. Cette situation favorable se produit quand elles ont été sectionnées en l’absence de maladie.
C’est une réunion des fibres conjonctives du lambeau avec les terminaisons des fibres de collagène de la surface radiculaire.
L’Adhérence Conjonctive
Les fibres conjonctives sont parallèles à la dent et se situent apicalement à l’épithélium jonctionnel et coronairement à la crête osseuse.
Cette attache peut être associée à un épithélium de jonction court ou long selon les circonstances.
Le Comblement Osseux
Correspond à la restauration clinique du tissu osseux dans une lésion parodontale. Il peut ou non être accompagné d’une régénération parodontale complète.
Attention : Un comblement osseux radiographique ne signifie pas automatiquement qu’il y a eu régénération parodontale complète avec nouveau ligament et nouveau cément.
Ostéogénèse
Se définit comme la croissance d’os à partir de cellules vivantes présentes au sein du greffon.
L’os autogène est le seul matériau capable de véritables propriétés ostéogéniques.
Ostéo-induction
Désigne la capacité d’un biomatériau à entraîner, par des facteurs protéiques qu’il contient (les Bone Morphogenetic Proteins ou BMPs), une néoformation osseuse.
Ostéo-conduction
Processus par lequel le matériau de comblement agit comme un échafaudage (scaffold) rendant possible une colonisation vasculaire secondaire capable de promouvoir une néoformation osseuse.
Remarque clinique importante : La cicatrisation est objectivée cliniquement par la profondeur au sondage et le niveau d’attache. Le gain d’attache clinique reste le critère de succès principal.
V. Définition et Objectifs de la Cicatrisation Parodontale
Définition Complète
La cicatrisation parodontale représente la guérison d’une plaie, caractérisée par la restauration sous forme de réattache ou de nouvelle attache.
Particularité parodontale : La cicatrisation parodontale présente la caractéristique unique d’être constituée par une surface dure (la racine dentaire) et un tissu mou (la gencive), seul capable d’effectuer un mouvement de migration vers la surface dentaire.
La cicatrisation est l’ensemble des événements spécifiques et prévisibles, sous-tendus par des principes biologiques, visant la réparation d’un tissu lésé. Elle réalise sa continuité avec restitution morphologique et fonctionnelle, assurant ainsi la survie du tissu concerné.
Objectifs Thérapeutiques
L’objectif primordial reste la guérison du parodonte et la reconstitution complète des tissus perdus : la régénération « ad integrum ».
Bien que cet objectif idéal ne soit pas encore systématiquement atteint, il est possible d’établir une échelle de succès thérapeutique :
1. Reconstitution complète par régénération
Possible principalement en cas de gingivite simple
2. Guérison des poches parodontales par réparation
Objectif réaliste dans la parodontite
3. Arrêt de la perte d’attache
Critère minimal de succès
4. Élimination de l’inflammation
Condition préalable à toute cicatrisation
Pour obtenir une régénération complète dans le cas de parodontite, une exigence supplémentaire du point de vue biologique et fonctionnel est nécessaire : l’exclusion de l’épithélium et éventuellement du tissu conjonctif gingival à la surface des racines.
C’est le principe fondamental de la Régénération Tissulaire Guidée (RTG).
VI. Classifications de la Cicatrisation Parodontale
Classification de Kramer
Kramer propose une classification complète de la chirurgie parodontale selon plusieurs critères :
Critères de classification :
- En fonction des tissus concernés
- En fonction du type de chirurgie
- En fonction de la chronologie thérapeutique
- En fonction du type de cicatrisation (le plus pertinent pour notre propos)
Selon le Type de Cicatrisation
A. Réattache par réparation
Caractéristiques :
- Épithélium jonctionnel long
- Adhésion épithéliale ou conjonctive
- Pas de néo-cément ni de néo-ligament
- Néoformation osseuse possible
- Sillon gingivo-dentaire (SGD) plus profond que la normale
B. Nouvelle attache par régénération
Caractéristiques :
- Formation d’un épithélium jonctionnel court
- Néo-cément présent
- Néo-ligament formé
- Nouvel os alvéolaire
- Sillon gingivo-dentaire court
Classification de Schroeder (1983)
Schroeder propose une approche tissulaire spécifique.
Au Niveau de l’Épithélium
Régénération épithéliale : Formation d’un néo-attachement complet
Ré-attachement épithélial : Restauration partielle
Au Niveau du Tissu Conjonctif
Régénération du tissu conjonctif : Néo-attachement complet avec fibres fonctionnelles
Ré-attachement du tissu conjonctif : Adhésion sans fibres fonctionnelles complètes
Remarque fondamentale : Il n’existe pas de réattache épithéliale au sens strict. L’épithélium est constamment renouvelé par les cellules basales. On parle donc plutôt de néo-formation épithéliale.
Classification de Bouchard et Étienne (1993)
Cette classification se base sur le mode de fermeture de la plaie.
Cicatrisation par Première Intention
Définition : Plaie fermée, plaie aseptique franche permettant une coaptation des berges de la plaie par sutures.
Avantages :
- Cicatrisation plus rapide
- Moins de complications
- Résultat esthétique supérieur
Cicatrisation par Deuxième Intention
Définition : Plaie ouverte, intervient lorsque les berges de la plaie sont béantes et ne peuvent être rapprochées.
Caractéristiques :
- Cicatrisation plus lente
- Phase de détersion prolongée
- Nécessite formation de tissu de granulation important
VII. Bases Mécaniques de la Cicatrisation
Modèle Cutané : La Référence
La plaie cutanée présente comme caractéristique la présence de deux berges muqueuses ou cutanées qui vont stabiliser le caillot sanguin.
Mécanisme : La cicatrisation aboutit au rapprochement des deux berges pour permettre la fermeture de la plaie. Ce modèle est relativement simple et prévisible.
Modèle Parodontal : La Complexité
La plaie parodontale présente une caractéristique unique : la présence d’une berge muqueuse (épithélium et tissu conjonctif) d’un côté et d’une surface dure (racine dentaire) de l’autre.
Défi mécanique : La cicatrisation dans ce cas de figure aboutit au rapprochement de la seule partie muqueuse vers la surface dentaire.
Cette configuration rend la cicatrisation plus difficile, d’autant plus que la cavité buccale est sous la dépendance de plusieurs facteurs locaux défavorables :
- Présence bactérienne permanente
- Forces occlusales cycliques
- Mouvements de la langue et des joues
- Variations de pH salivaire
Conséquence clinique : La stabilisation de l’interface tissu mou-surface radiculaire est cruciale pour obtenir une cicatrisation optimale.
VIII. Physiologie de la Cicatrisation : Les Trois Phases
La cicatrisation d’une plaie se déroule selon une séquence ordonnée en trois phases principales qui se chevauchent partiellement.
Phase 1 : Phase Exsudative (Détersion de la Plaie)
Chronologie : Débute immédiatement après le traumatisme
Événements immédiats (0-10 minutes) :
Immédiatement après le traumatisme, des sécrétions débutent à partir des vaisseaux sanguins et lymphatiques.
La coagulation est induite par activation de la thrombokinase libérée, conduisant à la formation de fibrine et du caillot sanguin.
Phase exsudative (10 minutes – 3 jours) :
Après environ 10 minutes, débute l’exsudation qui va assurer deux fonctions essentielles :
- La défense contre l’infection
- La détersion de la plaie
L’augmentation de la perméabilité capillaire favorise le passage vers la région traumatisée de :
- Plasma sanguin contenant des anticorps
- Leucocytes polymorphonucléaires
- Macrophages
Résultat : Les tissus nécrosés, les corps étrangers et les microbes sont éliminés et détruits par phagocytose et protéolyse. C’est le “nettoyage” biologique de la plaie.
Phase 2 : Phase Proliférative (Développement du Tissu de Granulation)
Chronologie : 3 à 14 jours
Formation du tissu de granulation :
Le tissu lâche néoformé remplaçant la matrice provisoire (thrombus rouge) est dénommé tissu de granulation.
Rôle central des macrophages :
Les macrophages jouent un rôle essentiel en sécrétant :
- Des facteurs de croissance
- Des cytokines capables de promouvoir l’angiogenèse
- Des facteurs de prolifération fibroblastique
- Des stimulateurs de synthèse du collagène
Évolution cellulaire :
Les fibroblastes envahissent le tissu de granulation et acquièrent un phénotype contractile myofibroblastique. Ces myofibroblastes contribuent activement à la contraction du tissu de granulation, rapprochant les berges de la plaie.
Synthèse matricielle :
On observe :
- Une synthèse précoce du collagène type III et de fibronectine, largement supérieure à la synthèse du collagène type I
- Une synthèse importante mais transitoire d’acide hyaluronique
- Une néo-vascularisation intensive (angiogenèse)
Le tissu de granulation apparaît cliniquement rouge, granuleux et saigne facilement au toucher.
Phase 3 : Phase de Maturation (Remodelage)
Chronologie : 14 jours à plusieurs mois (voire années)
Cette dernière phase peut se dérouler sur plusieurs mois. Elle est caractérisée par le remodelage du tissu conjonctif et la formation d’une cicatrice mature.
Transformations tissulaires :
Le tissu de granulation disparaît progressivement pour laisser place à un tissu conjonctif fibreux mature.
Régression vasculaire :
La plupart des capillaires formés précédemment disparaissent. Seuls les vaisseaux nécessaires à la nutrition tissulaire persistent.
Apoptose cellulaire :
La grande majorité des fibroblastes meurent par apoptose (mort cellulaire programmée), ne laissant qu’une population résiduelle pour l’entretien tissulaire.
Remodelage du collagène :
- Remplacement progressif du collagène type III par du collagène type I
- Organisation des fibres selon les lignes de force
- Augmentation de la résistance mécanique
- Réduction progressive de la vascularisation

Important pour le praticien : Même si la cicatrisation clinique semble complète après 3-4 semaines, le remodelage tissulaire se poursuit pendant plusieurs mois. C’est pourquoi il faut éviter les traumatismes sur les zones récemment cicatrisées.
IX. Modalités Cicatricielles des Différents Tissus Parodontaux
Cicatrisation Épithélio-Conjonctive (Gingivale)
A. Cicatrisation par Première Intention (Plaie Fermée)
La cicatrisation par première intention se réalise en présence d’une incision chirurgicale propre avec possibilité de suturer les berges. Elle présente deux aspects complémentaires.
Réparation Conjonctive
1 à 6 heures post-opératoires :
La matrice intercellulaire s’organise rapidement :
- Dégénérescence des cellules conjonctives superficielles à la plaie
- Migration des polynucléaires neutrophiles (PNN)
- Début de la détersion de la plaie par les macrophages
3 jours post-opératoires :
Apparition des cellules fibroblastiques qui vont synthétiser la nouvelle matrice.
3 à 7 jours :
Formation et évolution du tissu de granulation (bourgeon charnu) :
- Néo-vascularisation intensive
- Prolifération fibroblastique
- Début de ré-épithélialisation
7 jours et au-delà :
Formation d’une matrice de collagène avec remodelage fonctionnel des tissus.
Phénomène de contraction : La cicatrisation des plaies subit une contraction centripète au moment de la formation de la cicatrice. L’intensité de cette contraction est déterminée par le type et la taille des plaies.
Réparation Épithéliale
La réparation épithéliale se caractérise par trois phénomènes simultanés :
1. Différenciation cellulaire : Les cellules épithéliales modifient leur phénotype pour devenir migratoires
2. Prolifération : Augmentation du nombre de cellules par mitose
3. Migration cellulaire : Déplacement des cellules sur la surface de la plaie
Mécanisme détaillé :
Après la phase inflammatoire qui met en route la réparation, les cellules épithéliales situées sur les bords de la zone lésée se superposent les unes sur les autres et commencent à migrer par-dessus la plaie de façon à la couvrir.
Quand elles arrivent au contact du tissu conjonctif, elles se différencient, deviennent sphériques et apparaissent comme des cellules épithéliales basales.
D’autres cellules migrent ensuite et augmentent l’épaisseur de la couche épithéliale.
Maturation finale :
La couche superficielle se kératinise progressivement. La maturation se poursuit jusqu’à reconstitution d’un épithélium mature avec toutes ses couches.
Facteur déterminant : La durée de l’épithélialisation est directement fonction de la surface à recouvrir.
B. Cicatrisation par Seconde Intention (Plaie Ouverte)
Elle intervient après une perte de substance, une plaie due à une ulcération ou une plaie ouverte après la réalisation d’une chirurgie telle que la gingivectomie à biseau externe (GBE), la gingivoplastie, etc.
Elle comprend deux phases distinctes :
Phase 1 : La Détersion Suppurée
La détersion suppurée est le préalable indispensable à la cicatrisation. Elle élimine tous les tissus nécrosés et tout ce qui gêne le bourgeonnement.
Mécanisme :
Elle s’effectue à la limite du tissu mort et vif par clivage enzymatique. Ces enzymes proviennent de deux sources :
- Sources endogènes : Cellules spécialisées (leucocytes, macrophages) apportées par la réaction inflammatoire normale de l’organisme
- Sources exogènes : Bactéries saprophytes de la cavité buccale
Durée : Cette phase peut durer plusieurs jours selon l’importance de la nécrose tissulaire.
Phase 2 : La Fermeture
Pour obtenir la fermeture de la plaie, l’organisme fait appel à de nouveaux tissus appelés tissus de granulation, constitués de :
- Fibroblastes actifs
- Macrophages
- Capillaires néoformés
- Fibres de collagène immatures
Facteurs influençant la durée :
Le temps d’exposition de la plaie intervient significativement dans cette cicatrisation. Plus la plaie sera exposée longtemps, plus :
- Les débris à éliminer seront nombreux
- Le risque de contamination est élevé
- La cicatrisation sera longue
Règle clinique : La réparation sera d’autant plus difficile et longue que la perte de substance sera importante (plaie étendue).
Conclusion : La cicatrisation par deuxième intention est systématiquement plus lente que celle par première intention. Ceci est étroitement lié à la phase de détersion qui est beaucoup plus longue dans le cas des plaies ouvertes.
Cicatrisation Osseuse
La cicatrisation osseuse est un processus complexe et prolongé. Quatre phases principales interviennent dans la cicatrisation de la plaie osseuse.
Phase 1 : Phase de Comblement (Jours 1 à 4)
Chronologie : Du 1er au 4ème jour
Mécanisme :
Débute par une prolifération intensive des capillaires à partir de :
- Le desmodonte
- Le chorion gingival
- Les cavités médullaires ouvertes
Cette néo-vascularisation sera le préalable indispensable à l’organisation d’un tissu conjonctif jeune, riche en fibroblastes, qui subira ensuite des remaniements cicatriciels.
Formation du caillot sanguin :
Le caillot sanguin remplit l’espace et sert de matrice provisoire pour la colonisation cellulaire.
Phase 2 : Phase de Résorption (Jours 4 à 7)
Chronologie : Du 4ème au 7ème jour
Activité ostéoclastique :
Les ostéoclastes multinucléés adhèrent à la surface osseuse et forment des micro-chambres de résorption.
Mécanisme de résorption :
Sous ces micro-chambres :
- La phase minérale est dissoute par acidification locale
- La phase organique est mise à nu
- La matrice organique est dégradée par des enzymes spécifiques (collagénases)
Fonction : Cette phase prépare le terrain pour la formation d’os neuf en éliminant les débris osseux nécrosés et en lissant les surfaces.
Phase 3 : Phase Ostéoblastique (Jours 7 à 28)
Chronologie : Du 7ème au 28ème jour
Cette phase est caractérisée par une activité formatrice intensive.
Au 14ème jour (Formation d’os immature) :
- Formation de l’ostéoïde (matrice osseuse non minéralisée)
- Formation de travées grêles plus ou moins anastomosées
- Substance osseuse comportant des fibres de collagène et des ostéocytes
Au 28ème jour (Os immature en voie de minéralisation) :
L’os néoformé présente les caractéristiques suivantes :
- Très fibrillaire
- Disposé en nodules autour d’un tissu richement vascularisé
- Laisse présager la future structure ostéonique
- C’est un os jeune aux systèmes haversiens en formation
Observation histologique :
On rencontre :
- Des ostéocytes dans leurs lacunes
- De grandes cavités ostéocytaires à intense activité néoformatrice
- Un riche réseau vasculaire
- Le rebord alvéolaire tapissé d’ostéoblastes actifs
Phase 4 : Phase de Maturation (Jours 28 à 126 et au-delà)
Chronologie : Du 28ème au 126ème jour et au-delà
Décroissance de la formation osseuse :
À partir du 28ème jour, on observe une décroissance progressive de la formation osseuse :
- Formation devenue faible au 49ème jour
- Formation inexistante au 77ème jour
Transformation en os définitif (selon Wilderman) :
Du 49ème jour au 6ème mois :
- Transformation de l’os néoformé immature en os définitif mature
- L’os compact prend l’aspect d’un os haversien au 77ème jour (ébauche de corticale)
- Cette phase se poursuit même pendant un an ou plus
| Phase de comblement : | Phase de | Formationd’os immature au 14 ème jour | Os immature | Maturation | |||
| du 1 er au 4 ème jour | résorption : | En voie de | de l’os | ||||
| du 4ème au7ème jour | minéralisationau 28 ème jour | du 28 ème au126 ème | |||||
Remodelage continu :
Le remodelage osseux se poursuit bien au-delà de la cicatrisation clinique apparente. C’est pourquoi il faut respecter des délais suffisants avant toute sollicitation importante (comme la mise en charge d’implants).
À retenir : Bien que la cicatrisation osseuse radiographique puisse sembler complète à 3-4 mois, la maturation complète de l’os néoformé prend 6 à 12 mois.
Cicatrisation du Périoste
Selon Goldman et Smukler (1979), le périoste stimulé développe au bout de 21 jours une importante activité ostéogénique.
Mécanisme :
La couche interne du périoste (couche cambiale) est constituée de cellules au repos (cellules mésenchymateuses indifférenciées) qui peuvent être réactivées en cellules ostéogéniques par un stimulus approprié (traumatisme chirurgical, fracture, inflammation).
Application clinique :
Cette propriété est exploitée dans :
- Les techniques de régénération osseuse guidée
- Les greffes osseuses
- Les techniques de préservation alvéolaire
Importance du périoste :
Le périoste doit être préservé autant que possible lors des interventions chirurgicales car il constitue une source précieuse de cellules ostéoprogénitrices.
Cicatrisation du Desmodonte
Selon Melcher, le desmodonte joue un rôle régulateur crucial : il régularise la croissance en inhibant l’ostéogenèse au niveau de la surface radiculaire.
Principe fondamental :
Au niveau desmodontal, le ré-attachement ne peut avoir lieu qu’en dessous de l’épithélium jonctionnel, sauf si le praticien applique les techniques de :
- RTG (Régénération Tissulaire Guidée)
- ROG (Régénération Osseuse Guidée)
Ces techniques permettent une cicatrisation desmodontale optimale en excluant les tissus à prolifération rapide (épithélium et tissu conjonctif gingival).
Potentiel régénérateur :
Les cellules du ligament parodontal possèdent le potentiel de former :
- Nouveau cément
- Nouveau ligament parodontal
- Nouvel os alvéolaire
C’est pourquoi leur préservation et leur prolifération guidée sont essentielles pour obtenir une véritable régénération parodontale.
Cicatrisation du Cément
Évolution des concepts :
Si les premiers traitements consistaient à éliminer systématiquement le cément lésé de façon à mettre à nu la dentine saine, on préfère aujourd’hui :
- Soit l’exciser partiellement et sélectivement
- Soit lui faire subir une désinfection douce aux ammoniums quaternaires ou au chlorhydrate de tétracycline
Techniques modernes de régénération :
La Régénération Tissulaire Guidée (RTG) permet d’obtenir la formation d’un néo-cément. Cette néoformation peut être optimisée par l’emploi de facteurs de croissance, notamment :
- Les BMP (Bone Morphogenic Proteins ou protéines osseuses morphogéniques)
- Le PDGF (Platelet-Derived Growth Factor)
- Les EMD (Enamel Matrix Derivatives – dérivés de la matrice amélaire)
Particularité :
Il se formera toujours, entre cément ancien et néo-cément, une couche de matériel granulaire accumulé. Cette interface n’affecte généralement pas la fonction de l’attache nouvellement formée.
Temps de formation :
La formation de néo-cément nécessite environ 3 à 6 semaines après l’intervention, à condition que les conditions biologiques soient favorables.
X. Chirurgie Parodontale et Cicatrisation
Cette section détaille les modalités cicatricielles spécifiques à chaque type d’intervention parodontale.
Surfaçage Radiculaire
Immédiatement après le surfaçage :
L’attache épithéliale est rompue, créant une communication directe entre le tissu conjonctif et la surface radiculaire.
Deux heures après :
On peut observer :
- De nombreuses cellules polynucléaires neutrophiles
- Une vasodilatation locale
- De l’œdème
- Des signes de nécrobiose tissulaire
À ce moment, les cellules épithéliales montrent une très faible activité prémitotique (préparation à la division).
24 heures après :
On trouve des cellules épithéliales en intense activité mitotique dans toutes les zones épithéliales résiduelles. La prolifération épithéliale est lancée.
2 jours après :
Le sillon est entièrement recouvert d’épithélium. Cette rapidité de couverture peut être problématique car elle peut empêcher la formation d’une nouvelle attache conjonctive.
4 à 5 jours après :
Une nouvelle attache épithéliale apparaît dans la partie apicale du sillon. La guérison épithéliale complète se produit en une ou deux semaines.
Important : Cependant, le tissu conjonctif n’est mature que 6 à 9 semaines après surfaçage radiculaire.
Implication clinique : C’est pourquoi il faut respecter un délai d’au moins 6 à 8 semaines entre le surfaçage et une éventuelle chirurgie parodontale, pour permettre la maturation conjonctive complète.
Curetage Parodontal à l’Aveugle
Résultat cicatriciel :
Il y aura une réparation des cellules épithéliales et du tissu conjonctif par formation d’un long épithélium de jonction plus apicalement et d’une nouvelle attache conjonctive limitée.
Cicatrisation Épithéliale
Premières 24 heures :
La différenciation cellulaire débute dès les premières 24h.
Jusqu’à 48 heures :
La prolifération dure jusqu’à 48h après la réalisation de la plaie.
3ème au 7ème jour :
Épithélialisation progressive du sillon.
25 jours :
Le processus trouve son aboutissement au bout de 25 jours (cette durée varie selon la surface à recouvrir).
2 semaines après :
Kératinisation définitive des surfaces.
3 semaines :
La cicatrisation épithéliale clinique se termine au bout de 3 semaines.
Cicatrisation Conjonctive
Au fur et à mesure de la régression de l’inflammation :
3 jours : Formation d’un tissu de granulation
4 à 5 jours : Début de synthèse du collagène
14 jours : Une attache conjonctive organisée est en place
3 semaines : Le néo-cément n’apparaît pas avant 3 semaines
Stabilisation tissulaire :
Toutes ces données font apparaître une stabilisation des tissus au bout de 40 jours au minimum.
Règle clinique : Attendre au moins 6 semaines avant toute réévaluation ou nouvelle intervention.
Gingivectomie
Gingivectomie à Biseau Externe (GBE)
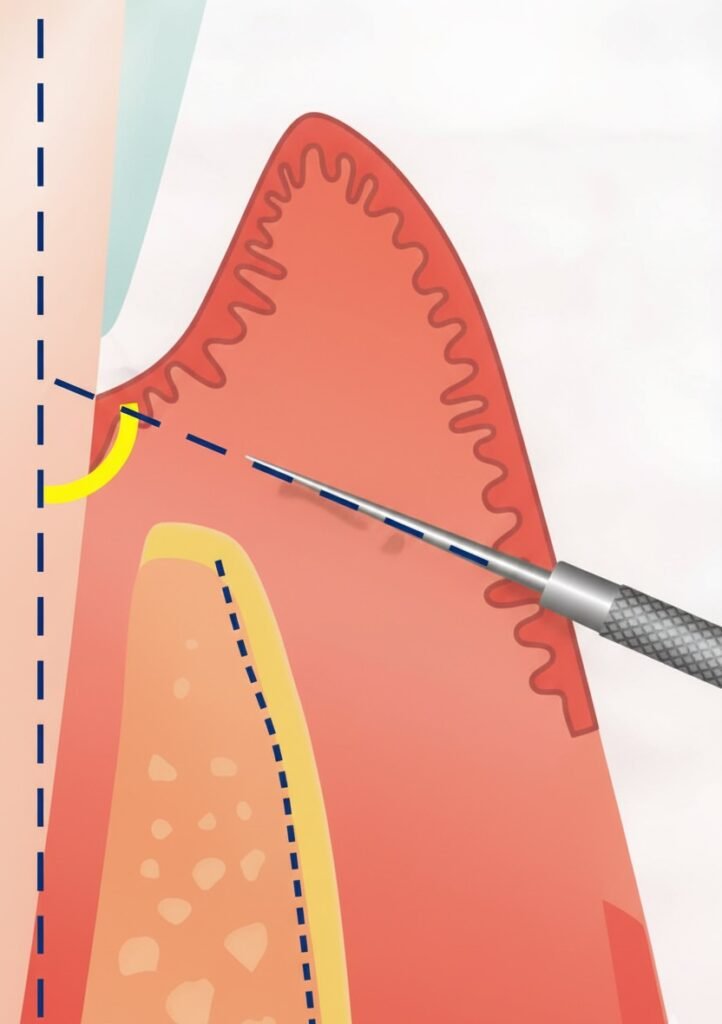
Type de cicatrisation : Cicatrisation de deuxième intention (détersion suppurée puis fermeture).
Chronologie :
9 à 18 heures : L’épithélialisation est plus rapide car les cellules proviennent directement des bords de plaie.
24 à 36 heures : Pic d’activité mitotique pour l’épithélium
3 à 4 jours : Pic d’activité mitotique pour le conjonctif
Deuxième semaine : Le tissu conjonctif prolifère sous l’épithélium en direction apicale
14 jours en moyenne : La kératinisation se fait rapidement
Cicatrisation complète :
- Cicatrisation clinique : après 3 semaines
- Fin de l’épithélialisation : 35 jours
Particularité : La GBE laisse une plaie ouverte qui cicatrise par granulation. Le pansement chirurgical est essentiel pour protéger la plaie et assurer le confort du patient.
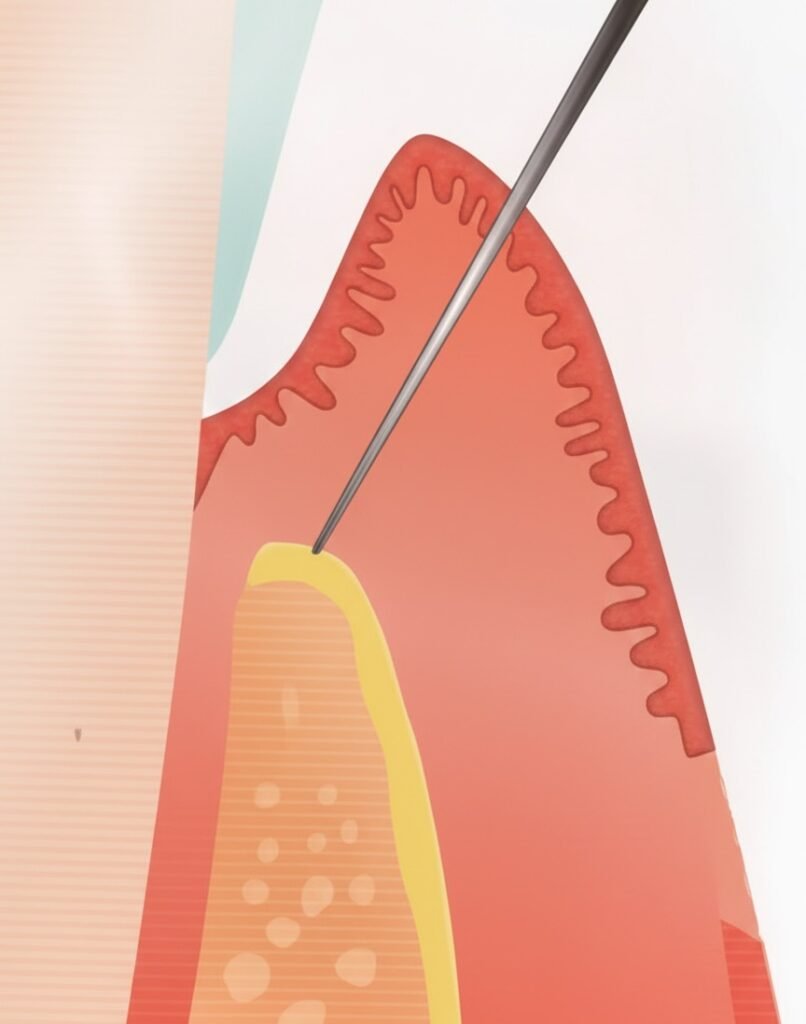
Gingivectomie à Biseau Interne (GBI)
Type de cicatrisation : Cicatrisation de première intention.
Processus :
Les cellules épithéliales vont subir une séquence ordonnée :
- Différenciation
- Prolifération
- Migration
- Maturation et kératinisation
Durée totale : Environ 15 jours
Avantage : Cicatrisation plus rapide et plus confortable pour le patient que la GBE.

Freinectomie et Freinotomie
Au Fond du Vestibule
Type de cicatrisation : Cicatrisation rapide de première intention
Mécanisme : C’est une cicatrisation dite « plaie fermée » où la mise en contact de la muqueuse sur le périoste profond élimine presque complètement la phase de détersion.
Au Niveau du Triangle d’Insertion du Frein
Type de cicatrisation : Cicatrisation de seconde intention
Mécanisme : C’est une cicatrisation dite « plaie ouverte » où la phase de réparation est retardée par une détersion importante.
Durée : La durée est fonction de la superficie et de la profondeur de la plaie.
Épithélialisation : Se fait en environ une semaine.
Approfondissement du Vestibule
Type de cicatrisation : Cicatrisation par seconde intention
Processus en deux étapes :
Étape 1 : Remplissage
Remplissage de la plaie par des tissus de granulation qui prolifèrent à partir des bords de la plaie.
Étape 2 : Recouvrement
Recouvrement de la plaie par l’épithélium qui migre à partir des berges de la plaie.
Résultat à 1 mois :
On obtient une gencive néoformée ayant un aspect particulier :
- Texture lisse
- Absence du piqueté
- Vascularisation apparente identique à la muqueuse alvéolaire
Résultat à 2 mois :
L’attache formée au périoste et indirectement à l’os sous-jacent la rend fonctionnellement semblable à la gencive attachée.
Stabilité : Cette nouvelle gencive attachée est stable dans le temps si l’hygiène bucco-dentaire est correcte.
Lambeau d’Épaisseur Totale
Facteur clé : La rapidité de la cicatrisation dépend de l’épaisseur du caillot.
Chronologie :
3ème et 4ème jour : La résorption du caillot commence
6ème et 7ème jour : Le caillot laisse la place au tissu de granulation, qui sera progressivement remplacé par du tissu conjonctif
2ème et 3ème semaine : Phénomène de résorption osseuse et apposition tissulaire concomitante
3 semaines : Les ostéoblastes sont présents et la formation osseuse commence
Entre 4ème et 5ème semaine (40 jours) : Phases de maturation et de réparation complète
Important : Le lambeau d’épaisseur totale entraîne toujours une certaine résorption osseuse par dénudation du périoste.
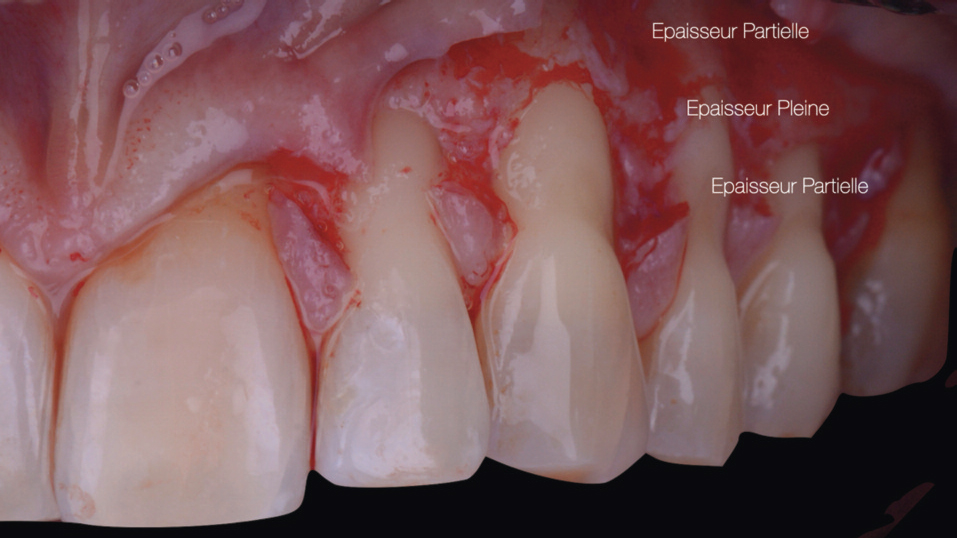
Lambeau d’Épaisseur Partielle
Avantage majeur : Le phénomène de résorption-apposition existe, mais dans ce cas il y a une certaine économie osseuse au cours de la cicatrisation grâce à la préservation du périoste.
Chronologie modifiée :
4ème jour : La résorption osseuse commence plus tôt (car le tissu conjonctif laissé en place est plus rapidement vascularisé)
Jusqu’à la fin de la 2ème semaine (15 jours) : La résorption se poursuit mais reste limitée
Conclusion : L’économie osseuse est significative par rapport au lambeau d’épaisseur totale, faisant du lambeau d’épaisseur partielle un choix préférentiel dans de nombreuses situations cliniques.

Lambeau de Widman Modifié et ENAP
Type de cicatrisation : La cicatrisation se caractérise par un long épithélium de jonction, y compris entre l’os et la surface radiculaire dans les lésions angulaires.
Similitude : Ce type d’intervention entraîne une cicatrisation comparable au lambeau d’épaisseur partielle.
Objectif : Ces techniques visent principalement la réduction de poche sans objectif régénérateur. L’accès pour le débridement est privilégié.
Lambeaux Déplacés : Greffes Pédiculées
Site Receveur
La cicatrisation comprend quatre stades distincts :
Stade 1 : Stade d’Adaptation (Jours 1 à 4)
Caractéristiques :
Une fine couche de fibrine s’interpose entre la surface radiculaire et le conjonctif du lambeau.
L’épithélium prolifère à la surface du lambeau et entre en contact avec la surface dentaire.
Phase critique : Cette phase est très fragile. Toute mobilisation du lambeau peut compromettre le résultat.
Stade 2 : Stade de Prolifération (Jours 4 à 21)
Jour 4 à 10 :
La couche de fibrine est progressivement envahie par le tissu conjonctif en provenance du lambeau.
Au bout de 10 jours, on observe des fibroblastes à la surface de la racine qui se différencient en cémentoblastes.
Jour 10 à 21 :
Des fibres de collagène prolifèrent le long de la surface mais il n’y a pas encore de liaison fibreuse véritable entre le tissu conjonctif et la surface de la racine.
Attention : À ce stade, le lambeau translatif ou la greffe gingivale libre reste encore très fragile. Il faut éviter toutes manœuvres traumatisantes (brossage vigoureux, alimentation dure).
L’épithélium, de son côté, prolifère à partir des bords coronaires en direction apicale, le long de la surface radiculaire.
Stade 3 : Stade d’Ancrage (À partir du 27ème jour)
Formation de l’attache :
Les fibres de collagène s’insèrent dans le néo-cément en formation.
Une véritable attache conjonctive commence à se former.
Stade 4 : Stade de Maturation (2 à 3 mois)
Maturation finale :
L’organisation des fibres de collagène se poursuit et au bout de 2 à 3 mois, elles s’insèrent solidement dans le cément.
La résistance mécanique de l’attache augmente progressivement.
Site Donneur
Lambeau déplacé coronairement : Cicatrisation de première intention (sutures possibles)
Lambeau déplacé latéralement, bi-papillaire, déplacé apicalement : Cicatrisation de deuxième intention (zone cruentée exposée)

Greffes Libres Épithélio-Conjonctives
Type de cicatrisation : Cicatrisation par première intention avec contact direct entre le conjonctif de la greffe et le périoste.
La cicatrisation est décrite en trois phases critiques :
Phase 1 : Phase Initiale (0-48 heures)
Nutrition “plasmatique” :
Pendant les premières 48h, le tissu greffé est nourri par une circulation “plasmatique” provenant des vaisseaux sanguins du lit receveur et de ses berges.
Phase critique : C’est la phase la plus critique. Le greffon doit rester parfaitement immobile. Toute mobilisation peut compromettre la survie du greffon.
Conseil clinique : Pansement chirurgical et sutures hermétiques sont essentiels.
Phase 2 : Phase de Revascularisation (Jours 2 à 11)
2ème jour :
Des vaisseaux et des capillaires se forment à partir du lit receveur et réalisent un pontage (anastomoses) avec les vaisseaux existant dans le greffon.
Limite : Ce pontage n’est possible que si la zone avasculaire n’est pas trop large (importance d’un greffon pas trop épais).
4ème jour :
La circulation sanguine est presque établie normalement dans le greffon.
Un nouveau tissu conjonctif unit fermement la greffe au conjonctif sous-jacent.
7ème jour :
La ré-épithélialisation commence à partir de la périphérie du greffon.
Phase 3 : Phase de Maturation (Jours 11 à 42)
14ème jour :
L’épithélium se kératinise et les fibres de collagène s’orientent fonctionnellement selon les lignes de force.
21ème jour :
Le tissu épithélial est complètement mature avec toutes ses couches.
Jusqu’au 42ème jour :
Le tissu conjonctif continue sa maturation, augmentant progressivement sa résistance mécanique.
Stabilité : À partir de 6 semaines, la greffe est solidement intégrée.
Site Donneur (Palais)
Type de cicatrisation : La plaie se cicatrise par deuxième intention (détersion, bourgeonnement, contraction et épithélialisation).
Chronologie :
Périphérie de la plaie : L’épithélialisation débute à la périphérie
10 à 15 jours : La plaie est complètement recouverte par un nouvel épithélium
7 à 15 jours supplémentaires : L’épithélium mature dans toute son épaisseur
4 mois : Maturation tissulaire complète
Important : Si un second prélèvement doit être effectué sur le même site, il faut attendre la maturation tissulaire complète, obtenue à partir de 4 mois.
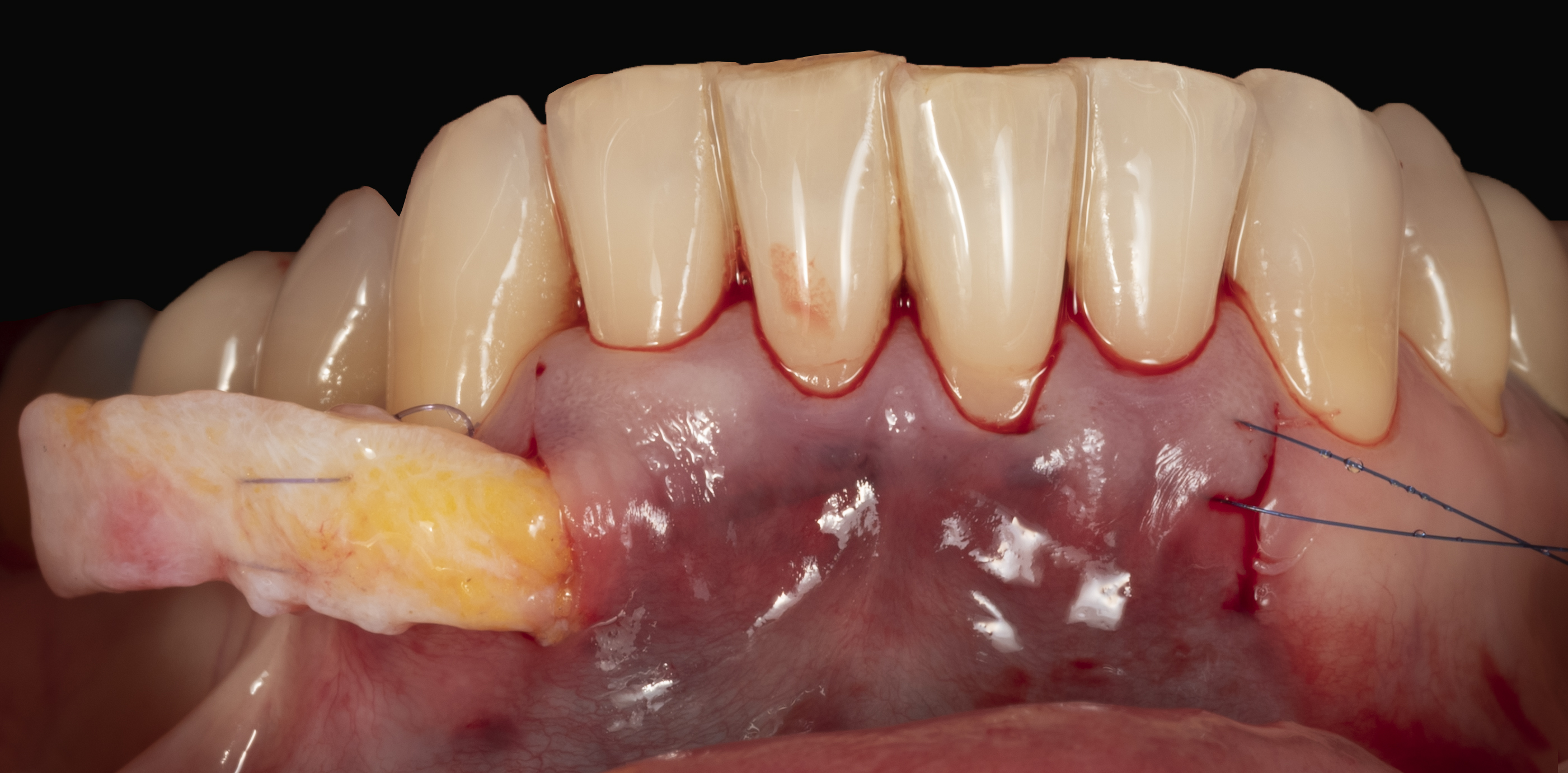
Greffes de Conjonctif Enfoui
Site Donneur
Avec les nouvelles techniques de prélèvement, notamment la technique de Bruno modifiée, la cicatrisation du site donneur se fait par première intention.
Avantage : Moins d’inconfort post-opératoire et cicatrisation plus rapide que le prélèvement traditionnel.
Site Receveur
Techniques bi-laminaires :
La cicatrisation du greffon se fait par première intention dans les techniques bi-laminaires :
- Greffe de Conjonctif (GC) associée à un lambeau déplacé coronairement
- GC associée à un lambeau déplacé latéralement
Techniques partiellement enfouies :
Dans les techniques de GC partiellement enfoui (technique de Bruno et technique de Langer) et la technique de l’enveloppe :
- Le greffon reste exposé au niveau de la partie coronaire du défaut radiculaire
- Sa cicatrisation est de deuxième intention dans cette zone
- Le reste du greffon cicatrise par première intention
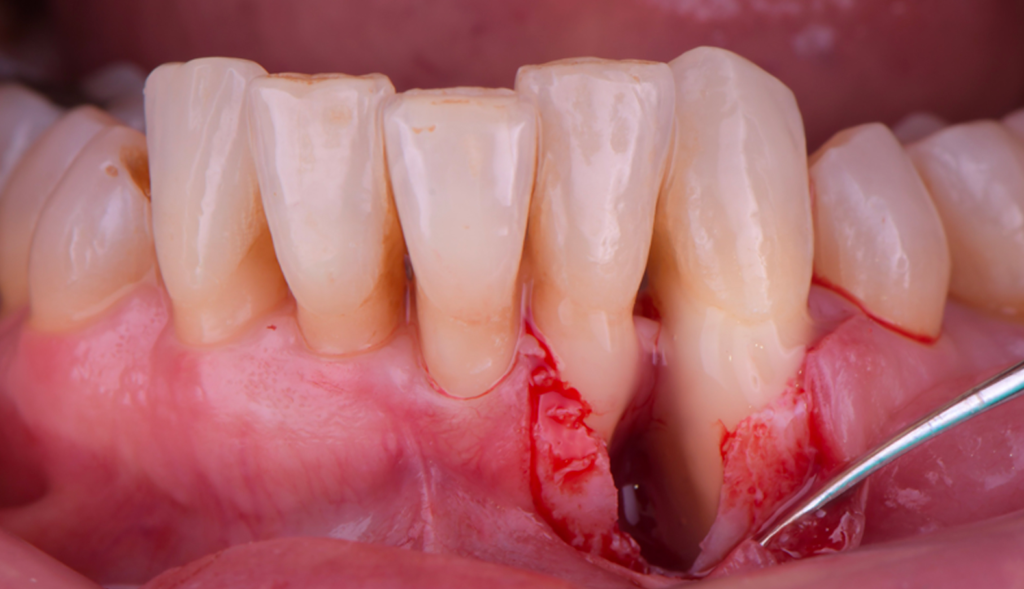
Chirurgie Osseuse Résectrice (COR)
Activité ostéoclastique :
Après COR, l’activité ostéoclastique (résorption) dure 2 à 3 semaines.
Phase de reconstruction :
Une phase de reconstruction ostéoblastique succède ensuite avec :
- Pic d’activité 3 à 4 semaines plus tard
- Une apposition osseuse achève la cicatrisation 6 mois plus tard
Stabilisation : La forme osseuse finale se stabilise généralement entre 6 et 12 mois post-opératoires.
Chirurgie Osseuse Reconstructrice
Mécanisme de cicatrisation :
La greffe d’os ostéogénique cicatrise à l’intérieur de l’os grandissant pendant le phénomène d’ostéogenèse, d’ostéo-induction et d’ostéo-conduction.
Gold Standard :
L’os autogène a longtemps été considéré comme le “gold standard” des matériaux de substitution osseuse. À l’heure actuelle, c’est le seul matériau ostéogénique reconnu.
Autres substituts osseux :
La plupart des autres substituts osseux ne permettent qu’une ostéo-conduction et/ou ostéo-induction. Ils se comportent comme une charpente pour conduire les facteurs de croissance (particulièrement les BMP) vers le site à combler.
Principe important :
La résorption du greffon osseux doit être simultanée avec la formation du nouvel os. Un déséquilibre peut conduire à :
- Résorption trop rapide : perte du volume greffé
- Résorption trop lente : retard de la régénération
Délai avant implantation :
Une fois le comblement osseux réalisé, une période de cicatrisation de 3 à 9 mois doit être observée avant de poser les implants dans le secteur greffé.
Ce délai permet :
- La maturation de l’os néoformé
- L’obtention d’une densité osseuse suffisante
- La vascularisation complète du site
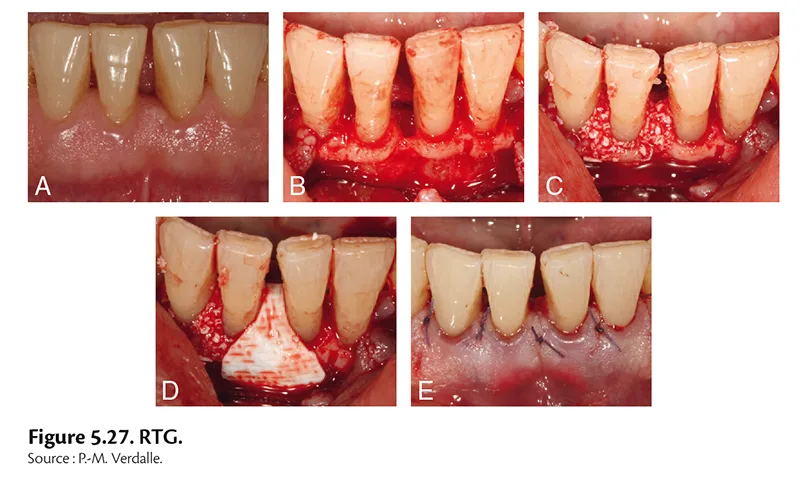
Cicatrisation par Régénération Tissulaire Guidée (RTG)
Principes biologiques fondamentaux :
La membrane RTG doit répondre aux principes biologiques suivants :
1. Histocompatibilité des surfaces : Pas de réaction inflammatoire excessive
2. Exclusion cellulaire : Limiter la progression apicale de l’épithélium et éviter le contact entre le tissu conjonctif du lambeau et la surface radiculaire
3. Stabilisation précoce du caillot : La membrane doit maintenir l’espace et stabiliser le caillot
4. Maintien de l’espace cicatriciel : Pour permettre la colonisation par les cellules du ligament parodontal
5. Adhérence du caillot : À la surface radiculaire
6. Induction cellulaire : Promotion de la différenciation des cellules souches en cellules parodontales
Délais de cicatrisation :
6 mois minimum : Quelle que soit la nature du matériau utilisé, on ne peut espérer obtenir de l’os avant 6 mois
6 à 12 mois : Selon certains auteurs, cette durée est nécessaire pour obtenir une cicatrisation incluant l’os alvéolaire
6 à 18 mois : Radiologiquement, l’os apparaît entre ces délais
Règle clinique : La patience est essentielle en RTG. Des évaluations trop précoces peuvent donner une impression d’échec alors que le processus régénératif est en cours.
XI. Facteurs Locaux Influençant la Cicatrisation
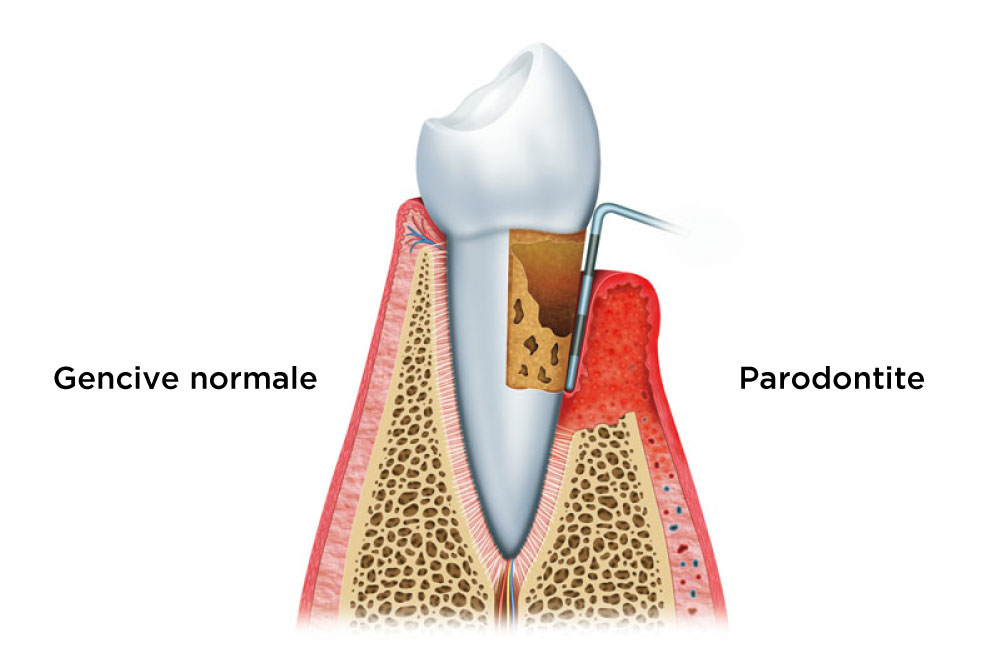
1. Facteurs Anatomiques
Siège de la plaie :
Le siège de la plaie dans le milieu buccal implique une difficulté majeure de stabilisation des pansements et des tissus en raison :
- Des mouvements constants (langue, joues, lèvres)
- De l’humidité permanente
- Des variations de pH salivaire
Morphologie de la lésion :
La morphologie de la lésion intervient dans la cicatrisation et conditionne certaines décisions thérapeutiques.
Exemples cliniques :
Certaines techniques nécessitent une importante quantité de tissu sain de recouvrement :
- Lambeau déplacé coronairement
- Techniques avec membranes RTG
D’autres ont besoin de tissu sain dans le but de recrutement tissulaire :
- Comblement osseux
- Régénération parodontale
Biotype parodontal :
Le biotype parodontal (fin vs épais) influence significativement :
- La capacité de cicatrisation
- Le risque de récession
- Le choix technique
2. Facteurs Microbiologiques
Défi bactérien constant :
La plaie est soumise au risque permanent d’infection car la cavité buccale abrite une communauté bactérienne complexe et abondante (environ 700 espèces différentes).
Rôle du pansement chirurgical :
Le pansement chirurgical permet la protection de la plaie mais favorise paradoxalement la stagnation des micro-organismes sous le pansement.
Solution : Hygiène rigoureuse et utilisation de bains de bouche antiseptiques en post-opératoire.
3. Facteurs Histologiques
Compartiment ostéo-desmodontal :
Les tissus desmodontaux pourraient acquérir leur potentiel régénérateur à partir de tissus osseux.
Il apparaît donc plus logique de parler d’un “compartiment ostéo-desmodontal” qui serait le siège d’une coaptation tissulaire.
Compétition tissulaire :
Ce compartiment est en compétition avec le compartiment épithélio-conjonctif gingival, qui prolifère plus rapidement.
Conséquence :
Toute perte de substance importante ou nécrose périphérique entraîne :
- Un retard de fermeture
- Une cicatrice pathologique
- Un risque de migration épithéliale apicale
4. Facteurs Mécaniques
Ces facteurs sont parmi les plus importants et les plus contrôlables par le praticien.
Distance des Berges (Étendue de la Plaie)
Plus la distance entre les berges est importante, plus la cicatrisation sera longue et difficile.
Règle clinique : Favoriser les techniques permettant un rapprochement maximal des berges (sutures sans tension).
Volume du Caillot
Il faut obtenir un caillot peu épais par compression douce des surfaces, tout en maintenant un espace favorable à la régénération.
Paradoxe : Trop de caillot retarde la cicatrisation, pas assez d’espace compromet la régénération.
Adhérence de l’Interface
L’adhésion précoce du caillot est une condition nécessaire à la régénération. Cette liaison est fragile et ne doit en aucun cas être perturbée.
Applications pratiques :
Dépose des sutures : Les sutures sont déposées vers le 14ème jour, afin de ne pas provoquer un décollement de l’interface tissu-racine.
Protection post-opératoire : Éviter tout traumatisme pendant les 2 premières semaines.
Forces Exercées sur le Caillot
Les forces exercées par :
- La mastication
- Le brossage (trop vigoureux ou trop précoce)
- Les mouvements de la langue
Ces forces créent une mobilité du pansement et une perturbation de la cicatrisation.
Recommandations :
- Alimentation molle pendant 2 semaines
- Brossage doux et adapté
- Éviter la zone opérée initialement
Forces Occlusales
Les forces occlusales exagérées engendrant une mobilité dentaire occasionnent un trouble lors de la cicatrisation, voire un échec chirurgical.
Solutions :
- Ajustement occlusal préopératoire si nécessaire
- Contention temporaire dans certains cas
- Éviter la mastication sur les dents traitées
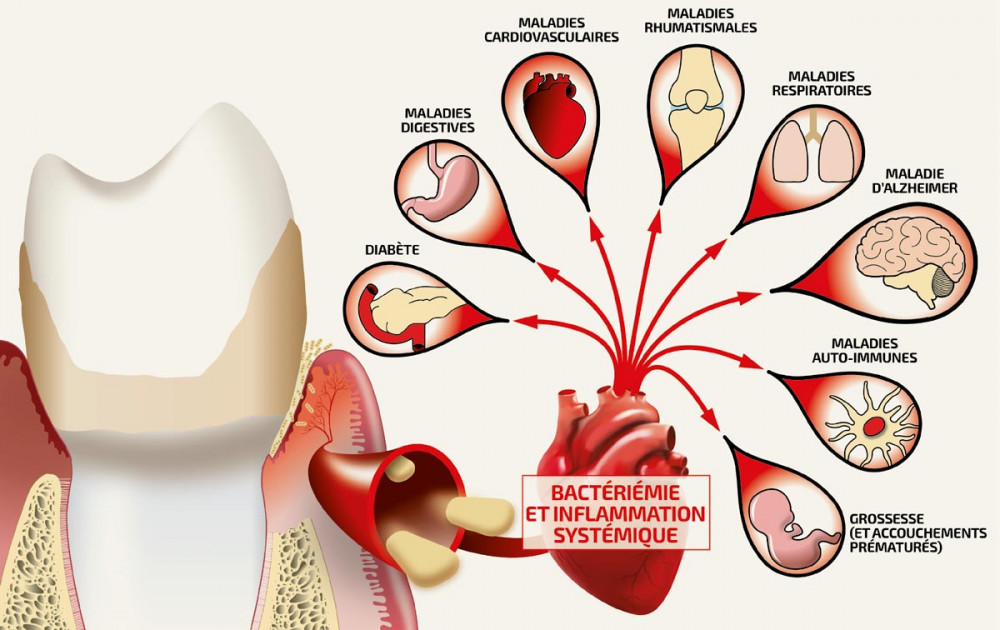
XII. Facteurs Généraux Influençant la Cicatrisation
1. L’Âge
Le processus cicatriciel est plus actif chez les sujets jeunes car la multiplication cellulaire se fait plus aisément.
Avec l’âge :
- Les cellules vieillissent
- Leur métabolisme diminue
- La cicatrisation parodontale devient plus lente et moins prévisible
- La vascularisation diminue
- La réponse immunitaire s’affaiblit
Implication clinique : Adapter les techniques et les attentes selon l’âge du patient.
2. Facteurs Nutritionnels
L’intense activité cellulaire mise en jeu par la cicatrisation nécessite un apport protidique et vitaminique suffisant.
Balance Azotée Positive
Lors du processus de cicatrisation, la balance azotée doit être positive. C’est-à-dire que les apports protéiques doivent être plus importants que les fuites protéiques.
Besoins Spécifiques
Le soin nutritionnel de la cicatrisation doit répondre de manière spécifique aux besoins majorés :
Protéines :
- Indispensables au processus de cicatrisation
- Besoin augmenté de 50 à 100% par rapport aux besoins normaux
Acides aminés spécifiques :
- Arginine : précurseur du collagène et de l’oxyde nitrique
- Proline : constituant majeur du collagène
Calories :
- Soutiennent l’anabolisme
- Permettent d’épargner les protéines pour la cicatrisation
Acides gras poly-insaturés :
- Favorisent la formation des membranes cellulaires
- Rôle anti-inflammatoire (Oméga-3)
Antioxydants :
- Vitamine C : cofacteur essentiel de la synthèse du collagène
- Vitamine E : protection contre le stress oxydatif
- Zinc : stimule la régénération tissulaire et la fonction immunitaire
Eau :
- Les besoins en eau sont augmentés en situation de cicatrisation
- Apport nécessaire : 1,5 à 2,5 litres par jour
Conseil pratique : Prescrire une supplémentation nutritionnelle dans les situations à risque (patients âgés, dénutris, fumeurs).
3. Facteurs Hormonaux
Glucocorticoïdes :
Les glucocorticoïdes (cortisol endogène, corticothérapie) ralentissent la cicatrisation en :
- Diminuant la collagénèse
- Réduisant la néo-vascularisation
- Affaiblissant la réponse inflammatoire initiale
- Inhibant la prolifération fibroblastique
Autres hormones :
- Hormones thyroïdiennes : influencent le métabolisme général
- Hormones sexuelles : peuvent moduler la réponse inflammatoire
4. Facteurs Toxiques
Alcool
L’alcool a un rôle toxique multiple :
- Altération de la fonction immunitaire
- Perturbation de la synthèse protéique
- Déficits nutritionnels associés
- Déshydratation
Tabac
Le tabagisme est l’un des facteurs les plus délétères pour la cicatrisation parodontale :
Effets négatifs :
- Vasoconstriction des capillaires
- Diminution de l’oxygénation des tissus
- Altération de la fonction des fibroblastes
- Diminution de la production de collagène
- Affaiblissement de la réponse immunitaire
- Augmentation du risque infectieux
Impact clinique : Le taux d’échec des interventions parodontales est 2 à 3 fois plus élevé chez les fumeurs.
Recommandation forte : Sevrage tabagique au moins 2 semaines avant et 6 semaines après l’intervention.
5. Maladies Systémiques
Maladies Hématologiques
Troubles de la coagulation :
- Hémorragies incontrôlées
- Désorganisation du caillot
- Retard de cicatrisation
Anémie :
- Diminution de l’oxygénation tissulaire
- Ralentissement de la cicatrisation
Insuffisance Rénale
L’élévation de l’urée sanguine est un cofacteur de retard de cicatrisation par :
- Altération de la qualité du collagène
- Perturbation de la fonction plaquettaire
- Déficit immunitaire associé
Diabète
Le diabète est caractérisé par de multiples altérations :
Altération du chimiotactisme :
- Diminution de la migration leucocytaire
- Affaiblissement de la réponse inflammatoire
Microangiopathie :
- Épaississement de la membrane basale des capillaires
- Diminution de la perfusion tissulaire
- Risque d’ischémie régionale
Hyperglycémie :
- Glycation des protéines (dont le collagène)
- Altération de la fonction leucocytaire
- Susceptibilité accrue aux infections
Gestion clinique :
- Contrôle glycémique optimal avant intervention (HbA1c < 7%)
- Antibioprophylaxie à discuter
- Surveillance post-opératoire renforcée
Pour un diabétique bien contrôlé, la cicatrisation peut être presque normale. Un diabète mal contrôlé est une contre-indication relative à la chirurgie parodontale.
6. Atteinte Immunologique
Les cellules immunocompétentes interviennent à différents niveaux de la cicatrisation.
Neutropénie :
- Altère la qualité de la phase inflammatoire
- Augmente le risque infectieux
- Retarde la détersion de la plaie
Immunosuppression :
- Déficit de la réponse inflammatoire
- Susceptibilité aux infections
- Retard de cicatrisation
Maladies auto-immunes :
- Inflammation chronique
- Altération de la cicatrisation normale
7. Facteurs Médicamenteux
Corticoïdes
Les corticoïdes présentent, à des doses élevées, une action inhibitrice multiple :
- Prolifération des fibroblastes ↓
- Chimiotactisme des macrophages ↓
- Synthèse du collagène ↓
- Synthèse des prostaglandines ↓
- Synthèse des glycosaminoglycanes ↓
- Formation du tissu de granulation ↓
- Épithélialisation ↓
Gestion clinique :
- Évaluer le rapport bénéfice/risque
- Adapter le protocole chirurgical
- Envisager une supplémentation vitaminique
Autres Médicaments
Immunosuppresseurs :
- Diminution de la synthèse de collagène
- Risque infectieux majoré
Anticoagulants :
- Risque hémorragique
- Nécessité d’adaptation du protocole
Bisphosphonates :
- Risque d’ostéonécrose (rare en parodontologie)
- Prudence avec les chirurgies osseuses
XIII. Facteurs Accélérant ou Retardant la Cicatrisation
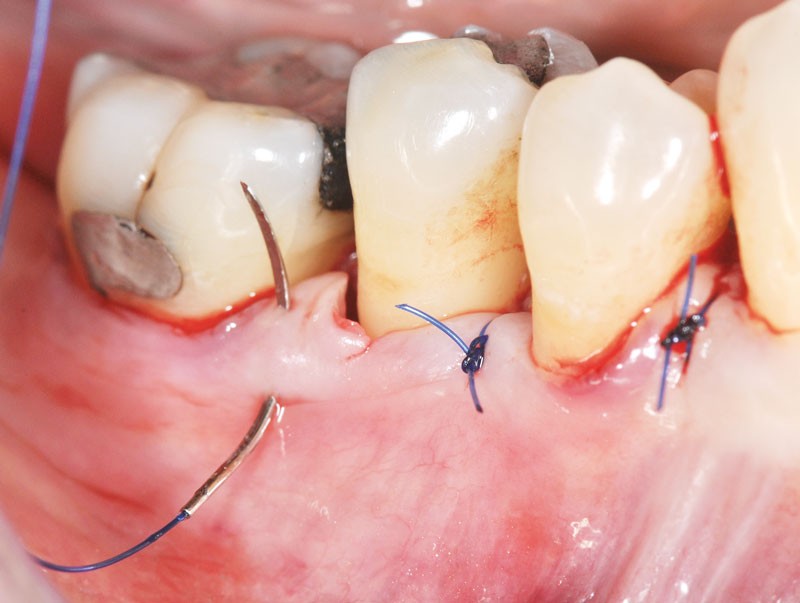
Facteurs Accélérant la Cicatrisation
1. Facteurs de Croissance
Durant la dernière décennie, plusieurs facteurs de croissance ont été identifiés et caractérisés. Certains semblent contribuer significativement à la régénération parodontale et osseuse.
Principaux facteurs de croissance :
PDGF (Platelet-Derived Growth Factor) :
- Stimule la migration et la prolifération des cellules du ligament parodontal
- Favorise la formation de nouveau cément et de nouvel os
- Disponible commercialement pour usage clinique
TGF-β (Transforming Growth Factor-beta) :
- Régule la prolifération cellulaire
- Stimule la synthèse de la matrice extracellulaire
- Impliqué dans la différenciation des ostéoblastes
IGFs (Insulin-Like Growth Factors) :
- Stimulent la prolifération des ostéoblastes
- Favorisent la synthèse du collagène
FGF (Fibroblast Growth Factor) :
- Stimule l’angiogenèse
- Favorise la prolifération des fibroblastes
BMPs (Bone Morphogenic Proteins) :
- Induisent la différenciation des cellules souches en ostéoblastes
- Propriétés ostéo-inductrices puissantes
- BMP-2 et BMP-7 les plus étudiées
EGF (Epidermal Growth Factor) :
- Stimule la prolifération des fibroblastes
- Active les kératinocytes
- Favorise la prolifération des cellules endothéliales vasculaires
Caractéristiques communes :
- Liaison à des récepteurs spécifiques à la surface des cellules cibles
- Action principalement locale
- Multifonctionnalité permettant de stimuler et/ou réguler diverses activités cellulaires
EMD (Enamel Matrix Derivatives) :
- Dérivés de la matrice amélaire
- Favorisent la régénération parodontale
- Utilisés couramment en clinique (Emdogain®)
2. Antibiotiques
L’antibiotique favorise ou facilite la cicatrisation en empêchant toute agression bactérienne.
Important : La prescription ne doit pas être systématique et ne remplace en aucun cas le traitement mécanique conventionnel (détartrage-surfaçage).
Indications des antibiotiques en chirurgie parodontale :
- Patients à risque (immunodéprimés, diabétiques)
- Greffes osseuses et RTG
- Parodontites agressives
- Certaines chirurgies complexes
Molécules fréquemment utilisées :
- Amoxicilline + acide clavulanique
- Métronidazole (+ amoxicilline dans certains cas)
- Azithromycine
- Doxycycline
3. Vitamines et Oligo-éléments
Vitamine C (Acide ascorbique) :
- Cofacteur essentiel de la synthèse du collagène
- Favorise la cicatrisation
- Dose recommandée : 500-1000 mg/jour en période post-opératoire
Vitamine A :
- Stimule l’épithélialisation
- Favorise la différenciation cellulaire
- Contre-balance partiellement les effets négatifs des corticoïdes
Vitamine D :
- Essentielle pour le métabolisme osseux
- Favorise l’absorption du calcium
- Rôle immunomodulateur
Vitamine K :
- Essentielle pour la coagulation
- Prévient les hémorragies
Vitamines du groupe B :
- Impliquées dans le métabolisme énergétique cellulaire
- Favorisent la cicatrisation
Fer :
- Nécessaire pour l’oxygénation tissulaire
- Prévient l’anémie
Magnésium :
- Cofacteur de nombreuses enzymes
- Impliqué dans la synthèse protéique
Cuivre :
- Cofacteur de la lysyl oxydase (réticulation du collagène)
- Favorise la production de collagène
Manganèse :
- Cofacteur enzymatique
- Impliqué dans la formation de la matrice osseuse
Zinc :
- Stimule la prolifération cellulaire
- Favorise la cicatrisation
- Renforce la fonction immunitaire
- Dose recommandée : 15-30 mg/jour en période de cicatrisation
Sélénium :
- Propriétés antioxydantes
- Protège contre le stress oxydatif

Facteurs Retardant la Cicatrisation
1. Obésité
Mécanismes :
- Diminution de la vascularisation du tissu adipeux
- Augmentation de la tension dans la plaie
- Inflammation chronique de bas grade
- Résistance à l’insuline
Impact clinique : Les patients obèses ont un risque accru de complications post-opératoires.
2. Tabagisme
Effets délétères multiples :
- Diminution de l’oxygénation de la plaie (vasoconstriction)
- Anomalies de la coagulation dans les petits vaisseaux sanguins
- Altération de la fonction des fibroblastes et de la synthèse du collagène
- Affaiblissement de la réponse immunitaire
- Augmentation du risque infectieux
Quantification : Le taux d’échec en chirurgie parodontale est multiplié par 2 à 3 chez les fumeurs.
Solution : Sevrage tabagique recommandé (idéalement 2 semaines avant et 6-8 semaines après).
3. Âge Avancé
Conséquences du vieillissement :
- Affaiblissement des défenses immunitaires
- Diminution de la résistance aux germes pathogènes
- Ralentissement du métabolisme cellulaire
- Diminution de la vascularisation
- Comorbidités associées
4. Diabète
Mécanismes de retard :
- Dysfonctionnement leucocytaire dû à l’hyperglycémie
- Risque d’ischémie régionale (oblitération vasculaire)
- Épaississement de la membrane basale des capillaires
- Glycation des protéines (dont le collagène)
- Susceptibilité accrue aux infections
Gestion : Le contrôle glycémique optimal est essentiel (HbA1c < 7%).
5. Mauvaise Circulation
Conséquences :
- Mauvaise alimentation de la plaie en substances nutritives
- Déficit d’apport en cellules sanguines
- Hypoxie tissulaire
- Retard de cicatrisation
Pathologies concernées :
- Artériopathie périphérique
- Maladie de Raynaud
- Insuffisance veineuse
6. Malnutrition
Effets :
- Perturbations de la phase inflammatoire
- Altération de la synthèse de collagène
- Déficit en protéines, vitamines et oligo-éléments
- Affaiblissement immunitaire
Populations à risque :
- Personnes âgées
- Patients atteints de maladies chroniques
- Troubles du comportement alimentaire
7. Médicaments Immunosuppresseurs
Effets :
- Diminution de la synthèse de collagène
- Affaiblissement de la réponse inflammatoire
- Risque infectieux accru
Exemples :
- Corticostéroïdes
- Méthotrexate
- Ciclosporine
- Tacrolimus
8. Irradiation (Radiothérapie)
Mécanismes :
- Diminution de l’irrigation sanguine par rétrécissement de la lumière vasculaire
- Fibrose tissulaire
- Altération de la capacité de cicatrisation
- Risque d’ostéoradionécrose
Gestion : Grande prudence avec les chirurgies osseuses chez les patients irradiés.
9. Stress Important
Mécanismes :
- L’augmentation du cortisol diminue le nombre de lymphocytes circulants
- Atténuation de la réaction inflammatoire
- Affaiblissement immunitaire
- Troubles du sommeil impactant la cicatrisation
Solution : Gestion du stress et anxiolyse si nécessaire.
10. Déficit Sensitif dans la Région de la Plaie
Conséquences :
- Réduction de la réaction inflammatoire
- Diminution de la réaction vasomotrice
- Risque de traumatisme non perçu
11. Corticoïdes
Effets multiples :
- Ralentissement de l’épithélialisation
- Diminution de la néo-vascularisation
- Inhibition de la contraction de la plaie
- Affaiblissement de la réponse inflammatoire
- Réduction de la synthèse de collagène
Dose-dépendant : Les effets sont proportionnels à la dose et à la durée du traitement.
Remarques Cliniques Importantes
Mobilité Dentaire
La mobilité dentaire rend instable la plaie, quelle que soit la nature d’intervention parodontale.
Solution : Réaliser une contention préopératoire si nécessaire.
Dans les greffes gingivales :
- Il faut impérativement que le greffon soit parfaitement stable
- Réalisation de sutures hermétiques
- Mise en place d’un pansement chirurgical adapté
Technique Chirurgicale
Facteurs d’échec liés à la technique :
- Utilisation d’instruments souillés
- Non-maîtrise des techniques chirurgicales
- Respect insuffisant des principes biologiques
- Traumatisme tissulaire excessif

Biotype Parodontal
Biotype fin :
- Plus fragile
- Risque accru de récession
- Nécessite des techniques adaptées
- Cicatrisation parfois moins prévisible
Biotype épais :
- Plus résistant aux traumatismes
- Cicatrisation généralement favorable
- Permet des techniques variées
Ces facteurs risquent d’occasionner l’échec de la thérapeutique chirurgicale s’ils ne sont pas pris en compte et maîtrisés.
XIV. Conclusion
Si des travaux de recherche clinique et de recherche fondamentale ont apporté des preuves scientifiques de la possibilité de formation d’une nouvelle attache, force est de constater qu’il n’existe pas actuellement de techniques chirurgicales donnant des résultats reproductibles et applicables systématiquement en clinique permettant la régénération totale des tissus perdus au cours de la maladie parodontale.

État Actuel des Connaissances
Les techniques de thérapeutiques régénératrices ou reconstructrices utilisées à ce jour aboutissent le plus souvent à :
- La formation d’une attache épithéliale longue
- Un comblement osseux (pas toujours complet)
- Plutôt qu’à la formation d’une véritable nouvelle attache conjonctive fonctionnelle
Progrès et Perspectives
Néanmoins, des progrès significatifs ont été réalisés :
Régénération Tissulaire Guidée (RTG) :
- Amélioration des membranes (résorbables vs non résorbables)
- Meilleure compréhension des principes biologiques
- Résultats encourageants dans certaines indications (lésions intra-osseuses)
Facteurs de croissance :
- PDGF, BMPs, EMD montrent des résultats prometteurs
- Utilisation clinique en augmentation
- Nécessité de protocoles standardisés
Biomatériaux :
- Évolution constante des substituts osseux
- Amélioration de l’ostéo-conduction
- Développement de matériaux bioactifs
Ingénierie tissulaire :
- Utilisation de cellules souches
- Thérapie génique (stade expérimental)
- Médecine régénérative personnalisée

Messages Clés pour le Praticien
1. Comprendre les limites biologiques
La cicatrisation parodontale reste un défi en raison de :
- L’environnement contaminé permanent
- La compétition entre différents types cellulaires
- La complexité de la régénération de tissus multiples
2. Maîtriser les principes fondamentaux
Le succès thérapeutique repose sur :
- La compréhension des mécanismes de cicatrisation
- Le respect des principes biologiques
- La maîtrise technique
- Le contrôle des facteurs locaux et généraux
3. Adopter une approche réaliste
Plutôt que de viser systématiquement la régénération complète (souvent impossible), il faut :
- Se fixer des objectifs thérapeutiques réalistes
- Privilégier l’arrêt de la progression de la maladie
- Obtenir une réparation stable et fonctionnelle
- Améliorer la qualité de vie du patient
4. Personnaliser l’approche thérapeutique
Chaque patient est unique avec :
- Des facteurs de risque spécifiques
- Une anatomie particulière
- Des attentes différentes
- Des capacités de cicatrisation variables
5. Maintenir une veille scientifique
La parodontologie évolue rapidement :
- Nouvelles techniques
- Nouveaux matériaux
- Meilleure compréhension des mécanismes biologiques
- Formation continue indispensable
Vision d’Avenir
L’avenir de la cicatrisation parodontale s’oriente vers :
Médecine personnalisée :
- Identification des profils de patients à risque
- Adaptation des protocoles thérapeutiques
- Prédiction des résultats
Thérapies biologiques :
- Facteurs de croissance de nouvelle génération
- Cellules souches et ingénierie tissulaire
- Modulation de l’inflammation
Technologies innovantes :
- Impression 3D de tissus
- Biomatériaux intelligents
- Nanomédecine
Approche intégrative :
- Lien avec la santé générale
- Prise en compte du microbiome
- Nutrition et mode de vie
Recommandations Finales
Pour optimiser la cicatrisation parodontale, le praticien doit :
- Établir un diagnostic précis de la lésion parodontale
- Contrôler l’inflammation avant toute chirurgie
- Préparer le patient (hygiène, facteurs de risque)
- Choisir la technique appropriée selon l’indication
- Maîtriser le geste chirurgical (atraumatique, précis)
- Respecter les principes biologiques de cicatrisation
- Assurer un suivi rigoureux post-opératoire
- Maintenir les résultats par thérapie parodontale de soutien
La cicatrisation parodontale demeure un domaine en constante évolution. Si la régénération complète « ad integrum » reste un objectif difficile à atteindre de manière prévisible, les progrès scientifiques et techniques permettent aujourd’hui d’obtenir des résultats cliniques satisfaisants et stables dans le temps, améliorant significativement le pronostic et la qualité de vie des patients atteints de maladies parodontales.
La clé du succès réside dans la compréhension approfondie des mécanismes biologiques de cicatrisation et leur application rigoureuse dans la pratique clinique quotidienne.
Ressources Complémentaires pour Approfondir
Lectures Essentielles
Pour les étudiants souhaitant approfondir leurs connaissances en parodontologie et cicatrisation, plusieurs ouvrages de référence en français sont disponibles :
Pour la pratique clinique quotidienne :
Le Guide clinique d’odontologie constitue une référence complète et actualisée, couvrant l’ensemble des aspects de la pratique odontologique, y compris la parodontologie.
Pour la formation académique :
Les Annales corrigées de l’internat en odontologie 2022-2024 permettent de se préparer efficacement aux examens tout en consolidant ses connaissances fondamentales.
Pour la spécialisation en chirurgie :
L’ouvrage Chirurgie orale offre une approche détaillée et illustrée des interventions chirurgicales, incluant les aspects cicatriciels.
Pour approfondir la parodontologie :
Le Référentiel internat en parodontologie constitue la référence académique pour la formation spécialisée en parodontologie.
Plateforme d’Entraînement en Ligne
Pour tester vos connaissances et vous entraîner avec des QCM en médecine dentaire, la plateforme ResiDentaire™ propose des ressources pédagogiques adaptées aux étudiants et praticiens.
Note de transparence : Cette page contient des liens d’affiliation. En cliquant dessus, vous n’êtes pas tenu de vous procurer les produits suggérés, mais si vous le faites, cela ne vous coûte rien de plus et cela m’aide à financer ce site et à continuer à produire du contenu éducatif de qualité pour la communauté dentaire.
Dernière mise à jour : Février 2026
Mots-clés : Cicatrisation parodontale, régénération tissulaire, réparation parodontale, RTG, facteurs de croissance, chirurgie parodontale, ligament parodontal, os alvéolaire, épithélialisation, tissu de granulation

Leave a Reply