Anesthésiques Locaux – Anesthésiologie Dentaire
Introduction
- Définition : Les anesthésiques locaux (AL) entraînent une perte de sensibilité au niveau du lieu d’administration.
- Mécanisme : Ils bloquent de façon réversible la transmission nerveuse.
- Utilisation : Largement utilisés en odontologie, anesthésiologie et dans de nombreuses spécialités médicales et chirurgicales.
- Indications principales : Prévention de la sensation de douleur.
Indications
- Anesthésie locale ou régionale.
- Actes chirurgicaux.
- Gestion des douleurs aiguës ou chroniques.
- Utilisation thérapeutique ou diagnostique.
- Remarque : L’anesthésie locorégionale comporte des risques et des accidents.
Historique
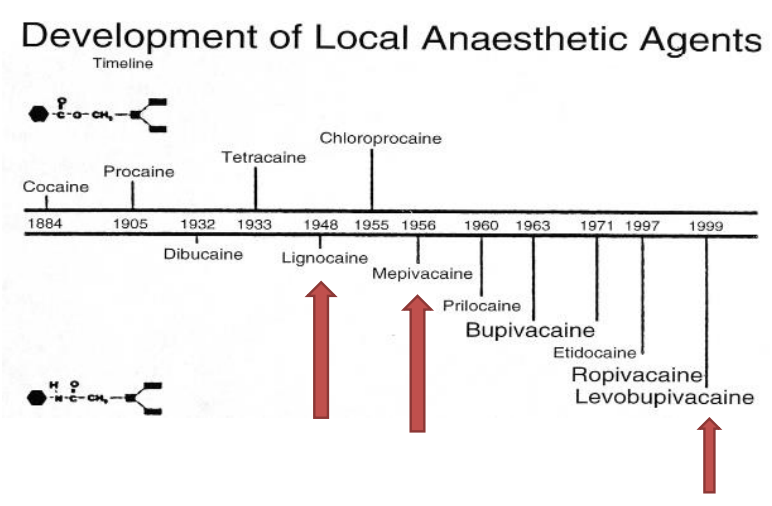
Développement des anesthésiques locaux
- Timeline du développement des agents anesthésiques locaux.
Physiologie
- Principe : L’anesthésie locale entraîne une perte de sensibilité par interruption de la conduction nerveuse.
- Mécanisme : La conduction de l’influx nerveux est liée aux modifications du gradient électrique via les canaux sodiques.
- Effet des AL : Inhibition réversible de la conduction nerveuse sans altération du nerf.
- Types de fibres affectées : Fibres sensitives, motrices et végétatives.
- Ordre de disparition des sensations :
- Sensation douloureuse.
- Sensation thermique.
- Sensation tactile.
Classification des fibres nerveuses
| Type de fibre | Myélinisation | Diamètre (µm) | Vitesse de conduction (m/s) | Fonction |
|---|
| Aα | ++ | 10-25 | 60-100 | Fibres motrices et proprioceptrices |
| Aβ, Aγ | ++ | 4-12 | 20-100 | Fibres sensitives et proprioceptrices |
| Aδ | + | 1-6 | 3-25 | Douleur, température, toucher |
| B | + | <3 | 3-15 | SNA préganglionaire |
| C | 0 | 0,3-2 | 0,2-2,5 | SNA postganglionaire, douleur, température, toucher |
Propriétés physicochimiques
- Mécanisme d’action primaire : Blocage des canaux sodiques voltage et temps dépendant.
- Propriétés essentielles :
- Solubilité lipidique.
- Fixation aux protéines.
- Degré d’ionisation.
Solubilité lipidique
- Les fibres nerveuses sont composées à 70 % de lipides.
- Une grande liposolubilité favorise une diffusion importante.
- Mesurée par le coefficient de partage huile/eau.
Fixation aux protéines
- Conditionne la durée d’action des AL.
- Une forte fixation protéique entraîne une durée d’action prolongée.
Degré d’ionisation
- Influence la capacité de l’AL à traverser les membranes.
Mécanisme d’action
- Action principale : Blocage des canaux sodiques voltage et temps dépendant.
- Impact : Stabilisation des membranes nerveuses par inhibition des flux sodiques entrants.
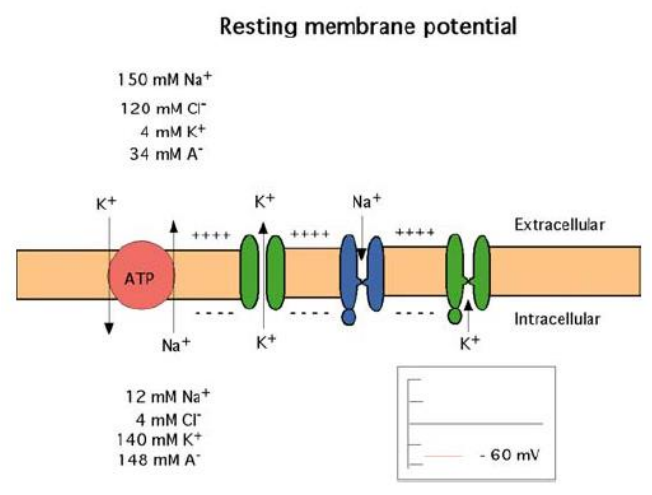
Potentiel de membrane au repos
- Maintien de l’équilibre électrique de la membrane nerveuse.
Potentiel d’action
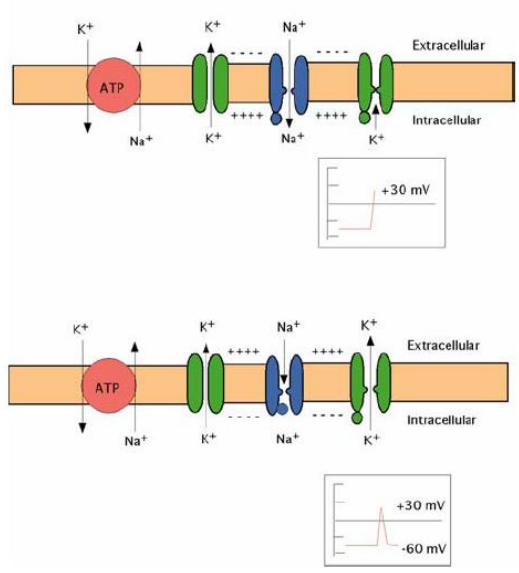
- Modifications électriques permettant la conduction nerveuse, bloquées par les AL.
Classification des anesthésiques locaux
- Structure moléculaire : Tous les AL possèdent une molécule composée de trois parties :
- Cycle aromatique (acide benzoïque ou para-amino-benzoïque) : pôle lipophile, rôle dans la diffusion et la fixation.
- Pôle hydrophile : Dérivé amine tertiaire (rarement secondaire) de l’alcool éthylique ou de l’acide acétique.
- Chaîne intermédiaire : Influence la liposolubilité, l’hydrosolubilité, la puissance et la toxicité.
Types de liaisons
- Liaison ester :
- Instable, dégradation rapide par hydrolyse enzymatique.
- Liaison amide :
- Plus stable, dégradation hépatique plus lente, durée d’action prolongée.
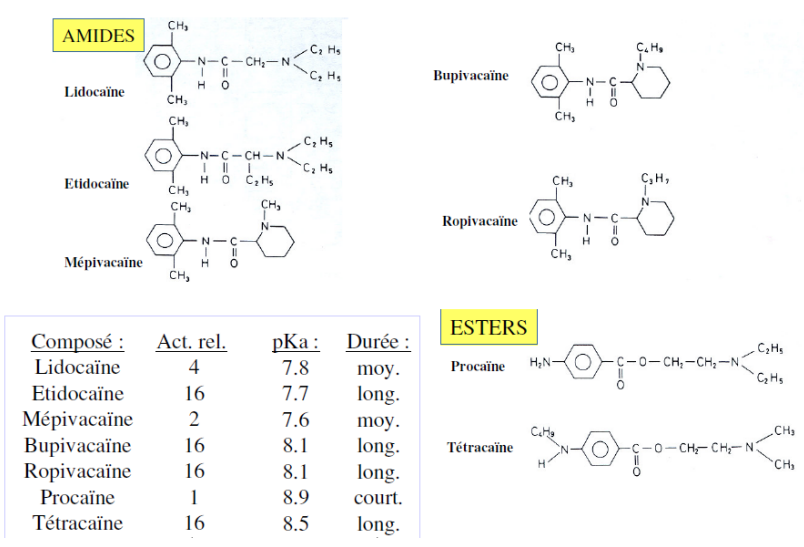
Pharmacologie
- Structure commune : Tous les AL partagent une structure moléculaire similaire et un mode d’action comparable.
- Différences entre molécules :
- Puissance.
- Délai d’action.
- Durée d’action.
- Toxicité.
Bloc anesthésique
- Délai d’action :
- Dépend de la fraction libre disponible pour traverser la fibre nerveuse.
- AL à faible pKa (lidocaïne, mépivacaïne) : 50 % non ionisés, diffusion rapide.
- AL à pKa élevé (tétracaïne, bupivacaïne) : Plus ionisés, diffusion plus lente.
- Puissance et durée d’action :
- Déterminées par le degré d’hydrophobie et le poids moléculaire.
- Solubilité lipidique élevée (bupivacaïne, étidocaïne) : Puissance et durée d’action supérieures.
- Solubilité faible (procaïne, chloroprocaïne) : Puissance et durée d’action réduites.
Tableau des propriétés pharmacologiques
| Agent | pKa | % Ionisé (Plasma, pH 7,40) | % Ionisé (Tissu, pH 7,10) |
|---|
| Procaïne | 8,9 | 97 | 99 |
| Chloroprocaïne | 8,7 | 95 | 98 |
| Tétracaïne | 8,5 | 93 | 96 |
| Lidocaïne | 7,9 | 76 | 86 |
| Prilocaïne | 7,9 | 76 | 86 |
| Mépivacaïne | 7,6 | 61 | 76 |
| Bupivacaïne | 8,1 | 83 | 91 |
| Étidocaïne | 7,7 | 66 | 80 |
| Ropivacaïne | 8,1 | 83 | 91 |
Comparaison des anesthésiques locaux
| Agent | Poids moléculaire | pKa | Coefficient de partage | Fixation protéique | Délai d’action | Durée d’action | Puissance |
|---|
| Esters | | | | | | | |
| Procaïne | 236 | 8,9 | 0,02 | 6 % | Long | 1h-1h30 | 0,5 |
| Chloroprocaïne | 271 | 8,7 | 0,14 | ? | Court | 1h | 1 |
| Tétracaïne | 264 | 8,5 | 4,1 | 80 % | Long | 3-4h | 4 |
| Amides | | | | | | | |
| Lidocaïne | 234 | 7,9 | 2,9 | 65 % | Court | 1h30-2h | 1 |
| Prilocaïne | 220 | 7,9 | 0,9 | 55 % | Court | 1h30-2h | 1 |
| Mépivacaïne | 246 | 7,6 | 0,8 | 75 % | Court | 2-3h | 1 |
| Bupivacaïne | 288 | 8,1 | 27,5 | 95 % | Intermédiaire | 3h-3h30 | 4 |
| Étidocaïne | 276 | 7,7 | 141 | 95 % | Court | 3h-4h | 4 |
| Ropivacaïne | 274 | 8,1 | 6,1 | 94 % | Intermédiaire | 2h30-3h | 3,3 |
Autre tableau comparatif
| Agent | Poids moléculaire | pKa | Coefficient de partage | Liaison protéique | Délai d’installation relatif | Puissance relative | Durée d’action relative |
|---|
| Amino-esters | | | | | | | |
| Procaïne | 272 | 8,9 | 0,6 | 5,80 % | 1 | 1 | 1 |
| Chloroprocaïne | 271 | 8,7 | – | – | – | – | – |
| Tétracaïne | 301 | 8,5 | 80 | 75 % | 2 | 16 | 8 |
| Articaine | 321 | 7,8 | 40 | 95 % | 0,8 | 6 | 2 |
| Amides | | | | | | | |
| Lidocaïne | 271 | 7,9 | 2,9 | 64 % | 0,8 | 4 | 1,5 |
| Mépivacaïne | 283 | 7,6 | 0,8 | 78 % | 1 | 2 | 1,5 |
| Bupivacaïne | 325 | 8,1 | 27,5 | 95 % | 0,6 | 16 vinosine | 8 |
| Prilocaïne | 257 | 7,9 | 0,8 | 55 % | 1 | 3 | 1,5 |
| Étidocaïne | 313 | 7,7 | 141 | 94 % | 0,4 | 16 | 8 |
| Ropivacaïne | 274 | 8,1 | 6,1 | 94 % | 1 | 8 | 8 |
Durée d’action
- Varie de 30 à 180 minutes selon les agents.
- L’adjonction d’adrénaline prolonge l’effet de l’AL.
Indications détaillées
- Applications : Endoscopies, chirurgies, soins dentaires.
- Types d’anesthésie locale :
- Infiltration : Injection dans la zone concernée.
- Conduction : Ciblage des nerfs et du territoire innervé.
- Spinale et péridurale : Anesthésie au niveau de la colonne vertébrale.
Métabolisme
- Esters :
- Hydrolysés dans le plasma, les globules rouges et le foie par des pseudocholinestérases.
- Amides :
- Métabolisés exclusivement par le foie via le cytochrome P450.
Contre-indications absolues
- Hypersensibilité aux anesthésiques locaux.
- Porphyrie.
- Anémie hémolytique.
- Troubles de la conduction cardiaque.
- Hypertension artérielle sévère.
- Épilepsie non contrôlée.
Formes biopharmaceutiques en odontostomatologie
- Transmuqueuse : Anesthésie de surface ou de contact.
- Sous-muqueuse : Anesthésie par infiltration via injection parentérale.
Voie transmuqueuse
- Application : Topique.
- Formes :
- Solides imprégnés d’AL (coton, disque de papier).
- Formes colloïdales (gels, pâtes).
- Formes gazeuses (spray).
Voie sous-muqueuse
- Objectif : Insensibilisation d’un territoire limité (une ou plusieurs dents).
- Conditionnements :
- Flacon : 10 à 50 ml, utilisé en milieu hospitalier.
- Cartouche : 1,7 à 1,8 ml, forme biopharmaceutique de choix.
- Conservateurs : Parabens, sulfites, éthylène-diamine-tétra-acétate (EDTA).
Indications principales des molécules
| Molécule | Indications principales |
|---|
| Articaine | Anesthésie locale ou locorégionale en odontostomatologie |
| Lévobupivacaïne | Anesthésies locale et de conduction (chirurgies des membres inférieurs, urologique, gynécologique, abdominale sous-ombilicale, césarienne) |
| Mépivacaïne | Anesthésie locale d’infiltration et régionale (blocs plexiques et tronculaires, anesthésie péridurale et caudale) |
| Lidocaïne | Anesthésies locale et péridurale |
| Prilocaïne | Anesthésie locale de la peau saine |
| Procaïne | Anesthésie locale d’infiltration et de conduction (blocs plexiques et tronculaires) |
| Ropivacaïne | Anesthésies locale et péridurale |
| Tétracaïne | Kératite pour forme collyre, anesthésie locorégionale |
Lidocaïne (Xylocaïne®)
Caractéristiques
- Anesthésique local de type aminoamide.
- Stabilisation des membranes nerveuses par blocage des flux sodiques entrants.
Indications
- Anesthésies locales ou locorégionales.
- Anesthésies locales par infiltration.
Contre-indications absolues
- Allergie aux aminoamides.
- Porphyrie.
- Troubles de conduction intracardiaque.
- Épilepsie non contrôlée.
- Antécédent d’hyperthermie maligne.
Contre-indications liées aux formes adrénalinées
- Insuffisance coronarienne.
- Troubles du rythme ventriculaire.
- Injection intraveineuse.
- Hypertension artérielle sévère.
- Cardiomyopathie obstructive.
- Hyperthyroïdie.
- Injection au niveau des extrémités.
- Traitement par IMAO ou antidépresseurs tricycliques.
Posologie et mode d’administration
- Concentrations : 0,5 % (5 mg/ml), 1 % (10 mg/ml), 2 % (20 mg/ml).
Effets secondaires
- Cardiovasculaires : Hypotension, bradycardie, troubles du rythme, fibrillation ventriculaire.
- Respiratoires : Dépression respiratoire, apnée.
- Neurologiques : Bourdonnements d’oreille, dysphorie, surdité, convulsions.
- Allergiques : Risque faible.
Surdosage
- Convulsions généralisées, arrêt cardiorespiratoire.
Articaine
Caractéristiques
- Chlorhydrate d’articaine, AL à fonction amide.
- Souvent associé à l’adrénaline pour :
- Ralentir le passage dans la circulation générale.
- Maintenir une concentration tissulaire active prolongée.
- Réduire les saignements au champ opératoire.
Cinétique
- Installation de l’anesthésie : 2 à 3 minutes.
- Durée de l’anesthésie : Environ 60 minutes (2 à 3 fois plus courte pour une anesthésie pulpaire).
Formulations
- Ubistestin 4 %, Ultracaïn 4 %.
Bupivacaïne (Marcaïne®)
Indications
- Anesthésies locales ou locorégionales.
- Blocs centraux et périphériques.
- Infiltrations locales.
Posologie et mode d’administration
- Concentrations : 0,25 % (2,5 mg/ml), 0,5 % (5 mg/ml).
Effets secondaires
- Cardiovasculaires : Hypotension, bradycardie, troubles du rythme, fibrillation ventriculaire, arrêt cardiaque.
- Respiratoires : Dépression respiratoire, apnée.
- Neurologiques : Bourdonnements d’oreille, dysphorie, surdité, convulsions.
- Allergiques : Risque faible.
Surdosage
- Convulsions généralisées, arrêt cardiorespiratoire, troubles du rythme.
Mépivacaïne (Carbocaïne®)
Caractéristiques
- Anesthésique local de type aminoamide.
- Stabilisation des membranes nerveuses par blocage des flux sodiques entrants.
Indications
- Anesthésies locales ou locorégionales.
- Blocs centraux et périphériques.
- Infiltrations locales.
Contre-indications absolues
- Allergie aux aminoamides.
- Porphyrie.
- Troubles de conduction intracardiaque.
- Épilepsie non contrôlée.
- Antécédent d’hyperthermie maligne.
- Injection intravasculaire.
- Nourrisson de moins de 1 mois.
Contre-indications relatives
- Femme enceinte (fœtotoxicité observée chez l’animal).
- Pas d’AMM en France pour les rachianesthésies.
Posologie et mode d’administration
- Concentrations : 1 % (10 mg/ml), 2 % (20 mg/ml).
Effets secondaires
- Cardiovasculaires : Hypotension, bradycardie, troubles du rythme, fibrillation ventriculaire.
- Respiratoires : Dépression respiratoire, apnée.
- Neurologiques : Bourdonnements d’oreille, dysphorie, surdité, convulsions.
- Allergiques : Risque faible.
Surdosage
- Convulsions généralisées, arrêt cardiorespiratoire.
Autres anesthésiques
Doses maximales recommandées
| Anesthésique | Dose maximale |
|---|
| Articaine 4 % + Adrénaline | 7 mg/kg (500 mg) adulte, 5 mg/kg enfant |
| Bupivacaïne 0,5 % + Adrénaline | 2 mg/kg (90 mg) |
| Lidocaïne 2 % + Adrénaline | 7 mg/kg (500 mg) |
| Mépivacaïne 2 % + Lévonordéfrine | 6,6 mg/kg (400 mg) |
| Mépivacaïne 3 % sans vasoconstricteur | 6,6 mg/kg (400 mg) |
| Prilocaïne 4 % avec/sans adrénaline | 8 mg/kg (500 mg) |
Concentrations et contenu des cartouches
| Concentration (%) | mg/mL | mg dans une cartouche de 1,8 mL |
|---|
| 2 % | 20 | 36 mg |
| 3 % | 30 | 54 mg |
| 4 % | 40 | 72 mg |
Exemple de calcul pour un enfant de 15 kg
| Anesthésique | Dose maximale | Concentration | Volume maximal | Nombre maximal de cartouches (1,8 mL) |
|---|
| Lidocaïne | 105 mg | 20 mg/mL | 5,25 mL | 2,9 |
| Prilocaïne | 120 mg | 40 mg/mL | 3 mL | 1,67 |
| Mépivacaïne | 99 mg | 30 mg/mL | 3,3 mL | 1,8 |
| Articaine | 75 mg | 40 mg/mL | 1,88 mL | 1 |
Tableau des doses maximales
| Anesthésique local | Dose maximale | Quantité maximale de cartouches |
|---|
| Lidocaïne | 7 mg/kg (500 mg) | 13 |
| Mépivacaïne | 6,6 mg/kg (500 mg) | 11 |
| Prilocaïne | 8 mg/kg (500 mg) | 7 |
| Bupivacaïne | 2 mg/kg (200 mg) | 8 |
| Articaine | 7 mg/kg (500 mg), 5 mg/kg enfant | 10 (7 enfant) |
Spécificités en chirurgie dentaire
- Risques :
- Passage intravasculaire possible.
- Surdosage si grande quantité nécessaire.
- Proximité du système nerveux central (SNC).
- Vascularisation importante du site.
- Adjonction d’adrénaline.
Complications de l’anesthésie locorégionale (ALR)
- Risque d’intoxication grave : Tous les AL peuvent provoquer des intoxications sévères.
- Mécanismes :
- Passage massif dans la circulation par injection directe (survenue précoce).
- Résorption d’une quantité importante.
- Toxicité relative (par ordre croissant) : Lidocaïne = Mépivacaïne < Ropivacaïne < Lévobupivacaïne << Bupivacaïne.
Causes du surdosage
- Terrain du patient : Insuffisance hépatique.
- Âge et poids : Enfants de 2 à 6 ans (15 à 40 kg).
- Nature de l’AL : Concentration, dose, présence de vasoconstricteurs.
- Quantité administrée.
- État inflammatoire : Vasodilatation et résorption rapide.
- Injection intravasculaire : Absence de test d’aspiration.
Toxicité
- Facteurs influençant la toxicité :
- Type d’agent : Lidocaïne, procaïne, mépivacaïne et ropivacaïne moins toxiques que bupivacaïne.
- Vitesse d’injection.
- Adjonction d’adrénaline : Ralentit la résorption, réduisant la toxicité.
Nombre maximal de cartouches selon le poids
| Poids (kg) | Lidocaïne 2 % | Mépivacaïne 2 % | Mépivacaïne 3 % | Articaine 4 % |
|---|
| 10 | 1,9 | 1,8 | 1,2 | 1 |
| 20 | 3,8 | 3,6 | 2,4 | 1,9 |
| 30 | 5,8 | 5,5 | 3,6 | 2,9 |
| 40 | 7,7 | 7,3 | 4,8 | 3,8 |
| 50 | 9,7 | 9,1 | 6,1 | 4,8 |
| 60 | 11,6 | 11 | 7,3 | 5,8 |
| 65 | 12,6 | 11,1 | 7,4 | 6,3 |
| 70 | 13,8 | 11,1 | 7,4 | 6,8 |
| ≥80 | 13,8 | 11,1 | 7,4 | 6,9 |
Toxicité locale
- Vasodilatation.
- Toxicité neurologique.
- Toxicité musculaire.
Toxicité systémique
Toxicité neurologique
- Signes précoces :
- Paresthésies linguales et péribuccales.
- Lipothymies, acouphènes, vision trouble.
- Agitation, nervosité, paranoïa.
- Troubles de l’élocution, troubles de la conscience.
- Convulsions, dépression respiratoire.
Toxicité cardiaque
- Formes :
- Toxicté neurologique via le système sympathique.
- Toxicité directe.
- Manifestations :
- Troubles de la conduction (bloc auriculo-ventriculaire).
- Troubles du rythme graves, asystolie.
- Dépression myocardique, vasodilatation périphérique, hypotension, collapsus.
- Arrêt cardiocirculatoire.
Allergie
- Rareté : Allergie aux AL exceptionnelle.
- Cause fréquente : Conservateurs (ex. : méthylparaben).
- Terrain allergique : N’est pas une contre-indication absolue.
Traitement des complications
Mesures initiales
- Évaluer la conscience et la ventilation.
- Libérer les voies aéro-digestives supérieures.
- Allonger le patient et surélever les pieds.
- Contacter les secours.
Prise en charge médicale
- Oxygénation.
- Intubation trachéale et ventilation assistée si nécessaire.
- Administration de benzodiazépine ou thiopental pour convulsions.
- Perfusion d’intralipide (20 %, 100-200 ml sur 2 min, répétée si nécessaire).
- Atropine en cas de bradycardie.
- Adrénaline et réanimation cardiopulmonaire en cas d’arrêt.
Précautions d’emploi
Surveillance de base
- Respecter les doses maximales.
- Éviter l’injection dans une zone infectée.
- Respecter les règles d’asepsie pour les formes injectables.
- Injection lente avec test d’aspiration.
- Respecter le site d’injection.
- Utiliser la forme galénique adaptée.
Mesures complémentaires
- Disposer d’un matériel d’anesthésie-réanimation (monitoring de la pression artérielle, ECG).
- Avoir des médicaments appropriés (anticonvulsivants, atropine, myorelaxants).
Conclusion
- Efficacité : Les AL constituent un arsenal analgésique varié et efficace.
- Risques : Nécessité de connaître les complications potentielles.
- Bonnes pratiques : Une maîtrise de la pharmacologie et des règles cliniques est essentielle pour une utilisation sécurisée.
Anesthésiques Locaux – Anesthésiologie Dentaire
Voici une sélection de livres:
Anesthésiques Locaux – Anesthésiologie Dentaire






Leave a Reply