L’Émail Dentaire : Histologie Complète, Structure et Formation
Résumé rapide : L’émail est le tissu le plus dur du corps humain, d’origine épithéliale, formé par les améloblastes. Sa compréhension est essentielle pour les concours d’internat et la pratique clinique quotidienne.
Introduction : Pourquoi l’Émail Est-il au Cœur de l’Odontologie ?
L’émail dentaire est bien plus qu’une simple enveloppe protectrice. C’est un tissu unique, acellulaire après sa formation, incapable de se régénérer par lui-même, ce qui en fait l’un des sujets les plus cruciaux de l’histologie dentaire. Sa destruction — qu’elle soit d’origine carieuse, érosive ou traumatique — est définitive, d’où l’importance absolue de comprendre sa structure pour mieux le préserver.
Pour l’étudiant en odontologie, maîtriser l’histologie de l’émail, c’est poser les bases de la cardiologie, de l’endodontie, de la prothèse et de l’esthétique dentaire. Ce guide complet reprend l’ensemble des données histologiques fondamentales, enrichi de mises en contexte clinique, d’erreurs fréquentes et de cas commentés.
1. Définition et Origine de l’Émail Dentaire
L’émail est le tissu calcifié d’origine épithéliale qui recouvre les couronnes dentaires. Il résulte de la minéralisation du substrat organique synthétisé et sécrété par les améloblastes, cellules issues de l’épithélium adamantin interne (EAI).
Contrairement aux autres tissus minéralisés du corps (os, dentine, cémentum), l’émail est d’origine ectodermique et non mésenchymateuse. Cette particularité explique pourquoi il est définitivement formé après l’éruption dentaire : les améloblastes dégénèrent une fois leur mission accomplie.
2. Propriétés Physiques de l’Émail
La connaissance des propriétés physiques de l’émail est indispensable pour comprendre ses comportements cliniques face aux forces occlusales, aux agents chimiques et aux procédures restauratrices.
Dureté et Fragilité
L’émail est le tissu dentaire le plus dur du corps humain (environ 5 sur l’échelle de Mohs). Cette dureté exceptionnelle lui permet de résister à l’abrasion masticatoire. Cependant, il est cassant, particulièrement lorsqu’il n’est pas soutenu par la dentine sous-jacente. C’est pourquoi les fractures émail sans soutien dentinaire sont fréquentes lors de traumatismes.
Vulnérabilité Chimique
L’émail est vulnérable aux attaques acides. Un pH inférieur à 5,5 (pH critique de dissolution de l’hydroxyapatite) entraîne la déminéralisation de surface. Les boissons gazeuses, les jus de fruits et le reflux gastro-œsophagien sont des ennemis directs de l’émail. Sur le plan clinique, l’utilisation de dentifrices reminéralisants comme le Biomed Calcimax à 97% naturel peut contribuer à la protection de la surface amélaire entre deux consultations.
Couleur et Translucidité
Sa couleur varie généralement du jaune au gris. L’émail est semi-translucide : l’apparence visuelle de la dent est fortement influencée par la couleur de la dentine ou des matériaux de restauration sous-jacents. C’est ce qui explique pourquoi les dents à dentine fortement teintée paraissent jaunes même avec un émail intact.
Autres Propriétés Physiques Clés
- L’émail sain est lisse et brillant.
- Il est moins fluorescent que la dentine.
- Sa densité est plus élevée dans la zone externe que dans la zone interne.
- Son épaisseur est maximale dans la zone occlusale (> 2,5 mm) et diminue progressivement vers le collet dentaire.
- Il est plus radio-opaque que les autres tissus dentaires, ce qui permet de le distinguer facilement sur les radiographies.
3. Formation de l’Émail : L’Amélogenèse
L’amélogenèse est le processus de formation de l’émail, orchestré par les améloblastes. Ce processus se déroule en plusieurs étapes précises et séquentielles.
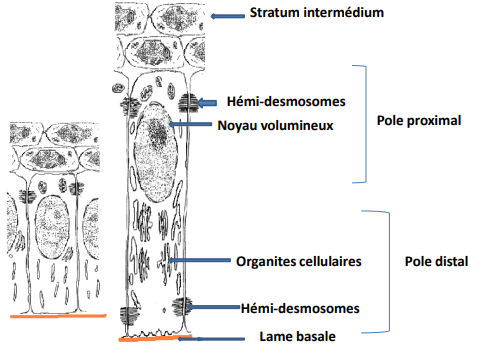
3.1 Histo-différenciation de l’Améloblaste Pré-sécréteur
Le pré-améloblaste s’allonge, son noyau migre vers le pôle proximal (proche du stratum intermedium), et les organites cytoplasmiques s’accumulent au pôle distal, en contact avec la membrane basale. Les cellules sont unies par des desmosomes aux deux pôles et par des fibres intermédiaires formant des toiles terminales (terminal web). Ainsi, l’améloblaste pré-sécréteur acquiert les caractéristiques d’une cellule sécrétrice typique.
3.2 Disparition de la Membrane Basale et Formation du Manteau Dentinaire
La membrane basale est dégradée par les métalloprotéases odontoblastiques, et ses fragments résiduels sont phagocytés par les améloblastes pré-sécréteurs. Cela conduit à la formation du manteau dentinaire, qui peut induire l’amélogenèse — c’est le signal de départ de la sécrétion amélaire.
3.3 Améloblaste Sécréteur sans Prolongement de Tomes — Émail Aprismatique Interne

La cellule accentue sa polarisation et dépose les protéines de l’émail directement sur le manteau dentinaire, formant l’émail aprismatique interne, d’une épaisseur d’environ 10 µm.
3.4 Formation de la Couche Papillaire
Les cellules du réticulum étoilé disparaissent par apoptose, entraînant un “collapsus” entre l’épithélium adamantin externe (EAE) et le stratum intermedium (SI), formant la couche papillaire. Ce rapprochement permet aux vaisseaux du follicule dentaire d’assurer la nutrition des améloblastes sécréteurs actifs.
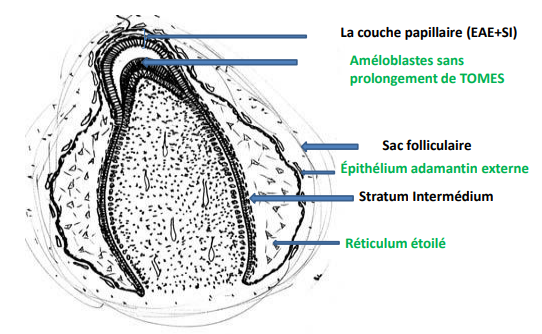
3.5 Améloblaste avec Prolongement de Tomes — Émail Prismatique Immature
Les améloblastes forment un prolongement conique appelé prolongement de Tomes à leur pôle distal. Les granules de sécrétion de l’émail sont acheminés vers deux sites :
Site de sécrétion proximal — Substance inter-prismatique : sécrétée par plusieurs améloblastes voisins, servant de moule contenant le prolongement de Tomes, donnant une apparence en dents de scie à la jonction émail-améloblaste.
Site de sécrétion distal — Prismes : chaque améloblaste sécrète un prisme à partir de l’émail aprismatique interne jusqu’à la surface de l’émail, chaque prisme traversant toute l’épaisseur de l’émail. Cet émail immature contient une forte fraction protéinique : les amélogénines.
3.6 Améloblaste de Maturation — Émail Mature
Les améloblastes réduisent leur taille, le nombre d’organites de synthèse diminue, et ils s’élargissent. Ils alternent cycliquement entre une bordure plissée (80 %) et lisse (20 %) à leur pôle distal, permettant :
- La balance entre acidification et neutralisation du pH de l’émail.
- L’élimination des fragments protéiques.
- Le transport du calcium pour la croissance des cristaux.
À la fin de la maturation, l’émail mature est composé de 96 % de cristaux, 3,2 % d’eau et 0,8 % de matières organiques. Un cristal initial de 3,1 nm d’épaisseur atteint 29 nm, et une largeur de 25 nm passe à 65 nm après maturation complète.
3.7 Améloblaste de Protection
L’améloblaste devient cubique, avec une diminution importante des organites cellulaires. Il sécrète une lame basale à la surface de l’émail, à laquelle il adhère par des hémidesmosomes. Les améloblastes de protection se confondent avec la couche papillaire (EAE + SI), formant l’épithélium adamantin réduit (EAR), qui isole l’émail du follicule dentaire avant l’éruption de la dent.
4. Produits de Synthèse de l’Améloblaste — La Matrice Amélaire
4.1 Protéines Non Amélogéniques : Améloblastine, Énaméline, Tuftéline
Elles représentent 10 % des protéines de l’émail. Elles initient la nucléation des cristaux, guident leur forme hexagonale et favorisent leur formation. La tuftéline joue un rôle particulier au niveau des touffes d’émail, zones de moindre minéralisation.
4.2 Les Amélogénines
Constituant 90 % des protéines de l’émail en formation, elles sont riches en proline (25-30 %), glutamine, leucine et histidine. Elles contrôlent l’orientation des cristaux, maintiennent leur espacement uniforme et confèrent une disposition régulière dans l’émail immature. Leur dégradation au stade de maturation est indispensable à la résistance finale de l’émail.
4.3 Les Protéases
Au stade de maturation, les protéases (notamment la MMP-20 et la kallikréine-4) dégradent les nanosphères d’amélogénines, permettant la croissance en épaisseur et en longueur des cristaux, ce qui confère à l’émail mature une résistance accrue grâce à sa forte minéralisation.
5. Structure Microscopique de l’Émail
5.1 Unité de Base : Le Cristallite
Le cristallite est un monocristal d’hydroxyapatite, de composition chimique proche de Ca₁₀(PO₄)₆(OH)₂, mesuré en nanomètres. Une coupe perpendiculaire à son axe révèle une section hexagonale ou rhomboédrique, composée d’environ 2 100 cristaux. Sa hauteur varie de 2 000 à 10 000 Å, pouvant atteindre 1 à 2 mm, voire traverser totalement l’émail.
5.2 Émail Aprismatique Interne
Situé en contact avec la dentine, c’est l’émail le moins minéralisé, formé de cristaux parallèles et perpendiculaires à la jonction amélo-dentinaire (JAD). Cette jonction présente des crêtes augmentant l’adhésion, plus prononcées dans la région coronale où le stress occlusal est élevé.
5.3 Émail Prismatique
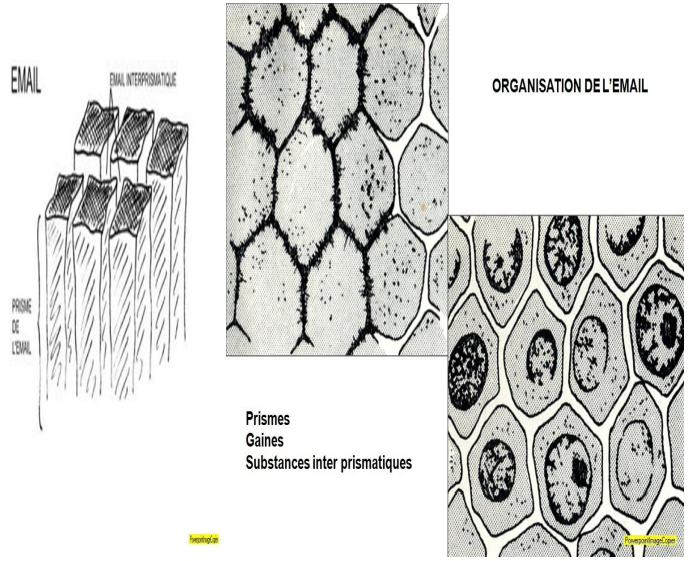
Il constitue la majeure partie de l’émail et se compose de deux structures :
Les prismes (4 à 8 µm) : cordons d’émail minéralisé traversant l’émail de la JAD jusqu’à la surface, formés de cristaux d’hydroxyapatite entourés d’une gaine organique, sécrétés par le pôle distal du prolongement de Tomes.
La substance inter-prismatique : même composition que les prismes mais avec une orientation différente des cristallites. Dans les prismes, les cristallites sont disposés en éventail (milliers de cristallites), tandis que dans la substance inter-prismatique, une centaine de cristallites forme un réseau distinct.
5.4 Gaine de l’Émail
C’est une substance moins minéralisée située entre les prismes et la substance inter-prismatique. Elle constitue un point de fragilité relatif, exploité lors du mordançage acide en prothèse et en collage.
5.5 Émail Aprismatique Externe
Situé à la surface externe, c’est l’émail le plus minéralisé (96 % de matrice minérale), formé au stade de maturation, avec des cristaux parallèles. C’est cette couche qui est la plus résistante aux agressions extérieures.
6. Structures Particulières de l’Émail
6.1 Bandes de Hunter-Schreger
Décrites par John Hunter (1771) et Christian Heinrich Theodore Schreger, ces bandes apparaissent dans la zone interne de l’émail après coloration par des colorants cationiques (ex. : bleu Alcian). Les diazonies (sombres, prismes sectionnés transversalement) alternent avec les parazonies (claires, prismes orientés longitudinalement), sans différence de composition. Leur rôle est de dissiper les contraintes mécaniques lors de la mastication.
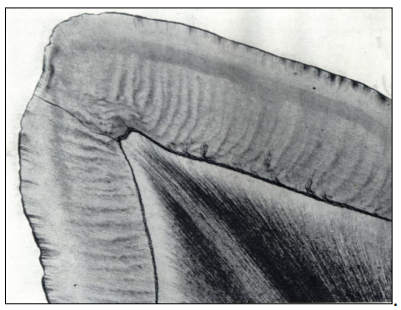
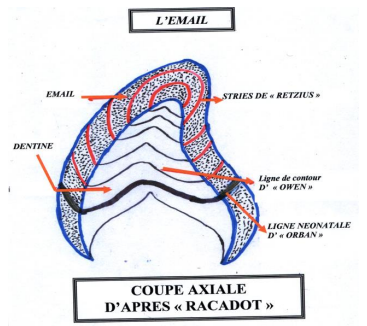
6.2 Stries de Retzius
Observées sur des coupes d’émail non déminéralisé, ces lignes brunâtres représentent des régions moins calcifiées, probablement dues à un ralentissement périodique de la formation de l’émail (rythme circadien de l’amélogenèse). En coupe longitudinale, elles forment des périkymaties (sillons parallèles au collet, espacés de 35 à 50 µm, parfois jusqu’à 100 µm). En coupe transversale, elles apparaissent comme des cercles concentriques, similaires aux lignes de croissance des arbres. Cliniquement, les périkymaties s’effacent avec l’abrasion physiologique liée à l’âge.
6.3 Émail Noueux
Dans la région superficielle, les prismes sont rectilignes, mais près de la dentine, leur orientation tortueuse donne un aspect noueux, rappelant les nœuds de bois. Cette organisation complexe augmente la résistance à la fracture dans les zones à forte contrainte.
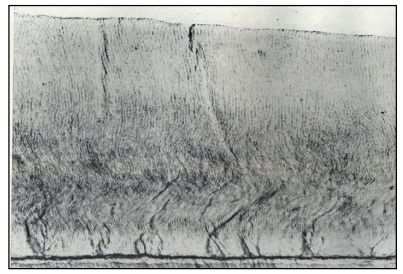
6.4 Buissons de l’Émail (Enamel Tufts)
Ce sont des zones mal minéralisées, remplies de substances organiques colorables, partant de la jonction émail-dentine et s’épanouissant vers la surface, à la manière de touffes d’herbe. Ils représentent des zones de moindre résistance structurale.
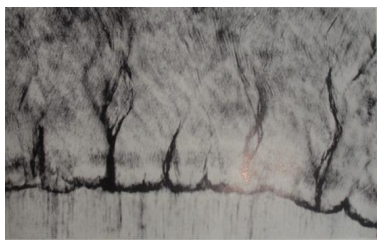
6.5 Lamelles de l’Émail (Enamel Lamellae)
Ces structures non minéralisées, riches en protéines (cytokératines), s’étendent de la surface de l’émail vers la dentine. Longtemps considérées comme des portes d’entrée pour les microbes, les données actuelles infirment ce rôle dans la pathogenèse carieuse.
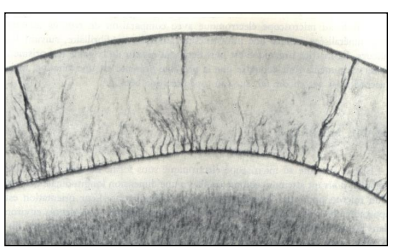
6.6 Fuseaux (Enamel Spindles)
Ce sont les portions terminales des fibres de Tomes des odontoblastes, fréquemment observées près de la dentine. Ils témoignent de la proximité fonctionnelle entre odontoblastes et améloblastes au cours de l’odontogenèse.
6.7 Cuticules de Nasmyth
Après l’éruption dentaire, l’émail est recouvert d’une pellicule amorphe translucide, appelée pellicule de Nasmyth (ou cuticule primaire), reliquat des améloblastes dégénérés formant une couche kératinisée. Lors de l’éruption, l’épithélium gingival forme une cuticule secondaire kératinisée. Après l’éruption, ces cuticules disparaissent, mais une pellicule acquise, issue de la salive, se forme, constituant le premier stade de la plaque bactérienne.
7. Tableau Récapitulatif — Structures Histologiques de l’Émail
Pour visualiser en un coup d’œil les différences entre les principales structures histologiques de l’émail, voici un tableau synthétique particulièrement utile pour la révision des concours.
| Structure | Localisation | Minéralisation | Origine | Rôle principal |
|---|---|---|---|---|
| Émail aprismatique interne | Contact JAD | Faible | Améloblaste sans prolongement | Base de l’amélogenèse |
| Émail prismatique | Zone centrale | Élevée | Prolongement de Tomes | Résistance mécanique principale |
| Émail aprismatique externe | Surface coronaire | Très élevée (96%) | Stade de maturation | Protection de surface maximale |
| Gaine de l’émail | Entre prismes et subs. inter-prismatique | Faible | — | Zone de mordançage acide |
| Buissons de l’émail | JAD → surface | Très faible | Défaut de minéralisation | Zone de faiblesse structurale |
| Lamelles de l’émail | Surface → dentine | Nulle (organiques) | Cytokératines | Artefact / rôle pathologique limité |
| Bandes Hunter-Schreger | Zone interne | Normale | Orientation des prismes | Dissipation des contraintes |
| Stries de Retzius / périkymaties | Toute l’épaisseur | Légèrement réduite | Rythme circadien | Marqueurs chronologiques de croissance |
| Fuseaux | Jonction JAD | Variable | Extensions odontoblastes | Témoin de l’odontogenèse |
8. Erreurs Fréquentes à Éviter en Histologie de l’Émail
Cette section s’adresse directement aux étudiants préparant leurs examens ou leur internat. Ces erreurs reviennent régulièrement dans les copies et les QCM.
Erreur 1 — Confondre l’origine de l’émail avec celle de la dentine
L’émail est d’origine épithéliale (ectodermique), alors que la dentine est d’origine mésenchymateuse (odontoblastes issus des cellules de la crête neurale). Confondre les deux lors d’un QCM de biologie du développement est une faute éliminatoire. Bonne pratique : mémoriser le couple “épithélium → émail” et “mésenchyme → dentine”.
Erreur 2 — Croire que l’émail peut se régénérer après l’éruption
Les améloblastes dégénèrent après l’éruption dentaire. L’émail est donc acellulaire et incapable d’autoréparation biologique. Toute perte d’émail est définitive. En clinique, cela justifie les stratégies préventives et l’usage de dentifrices protecteurs comme le Sensodyne Sensibilité & Gencives, particulièrement indiqué chez les patients présentant une érosion amélaire active.
Erreur 3 — Inverser les rôles des sites de sécrétion du prolongement de Tomes
Le pôle distal du prolongement sécrète les prismes ; le pôle proximal sécrète la substance inter-prismatique. Beaucoup d’étudiants inversent ces deux sites. Mnémotechnique : le prolongement pointe vers le prisme (D comme distal, D comme “droit vers le prisme”).
Erreur 4 — Considérer les lamelles de l’émail comme des voies d’entrée bactériennes
Cette ancienne conception est réfutée par les données actuelles. Les lamelles, bien que non minéralisées, ne constituent pas des portes d’entrée démontrées pour les bactéries cariogènes. Une copie qui maintient cette affirmation risque d’être pénalisée.
Erreur 5 — Négliger la différence entre diazonies et parazonies
Les diazonies (sombres) correspondent à des prismes en coupe transversale, les parazonies (claires) à des prismes en coupe longitudinale. Ces deux zones alternent dans les bandes de Hunter-Schreger et n’ont pas de différence de composition chimique — uniquement d’orientation.
Erreur 6 — Confondre la pellicule de Nasmyth et la pellicule acquise salivaire
La pellicule de Nasmyth est d’origine améloblastique (pré-éruptive), tandis que la pellicule acquise est d’origine salivaire (post-éruptive). La première disparaît après l’éruption. La seconde constitue le premier stade de la plaque bactérienne.
9. Cas Cliniques Commentés
Cas Clinique 1 — Érosion amélaire chez une jeune adulte
Présentation : Léa, 24 ans, consulte pour des sensibilités dentaires généralisées et une modification de l’aspect de ses dents antérieures qu’elle décrit comme “plus transparentes au bord”. Elle consomme 2 à 3 canettes de boisson énergétique par jour et souffre de reflux gastro-œsophagien non traité.
Problématique : L’interrogatoire et l’examen clinique révèlent une érosion amélaire généralisée, plus marquée sur les faces palatines des incisives supérieures (érosion intrinsèque liée au reflux) et sur les faces vestibulaires (érosion extrinsèque liée aux acides alimentaires). La translucidité au bord incisif est pathognomonique de la perte d’émail aprismatique externe.
Prise en charge : Orientation vers le médecin généraliste pour traiter le reflux. Conseils diététiques stricts (suppression des acides). Prescription d’un dentifrice reminéralisant à haute teneur en fluorure ou à hydroxyapatite. Surveillance rapprochée tous les 6 mois.
Point clé illustré : L’émail est acellulaire et irréversiblement perdu une fois érodé. La prévention et la détection précoce sont les seuls outils efficaces.
Cas Clinique 2 — Fluorose et aspect de l’émail
Présentation : Karim, 16 ans, adressé pour un bilan esthétique. Il présente des taches blanches opaques et des stries brunâtres sur la quasi-totalité des couronnes, sans historique de traumatisme. L’enfant a grandi dans une région à forte teneur en fluor dans l’eau potable.
Problématique : Le tableau clinique est cohérent avec une fluorose dentaire modérée. L’excès de fluor pendant l’amélogenèse perturbe l’activité des protéases, entraînant une rétention des fragments d’amélogénines dans la matrice et une hypominéralisation de l’émail mature. Les zones blanches correspondent à une porosité sub-surfacique, les zones brunâtres à une incorporation de pigments exogènes dans les défauts.
Prise en charge : Microabrasion amélaire pour les formes légères à modérées, suivie d’un polissage de surface. Pour les formes sévères avec perte de substance : restaurations composites ou facettes. Information du patient sur l’irréversibilité des lésions.
Point clé illustré : Les protéases jouent un rôle majeur dans la maturation de l’émail — leur inhibition (par excès de fluor) perturbe directement la structure finale et la minéralisation.
Cas Clinique 3 — Fracture d’émail non soutenu
Présentation : Marc, 35 ans, consulte en urgence après avoir mordu dans un noyau d’olive. Il présente une fracture coronaire sur la cuspide mésio-vestibulaire de la première molaire supérieure droite, avec un fragment d’émail décollé mais sans exposition dentinaire ni pulpaire.
Problématique : L’examen révèle une préparation ancienne (obturation centrale) qui a laissé de l’émail non soutenu par la dentine sur la cuspide. Ce type de configuration est une indication classique de la fragilité de l’émail non soutenu : sans la dentine sous-jacente pour absorber les contraintes de flexion, l’émail, bien que dur, se fracture de manière fragile.
Prise en charge : Retrait du fragment, polissage des berges, évaluation de la vitalité pulpaire. Recontourage composite ou indication d’un onlay selon l’étendue tissulaire résiduelle.
Point clé illustré : La dureté de l’émail ne signifie pas une résistance à la flexion. Le couple émail-dentine est solidaire — l’un sans l’autre perd ses propriétés biomécaniques optimales.
10. Foire Aux Questions (FAQ) — Histologie de l’Émail Dentaire
Quelle est la composition chimique exacte de l’émail mature et comment évolue-t-elle au cours de la maturation ?
L’émail immature contient une forte proportion de protéines (amélogénines notamment). Après maturation complète, l’émail atteint une composition de 96 % de cristaux d’hydroxyapatite, 3,2 % d’eau et 0,8 % de matières organiques. Ce processus implique la dégradation enzymatique des protéines matricielles et le transport actif du calcium pour permettre la croissance des cristaux.
Pourquoi l’émail ne peut-il pas se régénérer après l’éruption dentaire ?
Parce que les améloblastes dégénèrent au moment de l’éruption, après avoir formé l’épithélium adamantin réduit. Aucune cellule du tissu dentaire érupté n’est capable de produire de nouveaux cristaux d’hydroxyapatite amélaire. Seule une reminéralisation superficielle partielle est possible par les ions calcium et phosphate salivaires ou fluorures.
Quelle est la différence entre émail prismatique et émail aprismatique ?
L’émail aprismatique (interne et externe) est formé de cristaux orientés parallèlement, sans organisation en prismes. L’émail prismatique, qui constitue la majeure partie de l’émail, est organisé en prismes de 4 à 8 µm traversant toute l’épaisseur de l’émail depuis la JAD. L’émail aprismatique externe est paradoxalement le plus minéralisé des deux types.
Qu’est-ce que le prolongement de Tomes et quel est son rôle précis dans la formation de l’émail ?
Le prolongement de Tomes est une extension conique du pôle distal de l’améloblaste sécréteur. Son pôle distal sécrète les prismes, son pôle proximal sécrète la substance inter-prismatique. C’est donc un double site de sécrétion qui permet la construction simultanée des deux composantes structurales de l’émail prismatique.
Quelle est la signification clinique des stries de Retzius et des périkymaties ?
Les stries de Retzius reflètent les variations périodiques de la vitesse d’amélogenèse (rythme circadien). En surface, elles forment les périkymaties, visibles sur les jeunes dents non abrasées. Cliniquement, un stress métabolique important (fièvre élevée, malnutrition) pendant l’amélogenèse produit une strie accentuée, appelée ligne néonatale chez les dents présentes à la naissance.
Comment différencier la fluorose d’une hypominéralisation molaire-incisive (MIH) à l’examen clinique ?
La fluorose touche toutes les dents éruptées pendant la période d’exposition au fluor, avec une distribution symétrique et des opacités blanches diffuses. La MIH est asymétrique, affecte principalement les premières molaires permanentes et les incisives, avec des opacités bien délimitées, jaunes à brunes, et une tendance aux fractures post-éruptives. L’anamnèse et la distribution des lésions sont les clés du diagnostic différentiel.
Pourquoi le mordançage acide est-il efficace pour le collage sur l’émail ?
Le mordançage à l’acide orthophosphorique (35-37 %) dissout préférentiellement les prismes ou la substance inter-prismatique selon leur orientation, créant des microporosités à la surface. Ces anfractuosités permettent la pénétration de la résine adhésive et la formation de tags de résine, assurant une rétention micromécanique. La gaine de l’émail (moins minéralisée) est particulièrement sensible à cet effet.
Peut-on reminéraliser l’émail érodé avec un dentifrice ou un bain de bouche ?
Partiellement. La reminéralisation n’est possible qu’à un stade très précoce (lésion en “tache blanche” sub-surfacique), lorsque la couche superficielle est encore intacte. Une perte de substance macroscopique (cavitation) ne peut pas être reminéralisée et nécessite une restauration. Un bain de bouche fluoré sans alcool comme le Listerine Total Care 0% alcool peut contribuer à maintenir un environnement oral favorable à ce processus de reminéralisation précoce.
11. Ressources Complémentaires pour Aller Plus Loin
Pour les étudiants souhaitant approfondir leurs connaissances en histologie et en odontologie clinique :
- Guide clinique d’odontologie — la référence pratique pour relier histologie et clinique au quotidien.
- Annales corrigées de l’internat en odontologie 2022-2024 — indispensable pour s’entraîner sur des QCM en contexte d’examen.
- Référentiel internat en parodontologie — pour les aspects cliniques liés aux tissus de soutien et à la jonction amélo-cémentaire.
La plateforme ResiDentaire™ propose également des QCM en ligne spécialement conçus pour les étudiants en médecine dentaire, avec des modules dédiés à l’histologie.
Conclusion — Ce Qu’il Faut Absolument Retenir sur l’Émail
L’émail dentaire est un tissu d’exception : le plus dur du corps humain, formé une seule fois, irremplaçable et irrémédiablement perdu s’il est détruit. Sa compréhension histologique est la clé pour comprendre les mécanismes de la carie, de l’érosion et de l’hypominéralisation, justifier les protocoles de mordançage et d’adhésion en dentisterie restauratrice, expliquer aux patients pourquoi la prévention est irremplaçable, et réussir les QCM d’histologie en internat.
Les points essentiels à maîtriser : l’origine épithéliale de l’émail, les étapes de l’amélogenèse, le rôle du prolongement de Tomes, la composition des cristaux d’hydroxyapatite, et les structures particulières (Hunter-Schreger, Retzius, buissons, lamelles, fuseaux, Nasmyth).
Cette page contient des liens d’affiliation Amazon. En cliquant dessus, vous n’êtes pas tenu de vous procurer les produits suggérés, mais si vous le faites, cela ne vous coûte rien de plus, et cela m’aide à financer ce site.



[…] pénètrent dans la pulpe par les orifices apicaux sous forme de faisceaux myélinisés. Elles cheminent dans le canal radiculaire parallèlement aux axes vasculaires, se subdivisent en […]